6 итог по патшизе. Вариант 4 Виды расстройств функции эндокринных желез, их характеристика. Типы гормональных эффектов, их харка
 Скачать 6.14 Mb. Скачать 6.14 Mb.
|
|
2. Взаимодействие между гипофизом и железами-"мишенями" – основано на прямой положительной (стимулирующей) связи и обратной отрицательной (тормозящей) и носит также название "плюс-минус-взаимодействие". Например, аденогипофиз выделяет АКТГ, оказывающий стимулирующее действие на кору надпочечников и выделение кортизола, который, в свою очередь, тормозит секрецию АКТГ. Этот принцип является основой саморегуляции активности эндокринной системы и обеспечивает поддержание эндокринного гомеостаза (рис. 3). 3. Нервный контроль эндокринной активности. Осуществляется через гипоталамус. Основные пути: парааденогипофизарный (нервно-проводниковый), реализуемый через симпатические и парасимпатические нервы желез; трансгипофизарный, включающий гипоталамические факторы (гормоны) и гуморальный контроль функций аденогипофиза. Известные транспортные системы, обеспечивающие движение БАВ в гипофиз: выделение в портальную систему гипофиза гипоталамических факторов, активирующих (либерины) или угнетающих (статины) гормонопоэз в передней доле гипофиза (табл. 2); аксональный транспорт – перенос нейрогормонов (вазопрессина и окситоцина) из нейросекреторных ядер (супраоптического и паравентрикулярного) в заднюю долю гипофиза. 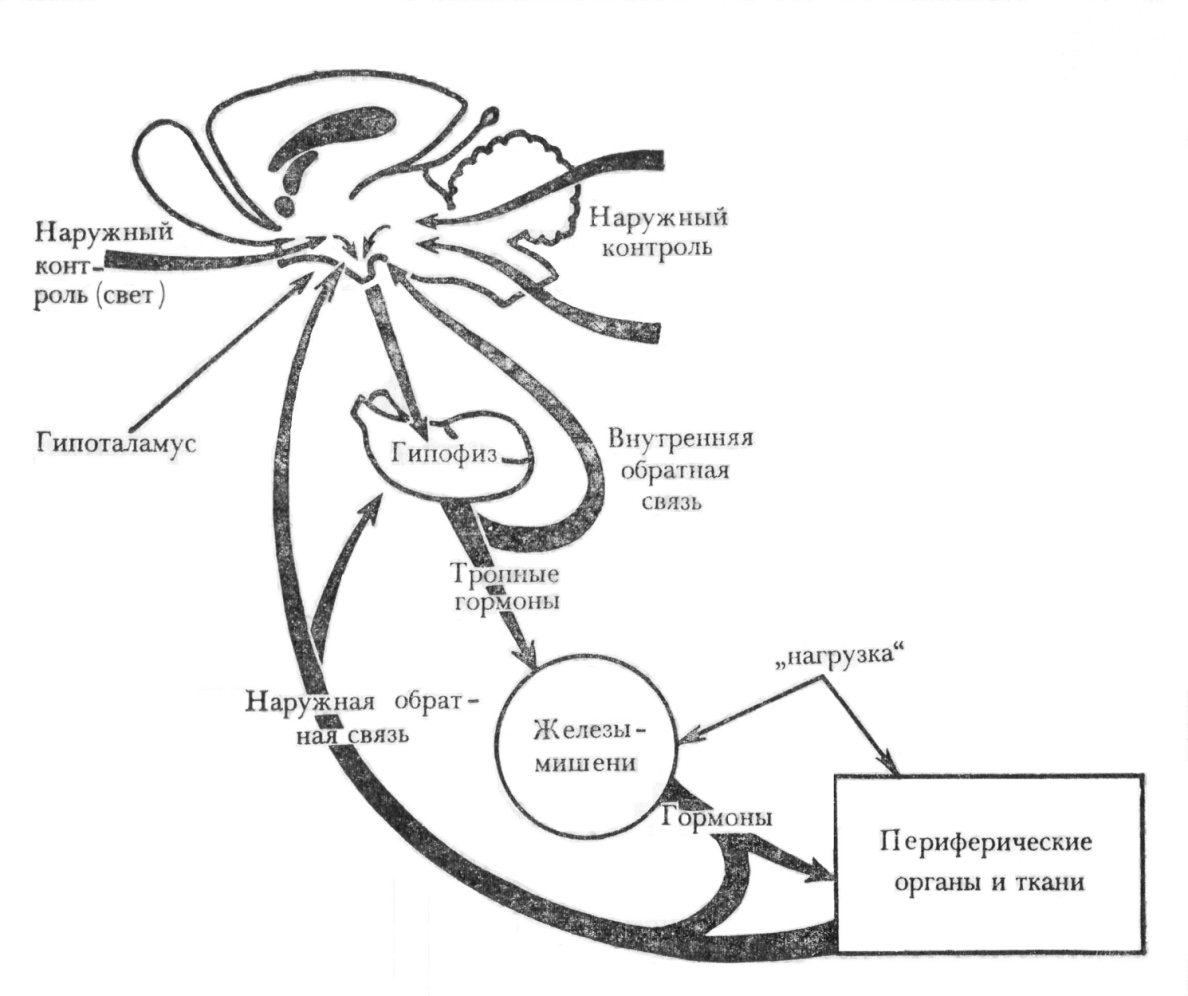 Гипоталамическая регуляция функций аденогипофиза контролируется отрицательной обратной связью. Например, кортиколиберин увеличивает секрецию АКТГ, который тормозит активность гипоталамических клеток, продуцирующих кортиколиберин. В системе регуляции активности длинных эндокринных осей "гипоталамус-гипофиз-железа-мишень" эта петля обратной связи носит название "короткой петли". Второй вариант регуляции активности такой же оси – "длинная петля" обратной связи, т.е. взаимодействие между гипоталамусом и железой-мишенью, основанное на существовании чувствительности гипоталамических нейронов, продуцирующих соответствующий рилизинг-фактор, к гормону соответствующей железы-мишени. Все эти взаимодействия обеспечивают поддержание эндокринного гомеостаза. 4. Внешний контроль. В нем принимают участие лимбические структуры, старая и новая кора, через которые осуществляются воздействия из внешней среды (холод, тепло, свет, факторы, вызывающие психическое и эмоциональное напряжение, и т.д.). Внешний контроль переводит эндокринную систему на иной функциональный уровень, соответствующий новым потребностям организма, т.е. адаптацию к меняющимся условиям внешней среды Мужский гипер и гипо гонадизм. Причины и мех-мы развития. Гипогонадизм (гипофункция половых желез) проявляется либо угнетением функции семенных канальцев без нарушения продукции андрогенов, либо недостаточным образованием этих гормонов, либо сочетанием обоих процессов. Кастрация. Наиболее полные проявления гипогонадизма развиваются после удаления половых желез. Кастрация в препубертатном периоде предупреждает развитие придаточных половых органов и вторичных половых признаков. Эта же операция после завершения развития сопровождается атрофией придаточных половых органов (семенных пузырьков, предстательной железы, препуциальных желез и др.) и вторичных половых признаков, уменьшается масса мышц, и в них откладывается большое количество жира. Кости становятся более тонкими и длинными. Задерживается инволюция вилочковой железы. Гипофиз гипертрофируется, и в нем появляются так называемые клетки кастрации. В связи с выпадением тормозящего влияния андрогенов усиливается выделение гипофизом гонадотропных гормонов (рис. 20- 19). У лиц, кастрированных до наступления половой зрелости, развивается евнухоидизм. При этом происходит чрезмерный рост костей в длину с запаздыванием заращения эпифизарных поясков. Это ведет к относительному увеличению длины конечностей. Наружные половые органы недоразвиты. Наблюдается скудный рост волос на теле и лице с женским типом оволосения на лобке. Мышцы недостаточно развиты и слабы, тембр голоса высокий. Распределение жира и строение таза имеют черты, свойственные женскому организму (рис. 20-20, 20-21). Половое влечение (либидо) и способность к половому акту (потенция) отсутствуют. При кастрации зрелых мужчин изменения менее резки, так как рост, формирование скелета и половых органов уже закончились. Гипергонадизм (усиление функции семенных желез) в препубертатном периоде приводит к преждевременному созреванию. Усиление функции семенников может быть вызвано: 1) повышением секреции гонадотропинов, как правило, в связи с патологическими процессами в гипоталамусе (воспалительные процессы, опухоли области серого бугра); 2) опухолями, исходящими из клеток Лейдига. Ранняя секреция андрогенов приводит к преждевременному развитию половых органов, лонного оволосения и полового влечения. Сначала мальчик быстро растет, а затем происходит задержка роста в результате преждевременного окостенения эпифизарных хрящей. В случаях преждевременного созревания, вызванного ранней секрецией гонадотропинов, стимулируется образование как андрогенов, так и сперматозоидов в семенных канальцах. При опухолях, исходящих из клеток Лейдига, образуются только андрогены. При этом угнетается сперматогенез, так как отсутствует секреция гонадотропинов и в первую очередь фолликулостимулирующего гормона. Роль синаптической стимуляции в повреждении нейронов. Роль процессов внутриклеточной сигнализации в нарушении деятельности нейрона. А)Возбуждающая синаптическая стимуляция может играть важную роль в развитии патологии нейрона. Усиленная и длительная синаптическая стимуляция сама по себе вызывает функциональное перенапряжение нейрона, которое может завершиться дегенерацией внутриклеточных структур. Эти повреждения усиливаются при нарушениях микроциркуляции и мозгового кровообращения, действии токсических факторов. Первостепенное значение синаптическая стимуляция имеет при развитии аноксических (ишемических) повреждений. Культура тканей нейронов становится чувствительной к аноксии лишь после установления синаптических контактов между нейронами. Синаптическая стимуляция реализуется через действие возбуждающих аминокислот (глутамат, аспартат, L-гомоцистеинат), причем эти повреждения подобны тем, которые возникают при ишемии и связаны с увеличенным содержанием внутриклеточного Са2+ . Этот эффект известен как нейротоксическое (или цитотоксическое) действие возбуждающих аминокислот. С синаптической гиперактивацией, действием возбуждающих аминокислот и гипоксией связаны повреждение и гибель нейронов при эпилептическом статусе и в постишемическом периоде. При этом к патогенному действию указанных факторов присоединяется энергетический дефицит. В связи с изложенным становятся понятными благоприятные эффекты (т.е. ослабление синаптического воздействия) уменьшения функциональной нагрузки, предотвращение дополнительных раздражений, «охранительное», по И.П. Павлову, торможение обратимо поврежденных нейронов. Б) После восприятия рецептором сигнала (связывания рецептором нейромедиатора, гормона и др.) в нейроне возникает каскад цепных метаболических процессов, обеспечивающих необходимую активность нейрона. Важную роль в этих процессах играют так называемые усилительные, или пусковые, ферменты и образующиеся под их влиянием вещества- посредники, вторичные мессенджеры (см. главу 20). Совокупность каскадных мембранных и внутриклеточных процессов составляет эндогенную усилительную систему нейрона, которая может обеспечить многократное усиление входного сигнала и возрастание его эффекта на выходе из нейрона. Так, каскад метаболических процессов аденилатциклазного пути может усилить эффект стимула в 107 -108 раз. Благодаря этому возможны выявление и реализация слабого сигнала, что имеет особое значение в условиях патологии, при нарушении синаптического проведения. Многие изменения функций нейрона связаны с действием патогенных агентов на определенные звенья систем внутриклеточной сигнализации. Фармакологическая коррекция деятельности нейрона и эффекты лечебных средств также реализуются через соответствующие изменения этих систем. Так, холерный и коклюшный токсины действуют на процессы, связанные с активностью мембранных G-белков, активирующих или угнетающих аденилатциклазу. Ксантины (теофиллин, кофеин) обусловливают накопление цАМФ, что приводит к усилению деятельности нейрона. При действии ряда противосудорожных препаратов (например, дифенилгидантоина, карбамазепина, бензодиазепинов) и психотропных средств (например, трифтазина) угнетаются разные пути фосфорилирования белков, благодаря чему снижается активность нейронов. Ионы лития, применяемые при лечении некоторых эндогенных психозов, ослабляют деятельность системы фосфоинозитидов. С усиленным входом Са2 + связана эпилептизация нейронов, блокада этого входа антагонистами Са2 + подавляет эпилептическую активность. Общие проявления невротическх состояний. Клинические фазы (стадии) развития невроза. Неврастения:причины,стадии проявления. Стадии: 1. Гиперстеническая – повышенная реактивность, раздражительность (быстро вспыхивает, быстро сгорает). 2. Гипостеническая – снижение силы нервных процессов. 3. Астеническая – ослабление нервных процессов, адинамичность и т.д.   Вариант 17. 1) Процессы составляющие эндокринную функцию, их сущность и значение. Генетически обусловленные дефекты биосинтеза гормонов. Процессы: а)биосинтез гормонов (Известны два основных типа генетического контроля синтеза гормонов:1. Прямой контроль ген → мРНК → прогормон → гормон.2. Опосредованный контроль по схеме: гены → мРНК → фермент → гормон. В соответствии с химическим строением гормоны разделяют в настоящее время на 4 группы: белки и пептиды; производные аминокислот; стероиды; простагландины) б) секреция гормонов (Освобождение гормона из секреторных гранул, 2. Освобождение из белковосвязанной формы (тиреоидные гормоны).3. Экзоцитоз (эмиоциоз) по схеме: миграция гранул, содержащих гормон, к мембране клетки → растворение мембраны в месте контакта → прорыв содержимого гранулы в межклеточное пространство → диффузия в капилляры.4. Диффузия через плазматические мембраны (стероидные гормоны)) в)транспорт гормонов кровью (Происходит в двух формах: свободной и связанной. В отношении транспорта в связанной форме выделяют: Специфическое связывание со специальными транспортными белками (например, транскортин транспортирует глюкокортикоиды, секс-сте-роидсвязывающий глобулин – половые стероиды).Неспецифическое связывание – связывание с гамма-глобулинами, адсорбция на эритроцитах. Биологическое значение связывания: предотвращение чрезмерного гормонального эффекта; создание биологического резерва гормона; защита гормона от быстрой инактивации; защита гормона от быстрого выведения) г) взаимодействие с клеткой мишенью (Взаимодействие гормона с клеткой-мишенью включает процесс рецепции и трансдукции. Рецепция основана на существовании на поверхности или внутри клетки специальных веществ (в частности, олигопептидов), обладающих высокой избирательной чувствительностью (аффинностью) к сигнальной молекуле-лиганду. Трансдукция. Образование комплекса гормон – рецептор инициирует активацию внутриклеточных процессов, обеспечивающих, в конечном итоге, ответ клетки. В зависимости от локализации рецепторов различают: мембранный и внутриклеточный, включающий: цитозольный и ядерный Мембранный тип рецепции характерен для белковых и полипептидных гормонов. Внутриклеточный. А. Цитозольный тип внутриклеточной рецепции. Б. Ядерный тип внутриклеточной рецепции установлен для тиреоидных гормонов) д) инактивация гормонов (В печени происходит биологическая инактивация стероидных гормонов, образующиеся метаболиты удаляются с мочой. Выведение гормонов и их метаболитов осуществляется почками с мочой, печенью с желчью, желудочно-кишечным трактом с пищеварительными соками, кожей с потом. Продукты распада пептидных гормонов поступают в общий пул аминокислот организма) Генетически обусловленные дефекты биосинтеза гормонов: а) гипофункция железы б)накопление в железе образующихся до места блокады промежуточных продуктов биосинтеза в)нарушение механизма обратной связи и развитие дополнительных патологических процессов 2)Женский гипер- и гипогонадизм: причины и механизмы развития. Варианты задержки полового развития у женщин. Варианты задержки полового развития у женщин: а)евнухоидизм б)инфантилизм Инфантилизм обычно является следствием недостаточности гипофиза, который не продуцирует не только гонадотропины, но и другие тропные гормоны. Если же недостаточность ограничивается только яичниками, недоразвитие касается главным образом половой системы и сопровождается преимущественно евнухоидизмом. Гипергонадизм. Этиологическими факторами гиперфункции яичников являются: а) патологические процессы в мозгу (опухоль задней части подбугорья, водянка мозга, менингиты, энцефалиты, дефекты мозга), которые приводят к раздражению ядер подбугорья, стимулирующих гонадотропную функцию гипофиза и усиливающих неврогенным путем реакцию яичников на действие гонадотропинов. Предполагают, что несекретирующие опухоли эпифиза могут являться причиной преждевременного полового созревания, так как мелатонин эпифиза тормозит секрецию гонадотропинов; б) гормонально-активные опухоли яичников. К их числу относится гранулезоклеточная опухоль (фолликулома) из клеток гранулезы фолликула и текома из клеток, окружающих фолликул. Обычно эта опухоль продуцирует эстрогены, реже - андрогены. Поэтому их называют феминизирующими в первом случае и вирилизирующими во втором; в) опухоль надпочечников, секретирующая эстрогены. В этом случае функция яичников по механизму обратной связи угнетается. Однако изменения в организме соответствуют таковым при гиперфункции. Результат гормональных расстройств зависит от основного механизма и возраста больного. Усиление функции яичников в препубертатном периоде приводит к преждевременному половому созреванию, которое заключается в развитии вторичных половых органов и признаков до 9-летнего возраста. Рано появляются менструации. Усиливается рост, который впоследствии задерживается в результате преждевременного окостенения эпифизарных хрящей. Идет накопление жира по женскому типу. Развиваются молочные железы и половые органы. В репродуктивном периоде выявляются расстройства менструального цикла. Гипогонадизм. Бывает первичный и вторичный. Причины первичного: (обусловленные патологией яичников. Наблюдается недостаточная продукция ими половых гормонов, а также компенсаторно увеличенный уровень ФСГ в крови) а) врожденные нарушения б) инфекции в) хирургическое удаление яичников Вторичный гипогонадизм (гипогонадотропный, внеяичниковый). Обусловлен дефицитом гонадотропных гормонов (ФСГ, ЛГ) транзиторного (преходящего) или постоянного (хронического) характера. Наиболее частые причины: ♦ Длительные состояния стресса. ♦ Хронические истощающие заболевания (например, синдром мальабсорбции, хронические миелолейкоз, остеомиелит, тубер- кулёз). ♦ Эндокринопатии (например, СД, синдром Иценко-Кушинга, гипотиреоидные состояния). ♦ Патология гипоталамуса (например, пороки развития).
♦ Патология гипофиза (например, при энцефалитах, травмах, кровоизлияниях или новообразованиях в области турецкого седла). Первичная и вторичная эндокринная недостаточность яичников характеризуется сходными признаками. К основным из них относят: нарушения менструального цикла, аменорею, бесплодие. 3)Механизмы развития гиперактивности нейрона. Гиперактивность нейрона обусловлена значительным, выходящим из-под контроля нарушением баланса между возбуждением и торможением нейрона в пользу возбуждения. В функциональном отношении она заключается в продуцировании нейроном усиленного потока импульсов, который может иметь различный характер: высокочастотные потенциалы действия; отдельные разряды; разряды, сгруппированные в пачки, и пр. Особый вид гиперактивности представляет собой пароксизмальный деполяризационный сдвиг (ПДС) в мембране, на высоте которого возникает высокочастотный разряд. Такой вид гиперактивности рассматривается как проявление эпилептизации нейрона. Указанный сдвиг баланса между возбуждением и торможением может быть обусловлен либо первичным усиленным возбуждением нейрона, преодолевающим тормозной контроль, либо первичной недостаточностью тормозного контроля. Первый механизм реализуется значительной деполяризацией мембраны и усиленным входом Na+ и Са2+ в нейрон, второй - расстройством механизмов, обеспечивающих гиперполяризацию мембраны: нарушением выхода К+ из нейрона и входа Cl- в нейрон. Существенным эндогенным регулятором активности нейрона является γ-аминомасляная кислота (ГАМК). Она вызывает торможение нейрона при связывании со своим рецептором. В результате усиливается поступление Cl- в нейрон. Различные виды спонтанной активности нейрона в эпилептическом очаге, вызванном столбнячным токсином в двигательной зоне коры головного мозга кошки. Кривые А и В - потенциалы, регистрируемые с поверхности мозга в эпилептическом очаге (ЭкоГ). Кривые Б и Г - запись электрической активности нейронов, выполненные с помощью внутриклеточного отведения. Нейрон может генерировать с разной частотой регулярные потенциалы действия. На кривой Г показано завершение потенциала высокочастотными разрядами. В это время на ЭкоГ (кривая В) в зоне очага появляется спайковый разряд (указан стрелкой) При растормаживании нейрона в связи с ослаблением торможения и деполяризацией мембраны происходит усиление поступления Са2+ в нейрон. Кроме того, Са2+, находясь уже в цитозоле, нарушает поступление С1- в нейрон, ослабляя, таким образом, изнутри ГАМКергическое торможение. С этим связана эпилептизация нейрона, возникающая под влиянием конвульсантов, которые нарушают ГАМКергическое торможение. Многие конвульсанты (например, пенициллин, коразол и др.) оказывают сложное действие на нейрон, одновременно активируя возбуждающие и инактивируя тормозные механизмы. Хроническая стимуляция нейрона (например, при прямом электрическом раздражении, синаптическом воздействии, под влиянием возбуждающих аминокислот и др.) даже слабой интенсивности может с течением времени привести к гиперактивации нейрона. С другой стороны, выключение афферентации нейрона также обусловливает его гиперактивацию. Этот эффект объясняется повышением чувствительности нейрона и нарушением тормозных процессов. Таким образом, патологическая гиперактивация нейронов, их эпилептизация представляет сложный комплекс разнообразных мембранных и внутриклеточных процессов. Для подавления эпилептической активности целесообразно комплексное применение веществ, нормализующих основные патогенетические звенья процесса. Среди корригирующих воздействий первостепенное значение имеют блокада поступления Са2+ и восстановление тормозного контроля. |
