6 итог по патшизе. Вариант 4 Виды расстройств функции эндокринных желез, их характеристика. Типы гормональных эффектов, их харка
 Скачать 6.14 Mb. Скачать 6.14 Mb.
|
|
Механизмы изменений при гиперпаратиреозе Первичный гиперпаратиреоз наблюдается при опухолях паращитовидных желез (болезнь Реклингаузена) и клинически проявляется в виде фиброзной остеодистрофии (остеопороза и остеомаляции - размягчения костей). Кроме того, он встречается при множественных эндокринных неоплазиях I типа (синдром Вернера) и II типа (синдром Сиппла). Вторичный гиперпаратиреоз – вторичная гиперфункция и гиперплазия желез при длительной гипокальциемии и гиперфосфатемии. Они возникают при патологии: почек (хроническая почечная недостаточность, тубулопатия); кишечника (синдром нарушенного всасывания); костей (сенильная остеомаляция, болезнь Педжета); недостаточность витамина D (при наследственных ферментопатиях и др.); при потере кальция во время беременности или лактации. Патогенез основных нарушений Избыток паратгормона → инактивация в остеобластах лактикоизоцитратдегидрогеназы и недостаток восстановленного никотинамидаденинфосфата → накопление молочной и лимонной кислот → развитие ацидоза в костной ткани → снижение активности щелочной фосфатазы + уменьшение образования фосфорной кислоты + декальцинация костей + лизис органического вещества костей и вымывание мукопротеидов → гиперкальциемия (цитрат и лактат кальция в крови) + гипофосфатемия → гиперкальциурия + мукопротеидоурез и образование цилиндров → кальцификация мукопротеидов → камни почек. Гипрекальциемия → образование нерастворимых солей кальция в результате окисления цитрата и лактата кальция в паренхиматозных органах и мышцах → кальциноз почек, желудка, легких и других органов. Кальциноз почек и камни почек → анурия → уремия. Декальцинация и лизис органического вещества костей → фиброзная остеодистрофия. Избыток паратгормона → снижение всасывания фосфатов в канальцах почек → гиперфосфатурия → гипофосфатемия. Неспецифические механизмы повреждения нейронов. Нарушение энергетического обеспечения нейрона Расстройство биосинтеза белка Дисбаланс ионов и жидкости Повреждение мембран нейронов Апоптоз нейронов Аутолиз компонентов нейронов    Виды психогенной боли Боли, провоцируемые эмоциональными факторами и обусловленные мышечным напряжением Боль как бред или галлюцинация у пациентов с психозами, исчезающая при лечении основного заболевания Боль при истерии и ипохондрии, не имеющая соматической основы Боль, связанная с депрессией, не предшествующая ей и не имеющая какой-либо иной причины Билет 9 1.Периферические механизмы нарушения активности гормонов и их характеристика Периферические механизмы нарушения активности гормонов могут быть обусловлены изменениями связанными с циркуляцией гормонов в кровеносном русле и повреждениями на клеточном уровне. Механизмы А) нарушения связывания гормонов белками плазмы. Большая часть гормонов (кортикостероиды, тироксин, инсулин, половые гормоны) образуют в крови комплекс с белками плазмы. Любое усиление или ослабление связи их с гормонами нарушает снабжение эффекторов гормоном. Б) Блокада циркулирующего гормона. Возможны следующие механизмы инактивации: инактивация гормона в связи с образованием аутоантител к тому или иному гормону. Такая возможность хорошо известна при лечении экзогенными гормональными препаратами изменения в активном центре или конформации молекулы гормона в связи с мутацией и замещением в молекуле гормона одной аминокислоты на другую. нарушение превращения прогормона в гормон. В) Блокада гормонального рецептора Очевидно, это довольно распространенный механизм, приводящий к гормональной недостаточности. Это происходит в тех случаях, когда активный гормон не находит своего рецептора на клетке или в ней в связи с потерей рецептора либо в связи с фиксацией на его поверхности антагонистов, конформационными изменениями и другими факторами, препятствующими соединению с гормоном. Обычно концентрация гормона в таких случаях нормальна либо увеличена. Г) Нарушение пермиссивного действия глюкокортикоидов Как указывалось выше, эффекты ряда гормонов «дистантного» действия, и, в частности, катехоламинов реализуются на фоне физиологических концентраций кортизола. Эту роль кортизола называют пермиссивной. Поэтому снижение концентрации кортизола ведет к уменьшению, а иногда и к извращению эффекта катехоламинов. Так, например, адреналин вызывает гликогенолиз в печени и липолиз в жировой ткани в присутствии кортизола. Д) Нарушение метаболизма гормонов При гепатитах и циррозах печени метаболизм гормонов угнетается. Замедление метаболизма кортизола приводит к задержке его в организме. Это включает механизм обратной связи и угнетает функцию коры надпочечников, что приводит к некоторой их атрофии (рис. 20-7). Снижение инактивации эстрадиола в печени у мужчин вызывает включение механизма обратной связи, в результате чего угнетается образование гонадотропных гормонов в гипофизе и как следствие снижается функция тестикул, развивается импотенция. Одновременно при циррозах печени тестостерон легче превращается в эстрогены. 2. Гиперкортизолизм: виды,причины и механизмы Повышенное содержание в крови глюкокортикоидов (гиперкортизолизм) может быть вызвано экзогенными причинами (введение значительных доз кортизола с лечебными целями) и эндогенными нарушениями, приводящими к гиперсекреции собственного гормона. Гиперпродукция кортизола служит проявлением как первичной патологии коры надпочечников – синдром Иценко-Кушинга (АКТГ-независимый), так и гиперплазии коркового вещества, вызванной повышенной секрецией гипофизарного АКТГ – болезнь Иценко-Кушинга при опухоли передней доли гипофиза или при эктопической продукции АКТГ или кортикотропин-рилизинг фактора (абдоминальная карцинома). Основные проявления гиперкортизолизма I.Первичный (периферический, надпочечниковый) гиперкортизолизм. Синтез кортизола стабильно повышен и не имеет суточной ритмики. Метаболические проявления следующие: 1. Снижение синтеза белка и увеличение их распада → уменьшение мышечной массы, остеопороз, атрофия кожи. 2. Усиление глюконеогенеза и другие влияния кортизола на обмен углеводов → гипергликемия (стероидный диабет). 3. Гипергликемия → подъем уровня инсулина → антилиполитическое действие инсулина "перекрывает" липолитический эффект кортизола → отложение жира и перераспределение его: жир откладывается преимущественно на лице (лунообразное лицо), на животе, над ключицами. Этот феномен объясняют изменением реакций рецепторов адипозоцитов в различных участках тела. 4. Артериальная гипертония в результате нарушения центральной регуляции сосудистого тонуса и регуляции водно-солевого обмена. II. Вторичный (центральный, гипофизарный) гиперкортизолизм. В его происхождении придают большое значение гипоталамическим нарушениям, в частности, ослаблению действия дофамина, тормозящего продукцию кортикотропин-рилизинг гормона и АКТГ. При этом избыток АКТГ стимулирует продукцию всех кортикостероидов и андрогенов. Анаболическое действие андрогенов ослабляет проявления нарушений метаболизма, обусловленных повышенным распадом белков, гликонеогенезом, перераспределением липидов. Поэтому проявления гиперкортизолизма бывают менее выражены. У женщин под действием андрогенов проявляются вирилизм, гирсутизм, нарушение менструаций. 3.Причины и механизмы нарушения энергообеспечения нейронов Нарушения энергообеспечения возникают при уменьшении поступления в мозг глюкозы и кислорода, снижении активности ферментов биологического окисления, разобщения процессов окисления и фосфорилирования, при нарушениях транспорта энергии и расстройствах процессов использования энергии. Наиболее частыми причинами уменьшения поступления в нейроны глюкозы и кислорода являются гипоксемия, гипогликемия, анемия, снижение мозгового кровообращения, увеличение диффузионного пути глюкозы и кислорода от сосуда к нейрону (при отеке мозга). Наиболее частыми причинами снижения активности ферментов биологического окисления являются ингибирование и/или денатурация ферментов (например, при отравлении цианидами и солями тяжелых металлов, при эндогенной интоксикации), недостаточность ферментов (например, при генетических дефектах, авитаминозах В1, В2), нарушение компартментализации ( например, при дезорганизации мембран митохондрий под воздействием ионизирующей радиации, высокой температуры, продуктов нарушенного обмена). Разобщение процессов окисления и фосфорилирования наиболее часто происходит при избытке в нейронах Са++ и накоплении жирных кислот. 4.Механихмы развития невропатической боли. Сравнительная характеристика соматической и невропатической боли А)Нарушение механизмов генерации и проведения болевого сигнала в нервных волокнах б)нарушение процессов контроля возбудимости ноциптивных нейронов в структурах головного и спинного мозга Соматическая - вызванная определённым внешним воздействием; - зависит от силы и характера раздражителя (адекватна ему); - мобилизует защитные силы организма; - является сигналом опасности (возможность повреждения). Б) Патологическая = невропатическая - вызванная повреждением нерв. системы; - не адекватна определённому воздействию; - не мобилизует защитные силы организма - является сигналом патологии, характерна для заболеваний нервной системы. Билет 10 1.Системы вторичных клеточных мессенджеров для гормонов дистантного действия Вторичные месс- это внутрикл вещества, концентрация которых строго контролируется гормонами, нейромедиаторами и другими внеклеточными сигналами. Такие вещества образуются из доступных субстратов и имеют короткий биохимический полупериод. Наиболее важными вторичными мессенджерами являются цАМФ, цГТФ , Са2+, инозит-1,4,5-трифосфат диацилглицери и монооксид азота. цАМФ является аллостерическим эффектором протеинкиназ А и ионных каналов. Системы циклических нуклеотидов. Последовательность событий: активный комплекс «гормон + рецептор» → активация аденилатциклазы (или гуанилатциклазы) → образование из АТФ (или ГТФ) циклического АМФ (или цГМФ) → активация соответствующих протеинкиназ → фосфорилирование и активация белков клетки. Прекращение эффекта обеспечивается инактивацией циклических нуклеотидов (фермент фосфодиэстераза) и их вымыванием из клетки. Фосфатидилинозитоловый цикл. Последовательность взаимодейст¬вий: активный комплекс «гормон + рецептор» → активация фосфоинозитдиэстеразы (фосфолипазы С) через комплекс с протеином G → гидролиз фосфатидилинозитола 4,5-дифосфата → образование инозитол-1,4,5-трифосфата и диацилглицерола. Дальнейшая организация активного ответа клетки реализуется следующими двумя механизмами: Инозитол-1,4,5-трифосфат → выход ионов кальция из эндоплазматического ретикулума → образование активного комплекса «кальций + кальмодулин» (рецепторный белок для кальция) → активация «кальций + кальмодулин» - зависимой протеинкиназы → фосфорилирование белков клетки. Диацилглицерол с участием ионов кальция → активация протеинкиназы С → образование эйкозаноидов и модуляция активности ионных каналов. 2.Механизмы нарушений функций организма при гипопаратиреозе Недостаток паратгормона → изменение активности ферментов в осте-областах с образование НАДФ-Н2 → снижение образования молочной и лимонной кислот → алкалоз в костях → повышение активности щелочной фосфатазы и образования свободной фосфорной кислоты → снижение мобилизации солей кальция из костной ткани + гиперфосфатемия → связывание ионов кальция и образование фосфорнокислого кальция с повышенным отложением его в костях → остеосклероз (остеопетроз). Гипокальциемия и относительное повышение содержания натрия → повышение нервно-мышечной возбудимости → судороги, ларингоспазм, пилороспазм. Недостаток паратгормона → снижение активности гепатоцитов и инактивации холинэстеразы + нарушение синтеза мочевины → накопление ацетилхолина + увеличение образования аммиака → повышение возбудимости подкорковых центров (судороги) + нарушение функции органов и систем. 3.Барьерные образования в НС.Состояния организма,сопровождающиеся повышением проницаемости ГЭБ. 1. Аксоны нейронов имеют миелиновую оболочку, пучки нервных во-локон и нервные стволы окружены эндо- и периневральными оболочками .2. Нейроны ЦНС окружены глиальными клетками, которые не только обеспечивают трофику нейрона и удаление продуктов его метаболизма, но и предохраняют нейрон от различных токсичных воздействий и неблагоприятных изменений гомеостаза. 3. Гематоэнцефалический барьер является специализированным барьером, образованным сосудистой стенкой и глиальными элементами (астроцитами), и обеспечивает защиту мозга от различных патогенных агентов эндо-генной и экзогенной природы. Патологическая проницаемость ГЭБ развивается при действии факторов различной природы: физических (травмы, радиация), химических (токсические жирорастворимые вещества, спирты), инфекционно-токсических, аллергических. Кроме того, проницаемость ГЭБ повышается при таких состояниях как шок, гипертонический криз, воспаление сосудов и оболочек мозга, отек и опухоли мозга, переохлаждение, тяжелые стрессовые ситуации. Важную роль повышение проницаемости ГЭБ играет при нарушении иммун-ной автономии головного мозга и развитии вследствие этого иммунной аутоагрессии с поражением нервной системы (например, рассеянный склероз). 4.Приины и звенья патогенеза ноцицептивной боли Причины:воспаление,травма,ишемия,отек тканей,мышечный спазм Звенья: -раздражение ноцицепторов при повреждении ткани -выделение альгогенов и сенситизация ноцицепторов в области повреждения -усиление ноцицептивного афферентного потока с периферии -сенситизация ноцицептивных нейронов на разных уровнях цнс Вариант №13. Механизмы блокады (инактивации) циркулирующего гормона. -инактивация гормона в связи с образованием аутоАТ к нему; Установлено образование антител к инсулину, СТГ, АКТГ у большинства лечившихся людей, что в ряде случаев сопровождается снижение лечебного эффекта препарата. -изменения в активном центре или конформации молекулы гормона в связи с мутацией и замещением в молекуле гормона одной аминокислоты на другую; На примере СТГ: есть группа больных карликовостью с очень высокой концентрацией СТГ в плазме крови, однако действия этот гормон на рост организма не оказывает. Гормон определяется иммунологически, что свидетельствует о сохранности его антигенных свойств. Больные отвечают увеличением роста на введение экзогенного СТГ, что указывает на наличие нормально функционирующих рецепторов к данному гормону. Сопоставление этих двух фактов дает основание сделать заключение о недостаточной активности эндогенного СТГ; -нарушение превращения прогормона в гормон. Установлено, что белковые гормоны секретируются вначале как прогормоны в составе более крупных полипептидных цепей, которые затем расщепляются. В обычных условиях С-пептид соединяет α- и β-цепи инсулина, и вся молекула называется проинсулином, физиологически неактивный. В результате протеолиза отщепляется С-пептид, и проинсулин превращается в активный инсулин. Нарушение отщепления С-пептида, очевидно, не дает инсулину возможности принять такую конформацию, в которой он наиболее активен. Альдостеронизм: виды, причины и механизмы развития. Различают первичный и вторичный альдостеронизм. Причина первичного альдостеронизма (синдром Конна) – опухоль клубочковой зоны коры надпочечников. Механизм: Избыток альдостерона приводит к усилению реабсорбции натрия в канальцах почек. Натрий задерживается в организме. Его концентрация в экстрацеллюлярных депо в большинстве случаев увеличивается. Одновременно в почках в связи с усилением реабсорбции натрия конкурентно тормозится реабсорбция калия, что ведет к значительной потере калия из клеток организма. Эта потеря компенсируется вхождением в клетки ионов натрия и водорода. Можно отметить следующие проявления альдостеронизма: (думаю, можно не писать их, но всё же) повышение АД, повышение реактивности сердца и сосудов к катехоламинам, мышечная слабость, временные параличи и парезы, гипергликемия, судороги, полиурия. Вторичный альдостеронизм развивается на фоне первичных процессов, протекающих вне надпочечников. К этим процессам относятся недостаточность правого сердца, циррозы печени, злокачественная гипертония и др. Основная причина - нарушение функционирования РААС. (Источник-интернет): Считают, что вторичный альдостеронизм обусловливается гиперсекрецией ренина из-за сужения почечных сосудов. Альдостеронизм развивается также при обструкции почечной артерии и снижении кровотока в пораженной почке. Стимуляция ренин-ангиотензинового механизма с гиперсекрецией альдостерона происходит и при гиповолемии, часто развивающейся при отечных состояниях. При сердечной недостаточности скорость секреции альдостерона может и не меняться, но снижение почечного кровотока и метаболизма альдостерона приводит к повышению уровня этого гормона в крови. 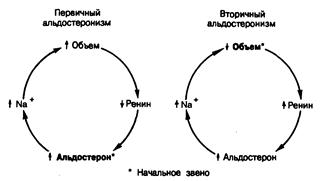 |
