Закон сохранения массы гласит, что в ходе химической реакции остается постоянной масса (число взаимодействующих атомов)
 Скачать 0.54 Mb. Скачать 0.54 Mb.
|
|
SiO3 | | | |||
| | СаС2+Н2О=С2Н2+Са(ОН)2Сколько литров ацетилена (н.у.) выделилось, если гидроксида кальция образовалось 7,4 г? n(Ca(OH)2) = n(C2H2) = 7,4/74 = 0.1 (моль); V(C2H2) = 0.1*22.4 = 2.24(л) | | | ||
| | Какую максимальную степень окисления может проявлять атом рения? +7 | | | ||
| | Сколько фосфорной кислоты (М=98 г/моль) вступило в реакцию H3PO4+Ca(OH)2→ CaHPO4+2H2O, если в результате образовалось 36 г воды? n(H2O) = 2n(H3PO4) = 36/18 = 2 моль, m(H3PO4) = 98*1 = 98(г) | | | ||
| | В каких единицах выражена универсальная газовая постоянная R, если ее значение равно 8,31 Дж/моль*K | | | ||
| | Моль – это единица количества вещества в системе СИ, равная такому его количеству, в котором содержится столько же основных структурных элементов этого вещества, сколько атомов содержится в 0,012 12С | | | ||
| | Требуется для реакции 0,5 моль гидроксида натрия. Этому количеству вещества соответствует его масса, равная 40/2 = 20(г) | | | ||
| | Одновременно в растворе могут находиться: буферные растворы | | | ||
| | Для вычисления количества вещества газа уравнением Авогадро можно воспользоваться, если: известен его объём | | | ||
| | Хлорная кислота – это HClO4 | | | ||
| | Какой объем кислорода (н.у.) пойдет на сжигание 24 г магния 2Mg+O2=2MgO? n(O2) = 2n(Mg) = 24/42 = 0.5(моль), V(O2) = 22.4*1 = 22.4(л) | | | ||
| | Присутствие хлоридов в водном растворе можно определить по образованию белого осадка с: Ag+ (серебро) | | | ||
| | Эквивалент азота в аммиаке равен… 14/3 = 4.6 г/моль | | | ||
| | Вычислить эквивалентную массу металла, если при взаимодействии 24 г его с соляной кислотой образовалось 2 г водорода 24/2 = Э/1; Э = 12 г/моль | | | ||
| | Эквивалентная масса гидроксида натрия равна… 40 г/моль | | | ||
| | 6,02·1023 молекул газа при нормальных условиях занимают объем: 22,4л | | | ||
| | В 98 г серной кислоты содержится водорода: 2г | | | ||
| | Постоянная Авогадро это: число частиц (атомов, молекул, ионов) в 1 моле вещества. Обозначается NA и равна (6,022045 ± 0,000031)*1023 моль -1 | | | ||
| | Определить карбонатную породу можно добавлением соляной кислоты | | | ||
| | Массовую долю железа в Fe2(SO4)3 можно вычислить по формуле: ω(Fe) = M(Fe)/M(Fe2(SO4)3*100% | | | ||
| | Первым доказательством сложного строения атома явилось открытие и изучение самопроизвольного распада атомов некоторых элементов, названное радиоактивностью | | | ||
| | Символ f соответствует значению орбитального квантового числа 3 | | | ||
| | Среди перечисленных элементов наибольшее сродство к электрону имеет какой-либо p-элемент VII группы | | | ||
| | У атома никеля число электронов на внешнем уровне составляет: 2 | | | ||
| | Состояние электрона в атоме описывается при помощи функции зависящей от координат x, y, z, названной волновой или пси-функцией, Ψ(x, y, z) | | | ||
| | На электронном энергетическом подуровне 6d могут разместиться 10 электронов | | | ||
| | В ряду Mg – Al – Ca металлические свойства убывают или возрастают: возрастают | | | ||
| | Координационное число железа в комплексе K[Fe(H2O)2(SO4)2] равно 4 | | | ||
| | Сколько протонов находится в ядре атома вольфрама? 74 | | | ||
| | Какое максимальное количество электронов может находиться на четвертом уровне? 2*n2 = 2*42=32 | | | ||
| | Символы только d-элементов расположены в ряду: | | | ||
| | Согласно квантовой теории, орбиталь – это: составляющая подуровня (s,p,d,f) | | | ||
| | Удаленность электрона от ядра атома определяется главным квантовым числом | | | ||
| | В ряду гидроксидов Ва(OH)2 – Al(OH)3 – Si(OH)4 основные свойства: усиливаются | | | ||
| | Какая электронная конфигурация возможна? | | | ||
| | Согласно теории Бора, энергия электрона в атоме определяется главным квантовым числом | | | ||
| | Набор значений магнитного квантового числа показывает ориентацию в пространстве (возможные значения проекции полного момента атома на ось z) | | | ||
| | Электролитом является вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы | | | ||
| | Белый осадок при добавлении раствора нитрата серебра образует следующий комплекс PtCl4×4NH3 | | | ||
| | В водном растворе комплексные соединения диссоциируют на на комплексный ион и ионы, составляющие внешнюю сферу | | | ||
| | Раствор отличается от химического соединения что состав раствора может изменяться непрерывно | | | ||
| | Нормальная концентрация это отношение количества эквивалентов растворенного вещества к объему раствора | | | ||
| | В одном килограмме 2 % раствора соляной кислоты масса растворенного вещества равна 20г | | | ||
| | Величина осмотического давления рассчитывается по формуле: π = iCRT | | | ||
| | К понятию «сильный электролит» не относится высказывание: то, что относится к слабому электролиту | | | ||
| | Для какого из растворов концентрацией 0,1 моль/кг содержание ОН– будет наибольшим? | | | ||
| | Выбрать способ расчета рН раствора сероводородной кислоты (H2S) pH = -lg2[H+] | | | ||
| | Гидролиз – это химическое взаимодействие с водой: соли, приводящее к образованию слабого электролита | | | ||
| | Буферный раствор образуется при реакции: | | | ||
| | Растворимость соли всегда возрастает при понижении концентрации в растворе одного из его ионов | | | ||
| | Раствор отличается от механической смеси … своей однородностью и возрастанием энтропии системы при смешении компонентов | | | ||
| | Массовая доля это – это отношение массы i-го компонента к массе смеси, выраженное в процентах | | | ||
| | Если в 2 кг раствора содержится 100 г серной кислоты, то массовая доля кислоты в растворе равна 5% | | | ||
| | Если в 2 литрах раствора содержится 0,8 г NaOH, то молярная концентрация раствора равна 0.01 моль/л | | | ||
| | В уравнении осмотического давления СМ – это молярная концентрация раствора | | | ||
| | Фенолфталеин в щелочной среде имеет цвет малиновый (рубиново-красный, пурпурный) | | | ||
| | Реакции Al(OH)3+3HCl→AlCl3+3H2O Отвечает следующее ионное уравнение Al(OH)3 + 3H+ = Al3+ + 3H2O | | | ||
| | Сильную кислоту можно отличить от слабой по: константе диссоциации большей 1×10−3 | | | ||
| | В растворе какой соли рН будет меньше 7? образованной сильной кислотой и слабым основанием | | | ||
| | Произведение растворимости это произведение концентрации ионов малорастворимого электролита в его насыщенном растворе при постоянной температуре и давлении | | | ||
| | В растворе содержится 1,6 кг воды и 400 г NaOH. Процентная концентрация раствора равна 20% | | | ||
| | Растворитель – это компонент раствора агрегатное состояние которого не изменилось при образовании раствора | | | ||
| | Молярная доля это концентрация, выраженная отношением числа молей вещества к общему числу молей всех веществ, имеющихся в растворе | | | ||
| | Выбрать способ расчета рН раствора серной кислоты pH = -lg2[H+] | | | ||
| | Сильным основанием является NaOH, KOH, LiOH, CsOH, FrOH, Ca(OH)2… | | | ||
| | рН раствора (NH4)2SO4 рассчитывается следующим образом: pH = -lg[H+] | | | ||
| | Растворимость BaSO4 можно понизить за счет: добавления одноименных ионов | | | ||
| | Произведение растворимости гидроксида алюминия выражается формулой K = [Al3+][OH-]3 | | | ||
| | Гидролиз нитрата аммония описывается уравнением NH4NO3 + H2O HNO3 + NH4OH | | | ||
| | В окислительно-восстановительных реакциях K2Cr2O7 является: окислителем | | | ||
| | при восстановлении перманганата калия в сернокислой среде образуется соединение: MnSO4 (сульфат марганца (II)) | | | ||
| | Окислителем не является | | | ||
| | В щелочной среде перманганат восстанавливается до степени окисления +6 | | | ||
| | Окислительно-восстановительная реакция пойдет под номером…. | | | ||
| | При протекании реакции KMnO4+Na2SO3+H2SO4= Перманганат калия является окислителем | | | ||
| | Правильные продукты реакции KMnO4+Na2SO3+KOH=указаны в номере….Na2SO3 + 2KOH + 2KMnO4 = Na2SO4 + 2K2MnO4 + H2O (манганаткалия) | | | ||
| | равновесное состояние – это когда: постоянно значение T во всех точках системы, существует определенное значение термодинамических параметров | | | ||
| | Для реакций, протекающих в объеме, скорость процесса определяется уравнением: 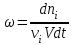 | | | ||
| | Во сколько раз возрастет скорость химической реакции при увеличении температуры системы на 200,если температурный коэффициент равен 2? V2 = V1*220 = 1048576V1; в 1048576 раз | | | ||
| | Во сколько раз возрастет скорость химической реакции при увеличении температуры системы на 100,если температурный коэффициент равен 2? 210 = 1024; в 1024 раза | | | ||
| | Для реакции: Ba(NO3)2 + H2SO4 BaSO4 + 2HNO3 константа равновесия равна Kc = 0 | | | ||
| | Скорость реакции пропорциональна произведению концентраций реагентов в степенях, равных их стехиометрическим коэффициентам | | | ||
| | Согласно правилу Вант-Гоффа, при повышении температуры на 100 скорость химической реакции: возрастёт в 2-4 раза | | | ||
| | Константа равновесия зависит от природы реагирующих веществ и температуры | | | ||
| | Для реакции: СаСО3 СаО + СО2 при понижении давления равновесие сместится в сторону прямой реакции | | | ||
| | Для реакции (считая ее элементарной) H2+I2=2HI скорость прямого процесса определяется уравнением: 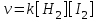 | | | ||
| | К простым веществам относятся состоящие из одного элемента и имеющие заряд 0 | | |||
| | Химический элемент- это совокупность атомов с одинаковым зарядом атомных ядер и одинаковым числом электронов в атомной оболочке | | |||
| | Относятся к основаниям: состоят из металла и групп(ы) OH | | |||
| | Химическая формула – это это обозначение качественного и количественного состава вещества при помощи символов химических элементов | | |||
| | К минералам не относятся: | | |||
| | Реакциями соединения называются химические реакции, в которых из двух или нескольких менее сложных по элементному составу веществ получается более сложное вещество | | |||
| | Количество вещества рассчитывают по формуле – n = m/M | | |||
| | Хлорная кислота это - HClO4 | | |||
| | Сколько моль вещества содержится в 64 г кислорода? n = 64/32 = 2 (моль) | | |||
| | Одним из минералов, входящих в состав вольфрамовых руд, является шеелит. Его формула – CaWO4, а химическое название: вольфрамат кальция | | |||
| | Карбонатами называются соли: образованные катионом металла и анионом угольной кислоты | | |||
| | К благородным газам относятся: элементы восьмой группы, главной подгруппы: He (гелий), Ne (неон), Ar (аргон), Kr (криптон), Xe (ксенон) и Rn (радон) | | |||
| | К щелочным элементам относятся: элементы первой группы, главной подгруппы: Li (литий), Na (натрий), K (калий), Rb (рубидий), Cs (цезий), Fr (франций) | | |||
| | В земной коре наиболее распространены элементы О (кислород), Si (кремний), Al (алюминий), Fe (железо), Ca (кальций), Na (натрий), К (калий), Mg (магний), Ti (титан), Mn (марганец) | | |||
| | Эквивалентная масса кислорода (г/моль) 8 | | |||
| | Эквивалентный объем хлора составляет (л/моль) 17.75 | | |||
| | Эквивалентная масса металла составляет 12. Чему равна эквивалентная масса его оксида? 20 | | |||
| | Эквивалентная масса азота в его оксиде составляет 7. Какой это оксид? N2O | | |||
| | Бор использовал в своей модели атома квантовые числа | | |||
| | Главное квантовое число может принимать значения [1;+∞) | | |||
| | Какую максимальную степень окисления может проявлять атом рения? +7 | | |||
| | Число квантовых чисел, характеризующих состояние электронов в атомах элементов, равно порядковому (атомному номеру Z) элемента (или числу протонов) | | |||
| | Порядок заполнения электронами орбиталей атома определяется принципами Принцип наименьшей энергии - электроны заполняют орбитали в порядке возрастания энергии орбиталей. Принцип Паули - на одной орбитали не может быть больше двух электронов. Правило Хунда - в пределах подуровня электроны сначала заполняют свободные орбитали (по одному), и лишь после этого образуют электронные пары. | | |||
| | "Запрет" Паули заключается в том, что в атоме не может быть даже двух электронов с одинаковыми значениями четырех квантовых чисел | | |||
| | Максимальное число электронов на одной орбитали равно 2n2, n – номер орбитали | | |||
| | Правило Хунда гласит: в пределах подуровня электроны сначала заполняют свободные орбитали (по одному), и лишь после этого образуют электронные пары. | | |||
| | К s-элементам относятся Li (литий), Na (натрий), K (калий), Rb (рубидий), Cs (цезий), Fr (франций), Be (бериллий), Mg (магний), Ca (кальций), Sr (стронций), Ba (барий), Ra (радий) | | |||
| | К p-элементам относятся B (бор), Al (алюминий), Ga (галлий), In (индий), Tl (таллий), C (углерод), Si (кремний), Ge (германий), Sn (олово), Pb (свинец), N (азот), P (фосфор), As (мышьяк), Sb (сурьма), Bi (висмут), O (кислород), S (сера), Se (селен), Te (теллур), Po (полоний), F (фтор), Cl (хлор), Br (бром), I (иод), At (астат), Ne (неон), Ar (аргон), Kr (криптон), Xe (ксенон), Rn (радон) | | |||
| | К d-элементам относятся Cu (медь), Ag (серебро), Au (золото), Zn (цинк), Cd (кадмий), Hg (ртуть), Sc (скандий), Y (иттрий), Ti (титан), Zr (цирконий), Hf (гафний), V (ванадий), Nb (ниобий), Ta (тантал), Cr (хром), Mo (молибден), W (вольфрам), Mn (марганец), Tc (технеций), Re (рений), Fe (железо), Ru (рутений), Os (осмий), Co (кобальт), Rh (родий), Ir (ирридий), Ni (никель), Pd (палладий), Pt (платина) | | |||
| | К f- элементам относятся все остальные | | |||
| | В атоме кислорода число неспаренных электронов равно 2 | | |||
| | В ряду элементов Li, Be, B, C, N, O, F Электроотрицательность возрастает | | |||
| | Химическая кинетика – это наука которая изучает скорость химической реакции | | |||
| | Кинетическое уравнение химической реакции записывается в следующем виде: v = k[A]a[B]b[C]c | | |||
| | |||||
