Методы аналитической биохимии. 1. Правила проведения работ в лаборатории при проведении биохимического анализа с использованием лабораторных животных
 Скачать 1.66 Mb. Скачать 1.66 Mb.
|
38. Электронный парамагнитный резонанс Cуть методаСуть явления: резонансное поглощение электромагнитного излучения неспаренными электронами. Электрон имеет спин Е с 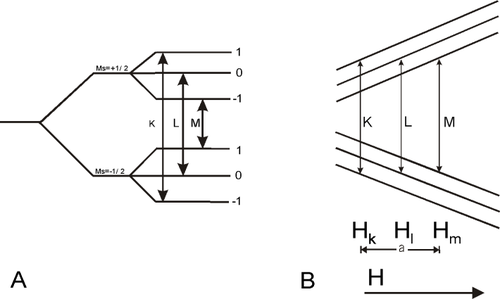 ли поместить свободный радикал (отсоединенный электрон) в магнитное поле, то его энергетическое поле расщепится. Это называется Земановским взаимодействием магнитного поля с магнитным моментом (J). Расщепление энергетических уровней электрона показано на рисунке. ли поместить свободный радикал (отсоединенный электрон) в магнитное поле, то его энергетическое поле расщепится. Это называется Земановским взаимодействием магнитного поля с магнитным моментом (J). Расщепление энергетических уровней электрона показано на рисунке.Если теперь к получившемуся парамагнитному центру приложить электромагнитное поле с какой-либо частотой ν, то оно будет вызывать магнитные дипольные переходы. При совпадении энергии электронного перехода с энергией фотонаэлектромагнитной волны будет происходить резонансное поглощение СВЧ излучения. Таким образом, условие резонанса определяются фундаментальным соотношением магнитного резонанса hν = gβB0. Поглощение энергии СВЧ поля наблюдается в том случае, если между уровнями существует разность заселённостей. Значение методаМетод ЭПР даёт уникальную информацию о парамагнитных центрах. Он однозначно различает примесные ионы, изоморфно входящие в решётку от микровключений. При этом получается полная информация о данном ионе (молекуле) в кристалле: валентность, координация, локальная симметрия, гибридизация электронов, сколько и в какие структурные положения электронов входит, ориентирование осей кристаллического поля в месте расположения этого иона, полная характеристика кристаллического поля и детальные сведения о химической связи. И, что очень важно, метод позволяет определить концентрацию парамагнитных центров в областях кристалла с разной структурой. Но спектр ЭПР это не только характеристика иона в кристалле, но и самого кристалла, особенностей распределения электронной плотности, кристаллического поля, ионности-ковалентности в кристалле и наконец просто диагностическая характеристика минерала, так как каждый ион в каждом минерале имеет свои уникальные параметры. В этом случае парамагнитный центр является своеобразным зондом, дающим спектроскопические и структурные характеристики своего микроокружения. Это свойство используется в т. н. методе спиновых меток и зондов, основанном на введении стабильного парамагнитного центра в исследуемую систему. В качестве такого парамагнитного центра, как правило, используют нитроксильный радикал, характеризующийся анизотропными g и A тензорами (выражение вектора силового напряжения). 39. ЯМР спектроскопия Спектроскопия ЯМР относится к неразрушающим методам анализа. Совр. импульсная ЯМР фурье-спектроскопия позволяет вести анализ по 80 магн. ядрам. ЯМР спектроскопия - один из осн. физ.-хим. методов анализа, ее данные используют для однозначной идентификации как промежут. продуктов хим. р-ций, так и целевых в-в. Помимо структурных отнесений и количеств. анализа, спектроскопия ЯМР приносит информацию о конформационных равновесиях, диффузии атомов и молекул в твердых телах, внутр. движениях, водородных связях и ассоциации в жидкостях, кето-енольной таутомерии, металлo- и прототропии, упорядоченности и распределении звеньев в полимерных цепях, адсорбции в-в, электронной структуре ионных кристаллов, жидких кристаллов и др. Спектроскопия ЯМР - источник информации о структуре биополимеров, в т. ч. белковых молекул в р-рах, сопоставимой по достоверности с данными рентгеноструктурного анализа. Число и положение линий в спектрах ЯМР однозначно характеризуют все фракции сырой нефти, синтетич. каучуков, пластмасс, сланцев, углей, лекарств, препаратов, продукции хим. и фармацевтич. пром-сти и др. Интенсивность и ширина линии ЯМР воды или масла позволяют с высокой точностью измерять влажность и масличность семян, сохранность зерна. Объект помещают в постоянное магнитное поле и подвергают действию радиочастотных и градиентных магнитных полей. В катушке индуктивности, окружающей исследуемый объект, возникает переменная электродвижущая сила (ЭДС), амплитудно-частотный спектр которой и переходные во времени характеристики несут информацию о пространственной плотности резонирующих атомных ядер, а также о других параметрах, специфических только для ядерного магнитного резонанса. Компьютерная обработка этой информации формирует объёмное изображение, которое характеризует плотность химически эквивалентных ядер, времена релаксации ядерного магнитного резонанса, распределение скоростей потока жидкости, диффузию молекул и биохимические процессы обмена веществ в живых тканях. Сущность ЯМР-интроскопии (или магнитно-резонансной томографии) состоит, по сути дела, в реализации особого рода количественного анализа по амплитуде сигнала ядерного магнитного резонанса. Для точного исследования спектров такие простые приспособления, как узкая щель, ограничивающая световой пучок, и призма, уже недостаточны. Необходимы спектральными аппаратами. Чаще всего основной частью спектрального аппарата является призма или дифракционная решетка. 40. Масс спектроскопия: принцип, оборудование, анализ чего и как. Область применения масс-спектрометрии. Область применения масс-спектрометрии - химический и структурный анализ веществ и соединений в органической химии, медицине, судебно-медицинской экспертизе, криминалистике, токсикологии, при производстве и контроле качества различных видов пищевой, парфюмерной, фармацевтической, промышленной и сельскохозяйственной продукции, при наркотическом и экологическом контроле, а также в учебных, научно-исследовательских учреждениях и центрах санэпиднадзора. Предназначена для обнаружения и определения веществ и соединений, входящих в состав медицинской, пищевой, сельскохозяйственной и других видов продукции, лекарственных, психотропных и наркотических средств, биологических систем; для определения химической структуры веществ в очень малых количествах (допинги, ксенбиотики, яды и т.д.). Масс-спектрометрия'>Принцип действия масс-спектрометра. Масс-спектрометрия — метод исследования вещества путём определения отношения массы к заряду (качества) и количества заряженных частиц, образующихся при том или ином процессе воздействия на вещество . Масс-спектрометр — это вакуумный прибор, использующий физические законы движения заряженных частиц в магнитных и электрических полях, и необходимый для получения масс-спектра. Масс-спектр — это зависимость интенсивности ионного тока (количества) от отношения массы к заряду (качества). Природа анализируемого вещества, особенности метода ионизации и вторичные процессы в масс-спектрометре могут оставлять свой след в масс-спектре. Так ионы с одинаковыми отношениями массы к заряду могут оказаться в разных частях спектра и даже сделать часть его непрерывным. Ионы бывают однозарядные и многозарядные, причём как органические, так и неорганические. Большинство небольших молекул при ионизации приобретает только один положительный или отрицательный заряд. Атомы способны приобретать более одного положительного заряда и только один отрицательный. Белки, нуклеиновые кислоты и другие полимеры способны приобретать множественные положительные и отрицательные заряды. Атомы химических элементов имеют специфическую массу. Таким образом, точное определение массы анализируемой молекулы, позволяет определить её элементный состав. Масс-спектрометрия также позволяет получить важную информацию об изотопном составе анализируемых молекул. Основные характеристики масс-спектрометров. Важнейшими техническими характеристиками масс-спектрометров являются: чувствительность (чтобы достигнуть как можно большей чувствительности при улучшении отношения сигнала к шуму прибегают к детектированию по отдельным выбранным ионам.) динамический диапазон, разрешение, (Использовать высокое разрешение на приборах с двойной фокусировкой, где можно добиться высокого уровня достоверности не жертвуя чувствительностью) скорость сканирования. Итак, абсолютным рекордсменом по чувствительности является органический хромато-масс-спектрометр высокого разрешения с двойной фокусировкой. По характеристике сочетания чувствительности с достоверностью определения компонентов следом за приборами высокого разрешения идут ионные ловушки. В них используется искривлённый префильтра, предотвращающего попадание нейтральных частиц на детектор и, следовательно, снижению шума. Способы и приемы разделения ионов при масс-спектрометрии. Масс-спектрометр требует создания в нем очень чистого вакуума. Нейтральные молекулы исследуемого газа поступают в область камеры ионизации, где подвергаются столкновению с ионизирующими электронами. При этом часть молекул (около 0,1%) превращается в ионы. |
