аиа. А. Л. Лапидус, И. А. Голубева, Ф. Г. Жагфаров
 Скачать 5.47 Mb. Скачать 5.47 Mb.
|
На эффективность процесса осушки влияют следующие параметры: давление, температура контакта, природа абсорбента и его концентрация.Повышение давления снижает влагосодержание газа и, следовательно, уменьшает количество раствора, которое необходимо подавать на осушку для получения газа с заданной точкой росы. В значительной степени осушка зависит от температуры контакта газ - абсорбент. Повышение температуры контакта увеличивает парциальное давление воды над абсорбентом и тем самым повышает точку росы осушаемого газа. При понижении температуры контакта наблюдается обратный эффект. Обычно абсорбционная осушка проводится при температуре осушаемого газа не выше 45-50ºС. 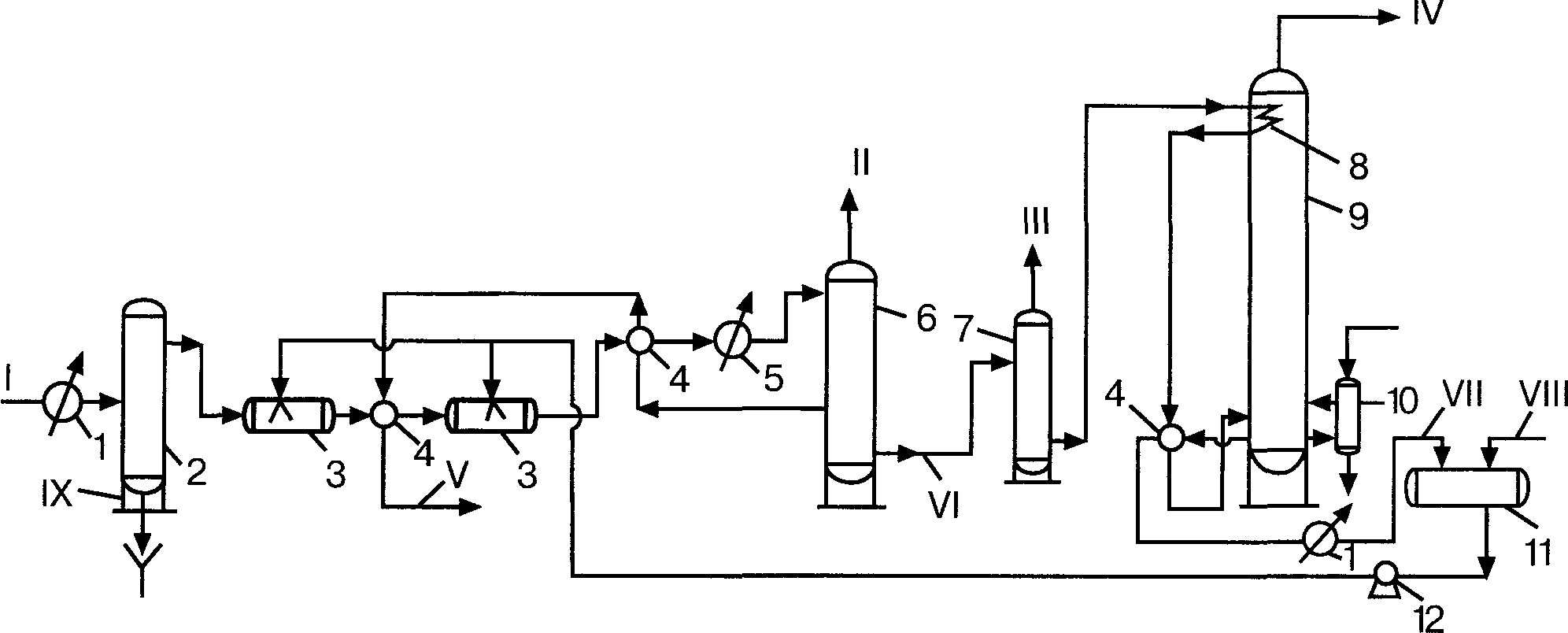 Рис. 16. Принципиальная схема установки осушки газа с впрыском гликоля: 1 — водяной холодильник; 2 — водоотделитель; 3 — узел впрыска гликоля; 4 — теплообменник; 5 — пропановый холодильник; 6 — трехфазный разделитель; 7 — выветриватель; 8 — змеевик; 9 — отпарная колонна; 10 — кипятильник;11 — емкость для гликоля; 12 — насос. Потоки: I — сырой газ; II — осушенный газ; III — газы выветривания; IV – пары воды; V-углеводородный конденсат; VI - насыщенный гликоль; VII – регенерированный гликоль; VIII – свежий гликоль; IX – вода. Экономически важным параметром процесса осушки является кратность абсорбента, т. е. количество гликоля, циркулирующее в системе, на 1 кг извлекаемой влаги. На большинстве установок, использующих ТЭГ, кратность составляет 10 - 35 л/кг влаги. На установках двухступенчатой глубокой осушки с депрессией точки росы до 90°С кратность возрастает до 70 л/кг. Очень важна роль концентрации абсорбента. Чем меньше воды содержится в абсорбенте, тем ниже точка росы осушаемого газа. Обычно для осушки газов, имеющих температуру 0-40ºС, применяют растворы, содержащие 90-98,5 % ДЭГ или 95-99 % ТЭГ. Глубина осушки газа от влаги существенно зависит от концентрации гликоля на входе в абсорбер, т.е. от степени регенерации гликоля. Однако термическая десорбция воды не позволяет достичь концентрации выше 97% из-за того, что при температурах 164°С (ДЭГ) и 206°С (ТЭГ) гликоли начинают разлагаться. При этих условиях максимальная (теоретическая) степень регенерации составляет для диэтиленгликоля — 96,7%, для триэтиленгликоля — 98,1%. При концентрации гликоля 96 -97% точка росы газа после осушки снижается не более чем на 30°С (это депрессия точки росы). Если же концентрация гликоля на входе в абсорбер составляет 99%, то депрессия точки росы возрастает до 40°С. Такая депрессия точки росы оказывается в ряде случаев (низкотемпературная переработка газа) также недостаточной, и поэтому для углубления осушки газа используют вакуумную десорбцию влаги из гликоля (при давлении 0,06 - 0,08 МПа и температуре около 200°С). Концентрация регенерированного гликоля в этом случае повышается до 99,5%, а депрессия точки росы возрастает до 50 - 70°С. Более широкое распространение получили схемы десорбции гликоля с вводом отпарного агента в десорбер. В качестве такого агента используют обычно осушенный газ с верха абсорбера, предварительно нагреваемый до 180 - 200°С и подаваемый через маточник в низ десорбера. Ввод этого агента позволяет снизить парциальное давление паров воды в десорбере, т. е. обеспечить эффект вакуума и за счет этого довести концентрацию гликоля до 99,3 - 99,6%. Максимально возможную депрессию точки росы газа (80 -90°С) можно достичь, используя двухступенчатую осушку. В этом случае установка имеет две системы абсорбции и десорбции. На первой ступени газ грубо осушается гликолем с концентрацией 96 - 97%, а затем поступает в абсорбер второй ступени, где гликолем с концентрацией 99,5-99,6% глубоко доосушается. Соответственно в десорбере первой ступени влага десорбируется при давлении, близком к атмосферному, а на второй ступени -под вакуумом или с вводом в десорбер отпарного агента. Можно использовать также регенерацию гликоля при пониженном давлении, добавление в состав гликоля гигроскопичных солей (хлоридов кальция, цинка и т.д.), использование азеотропной регенерации и отдувку воды нагретым газом (очищенного и осушенного природного газа или любого инертного газа, например азота и т.п.). Применение данных способов позволяет получать гликоль со степенью регенерации 99% и выше. При использовании азеотропной перегонки в качестве азеотропообразователей вводят низкокипящие вещества, образующие с водой азеотропные смеси: бензол, толуол, ксилол и др. Их вводят в количестве не более 10 % от массы абсорбента через перфорированную трубу под уровень горячего раствора гликоля. Температура кипения образующегося азеотропа ниже температуры кипения воды, что позволяет повысить массовую долю регенерированного гликоля до 99,9 % и достигать точки росы осушенного газа минус 75 оС. Экономичность работы установок осушки зависит от потерь гликолей, связанных, в основном, с механическим уносом, разложением и окислением при регенерации, испарением в потоке осушенного и отпарного газов, уносом с конденсатом воды и ее парами, выходящими с верха десорбера и отводимыми в канализацию или атмосферу. На установках НТС гликоль теряется также за счет растворения в углеводородном конденсате. Наибольшей летучестью (большие потери) характеризуются ЭГ, наименьшей ТЭГ, поэтому для осушки газов при обычных температурах применяют ДЭГ и ТЭГ. В процессе осушки газов при низких температурах, когда осушающий раствор впрыскивается в поток охлаждаемого газа для разрушения гидратов, чаще всего используется ЭГ, так как он менее растворим в углеводородном конденсате, выделяющемся из газа. Присутствие ароматических углеводородов в бензине и конденсате повышает растворимость в них гликолей, а, следовательно, и потери их. Разбавление гликолей водой снижает их растворимость в углеводородах. Ориентировочные потери ДЭГ за счет уноса с газом составляют до 80 %, с конденсатом - 12 %, за счет утечек в сальниках и прочих - 8 % от общего количества потерь. Годовые потери ДЭГ на установках НТС достигают 43 г/1000 м3. Для хорошего разделения смеси рекомендуется закладывать в проект фазового разделителя нагрузку 385 л/ч жидкости на 1 м2 поверхности раздела фаз. На вспениваемость гликолей существенное влияние оказывают механические примеси и углеводородный конденсат. Для снижения потерь ДЭГ с сухим газом за счет механического уноса иногда применяются антивспениватели (триалкил-фосфат, октиловый спирт, силиконы). При огневом подогреве в системе регенерации необходимо контролировать условия работы топливных форсунок, чтобы исключить местный перегрев, вызывающий разложение гликолей и повышающий кислотность раствора. Кислотность следует поддерживать на уровне рН 7,3 путем периодической добавки тетрабората натрия, меркаптобензотиазола или МЭА. Рост рН выше 8-8,5 за счет ввода избытка указанных реагентов вызывает вспенивание раствора и увеличение потерь. Адсорбционная осушка Сущность адсорбционной осушки состоит в избирательном поглощении поверхностью пор твердого адсорбента молекул воды с последующим извлечением их из пор внешними воздействиями (повышением температуры адсорбента или снижением давления среды). Осушка газа твердыми осушителями осуществляется в аппаратах периодического действия с неподвижным слоем осушителя. Полный цикл процесса осушки состоит из стадий адсорбции, регенерации и охлаждения адсорбента. В качестве осушителей применяют силикагели, алюмосиликагели, активированный оксид алюминия, бокситы и молекулярные сита (цеолиты). Их адсорбционная емкость существенно зависит от размера пор и соответственно удельной поверхности последних. Особенность молекулярных сит заключается в способности поглощать не только влагу, но и сероводород и углекислоту, т.е. очищать газ от кислых компонентов. Для уменьшения сопротивления движению газа адсорбенты изготавливают в виде шариков или гранул. Требования к осушителю очень жесткие: он должен быстро поглощать влагу из газа и легко регенерироваться, выдерживать многократную регенерацию без существенной потери активности и прочности, иметь высокую механическую прочность и поглотительную способность, оказывать малое сопротивление потоку газа, иметь невысокую стоимость. Иногда применяют комбинацию двух осушителей в одном аппарате, например, силикагеля и активированного оксида алюминия, что позволяет сочетать высокую поглотительную способность силикагеля с высокой степенью осушки газа оксидом алюминия. Для регенерации осушителя используют нагретый газ. Температура десорбции обычно равна 160-180оС (для молекулярных сит — 280 - 290ºС). Установка осушки адсорбцией состоит, как минимум, из двух адсорбционных аппаратов. Принципиальная схема установки приведена на рис. 17. Влажный газ, пройдя через каплеотбойник, поступает сверху в один из адсорберов и проходит его насквозь. Другой адсорбер в это время находится на стадии регенерации или охлаждения. Осушенный газ поступает на дальнейшую переработку или в газопровод. Часть исходного газа, пройдя через трубчатый подогреватель, направляется в низ другого адсорбера для регенерации осушителя. Газ с регенерации проходит теплообменник для охлаждения, сепаратор для отделения воды и смешивается с основным потоком влажного газа. Полный цикл работы одного аппарата включает четыре следующих периода: адсорбция при температуре 35 - 50°С, давлении 8-12 МПа, длительности контакта газа с адсорбентом не менее 10 с (скорость газа в аппарате 0,15 - 0,30 м/с). Длительность адсорбции выбирают исходя из адсорбционной емкости поглотителя, начальной и конечной влажности газа, загрузки адсорбента в аппарате; нагрев адсорбента, который производится после переключения аппарата с режима адсорбции на десорбцию. Нагрев ведется горячим газом из трубчатого нагревателя со скоростью не более 60°С в час. Время, затрачиваемое на нагрев, составляет 0,6 -0,65 от периода адсорбции; десорбция - вытеснение из пор адсорбента поглощенной воды и восстановление его адсорбционной активности. Она начинает происходить, когда температура адсорбента достигнет 200 -250 °С (для силикагелей) или 300 - 350 °С (для цеолитов). Горячий газ в периоды нагрева и десорбции проходит слой адсорбента в направлении, противоположном направлению осушаемого газа в периоде адсорбции (т. е. снизу вверх); охлаждение адсорбента, его начинают после завершения десорбции и переключения аппарата на режим адсорбции (осушки). Охлаждение ведут исходным холодным газом. Период охлаждения занимает 0,35 - 0,40 от времени, затрачиваемого на адсорбцию. При адсорбционной осушке наличие в газе углеводородов от бутанов и выше осложняет процесс, потому что эти углеводороды поглощаются в стадии адсорбции на выходной части слоя адсорбента и при десорбции воды при высокой температуре склонны к образованию коксовых отложений в порах адсорбента. Постепенное закоксовывание адсорбента ведет к снижению его адсорбционной емкости, поэтому требуется периодически регенерировать адсорбент, т. е. выжигать из его пор кокс. При осушке газов, содержащих кислые компоненты, наиболее надежными в работе являются цеолиты. Отличительной особенностью адсорбционного метода осушки по сравнению с абсорбционным является высокая степень осушки газа вне зависимости от его параметров, компактность установки, малые капитальные затраты для установок малой мощности. Недостатками метода являются большие расходы на адсорбент, высокое сопротивление потоку газа и большие затраты при строительстве установок большой мощности. Развитие адсорбционного метода идет в направлении разработки короткоцикловых процессов осушки газов. Продолжительность циклов адсорбции и десорбции составляет 1,5-10 ч, причем адсорбция ведется при повышенном давлении и температуре окружающего воздуха, а десорбция — при атмосферном давлении и той же температуре. Преимущество короткоцикловой адсорбции заключается в повышении производительности и возможности полной автоматизации процесса. Адсорбционная осушка позволяет достичь депрессию точки росы до 100°С (точка росы до минус 90ºС). Поэтому этот метод применяют, когда требуется высокая глубина осушки. Очищенный природный газ, направляемый, например, на гелиевый завод, обязательно подвергают адсорбционной осушке на цеолитах, так как к сырью установок 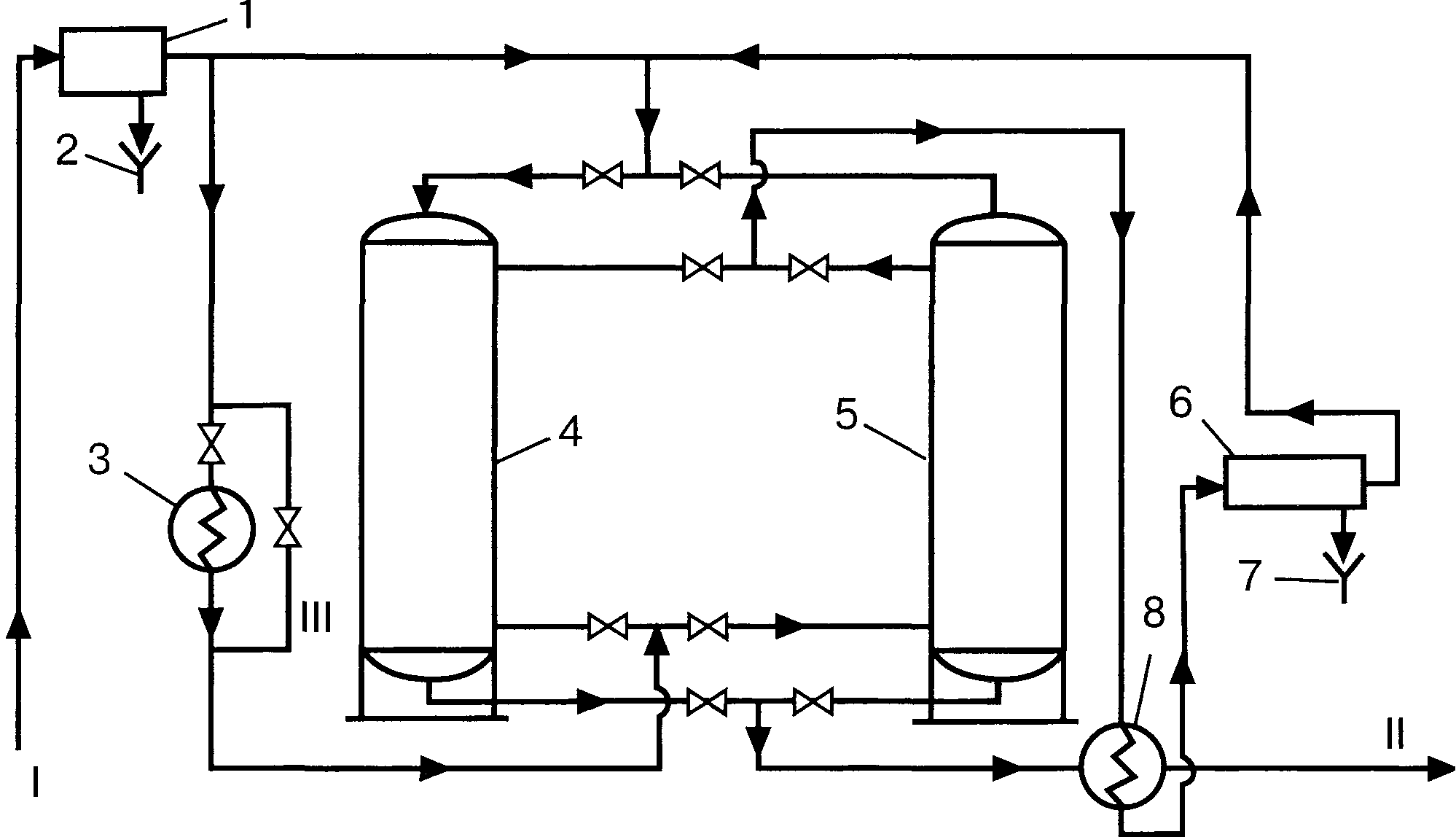 Рис. 17. Tехнологическая схема осушки газа твердыми поглотителями: 1—водоотбойник; 2, 7 — воронка; 3 — трубчатый нагреватель; 4, 5 — адсорберы; 6 — сепаратор; 8 теплообменник Потоки: I — влажный газ; II— осушенный газ; III — обводная линия. низкотемпературной переработки предъявляются жесткие требования по содержанию влаги (точка росы должна быть не выше минус 70 °С). 2.3. Очистка газов от химических примесейК числу нежелательных химических примесей, содержащихся в природных нефтяных газах относятся токсичные и коррозионно-агрессивные серосодержащие соединения, а также негорючие инертные газы, снижающие теплоту сгорания углеводородного газа. Среди серосодержащих примесей чаще всего присутствуют сероводород (H2S), серооксид углерода (СОS), сероуглерод (СS2) меркаптаны (CnH2n-1-SH), а в газовом конденсате – также сульфиды (R-S-R) и дисульфиды (R-S-S-R). В состав инертных газов входят диоксид углерода, азот и гелий. Характеристика химических примесейСероводород (H2S). Из сернистых соединений, входящих в состав природных газов, сероводород является наиболее активным. В нормальных условиях - это бесцветный газ с запахом тухлого яйца, плотностью 1,93 кг/куб м. Сероводород – сильный нервно-паралитический яд: острое отравление человека наступает при концентрации 0,2-0,3 мг/л, а концентрация 1 мг/л – смертельна. При вдыхании сероводорода в этой концентрации отравление развивается почти мгновенно: судороги и потеря сознания оканчиваются смертью от остановки дыхания. Индикатором на повышение концентрации сероводорода являются глаза – жжение, покраснение, опухание век. Его токсичность проявляется также в раздражающем действии на слизистые оболочки верхних дыхательных путей. Предельно-допустимая концентрация его в воздухе рабочих помещений составляет 0,01 мг/л. Сероводород обладает также высокой коррозионной агрессивностью, наличие влаги в газе усиливает коррозионное действие сероводорода и других кислых компонентов. В настоящее время добыча сероводородсодержащего природного газа в странах СНГ составляет около 10% всего объема потребляемого газа. При этом содержание сероводорода в газах колеблется в широких пределах – от нескольких долей до нескольких десятков процентов. Такой газ перед подачей потребителю подвергают очистке ввиду ядовитости сероводорода, его коррозионной агрессивности, отравляющему действию на многие катализаторы, применяемые при химической переработке природных газов. От сероводорода очищают природный газ, газы различных нефтеперерабатывающих и нефтехимических процессов (гидроочистки, крекинга, риформинга, пиролиза и др.). Газы различаются содержанием сероводорода. Природные газы могут быть бессернистыми или содержать значительные количества сероводорода. Например, природные газы Оренбургского месторождения содержат 4—6% сероводорода, Астраханского—25%, а в некоторых природных газах содержание сероводорода достигает 50 - 70% (об.), например в месторождениях Харметтен, Пантер-Ривер и Барберри в Канаде, Миссисипи в США, Жаолангиуанг в КНР и др. Газы нефтепереработки и нефтехимии могут содержать от 0,5 до 15% сероводорода. Требования к степени очистки от сероводорода зависят от назначения газа. При очистке газов, выбрасываемых в атмосферу, содержание сероводорода должно соответствовать ПДК. При очистке технологического газа содержание сероводорода регламентируется требованиями процессов дальнейшей переработки. В частности, для химических синтезов содержание сероводорода в технологическом газе иногда может находиться в пределах от 1 до 50 мг/м3. Природный газ очищают даже при малых количествах в нем сероводорода, поскольку его допустимое содержание в газе, закачиваемом в магистральные газопроводы, не должно превышать 20 мг/м3. В большинстве же случаев очистку газов предпринимают не только для доведения содержания в нем вредных примесей до установленных норм, но и для их извлечения с целью промышленной утилизации. Сероводород, выделяемый при очистке, перерабатывают в элементарную серу или серную кислоту. Так, например, более 30% мирового производства серы - из природных газов, богатых сероводородом; более 5 млн.т./год серы производят в настоящее время Оренбургский и Астраханский ГПЗ. Сероуглерод (дисульфид углерода, CS2) – летучая бесцветная жидкость плотностью 129.7 кг/куб м, кипящая при температуре 46,3оС. В воде не растворяется, но придает ей запах, хорошо растворим в этаноле и хлороформе. В воздухе легко воспламеняется. При повышенных температурах реагирует с водородом, образуя сероводород. Сероуглерод ядовит, вызывает острые отравления при концентрациях в воздухе даже 0,001 мг/куб м. Серооксид углерода (COS) - бесцветный легко воспламеняющийся очень ядовитый газ не имеющий запаха, конденсирующийся при температуре 50,2С, ПДК серооксида углерода – не более 1 мг/куб м в производственных помещениях, не более 0,15 мг/куб м – в населенных пунктах. При нагревании разлагается с образованием диоксида углерода, сероуглерода, оксида углерода и серы. Меркаптаны (тиолы, RSH) – аналоги спиртов, в которых кислород замещен атомом серы. В связи с тем, что энергия диссоциации связей S-H меньше, чем связей О-Н, меркаптаны химически более активны, чем спирты. Это сероорганические соединения с резким неприятным запахом, нерастворимые в воде, но хорошо растворимые в органических растворителях. Резкий запах меркаптанов используется при применении их в качестве одорантов природного газа, особенно при испытании на плотность газовых сетей и систем. При контакте с металлами меркаптаны реагируют с ними с образованием меркаптидов металлов, то-есть протекает так называемая меркаптановая коррозия. При нагревании до 300оС меркаптаны разлагаются с образованием сероводорода и сульфидов. Для большинства катализаторов меркаптаны являются ядами. Сульфиды и дисульфиды (R-S-R, R-S-S-R) - хорошо растворимые в углеводородах, но практически нерастворимые в воде вещества. Они нейтральны, но реагируют со щелочью. При нагревании до 400оС сульфиды разлагаются с образованием сероводорода и алкенов, а дисульфиды – дополнительно к этим соединениям - меркаптанов. По сравнению с сульфидами дисульфиды более реакционноспособны. Диоксид углерода – бесцветный негорючий газ, обладающий кислыми свойствами. При температуре минус 78,5ºС при нормальном давлении образует «сухой лед», минуя жидкое состояние. Термически устойчив, диссоциирует при температурах выше 200ºС. В воде растворим ограниченно. Азот и гелий – негорючие инертные газы, ухудшающие теплоту сгорания газов. Гелий, хотя и содержится в газе в небольших количествах, но специально извлекается из газа для целевого использования. Методы очистки газов от кислых компонентов В настоящее время для очистки газа от кислых компонентов используют три группы методов: абсорбционные, адсорбционные и каталитические. Абсорбционные методы включают три различные группы очистки в зависимости от природы взаимодействия кислых компонентов с активной частью абсорбента. Процессы физической абсорбции, в которых извлечение кислых компонентов происходит за счет их растворимости в органическом абсорбенте. Хемосорбционные процессы основаны на химическом взаимодействии сероводорода и диоксида углерода с активной частью абсорбента. Процессы физико-химической абсорбции используют комбинированные абсорбенты – смесь физического абсорбента с химическим. Адсорбционные методы очистки газов основаны на селективном извлечении кислых компонентов твердыми поглотителями – адсорбентами. В том случае, когда извлекаемый компонент удерживается адсорбентом только физическими силами, имеет место физическая адсорбция. Если извлекаемый компонент вступает с адсорбентом в химическое взаимодействие говорят о химической адсорбции. Каталитические методы очистки газов применяют в тех случаях, когда в газе присутствуют соединения, недостаточно полно удаляемые с помощью жидких или твердых поглотителей, например сероуглерод, серооксид углерода, сульфиды, дисульфиды, тиофен, а также в тех случаях, когда требуется тонкая очистка газа. В промышленности нашли применение два вида каталитических процессов – окислительные и восстановительные. Окислительные методы заключаются в проведении реакций каталитического окисления сероводорода до элементарной серы или каталитического окисления меркаптанов до дисульфидов. Восстановительные методы заключаются в восстановлении сернистых соединений при взаимодействии их с водородом (гидрирование) или с водяным паром (гидролиз), а также в гидрировании диоксида углерода до метана. При восстановлении сернистых соединений все они превращаются в сероводород. После проведения любых каталитических процессов очистки от сернистых соединений требуется последующее отделение продуктов каталитических превращений, например, после каталитического гидрирования газ направляют на очистку от сероводорода. Кроме перечисленных промышленных методов очистки газов от кислых примесей, разрабатываются новые методы: микробиологические, мембранные, фотохимического разложения. Выбор процесса очистки природного газа от кислых компонентов зависит от многих факторов: состава и параметров сырьевого газа, требуемой степени очистки, области использования товарного газа и др. |
