Билет 1 Предмет, задачи и методы патофизиологии. Ее место и значение в системе медицинских наук. Связь патофизиологии с другими науками
 Скачать 0.59 Mb. Скачать 0.59 Mb.
|
|
Задача Пациент Т, 38 лет. Жалобы на сильную головную боль, головокружение, приступы сердцебиения и боли в области сердца, потливость, крупную дрожь во всём теле и чувство страха смерти при тяжелой физической нагрузке. В покое: АД -140/90 мм рт. ст., ЧСС - 76 уд/мин; общие анализы крови и мочи без изменений. При дозированной физической нагрузке: АД - 230/165 мм рт. ст., ЧСС -188 уд/мин; глюкоза крови -200 мг %; в моче повышен уровень катехоламинов и их метаболитов. На рентгенограмме поясничной области увеличение размеров левого надпочечника; размеры и контуры почек нормальные. Вопросы: 1. Какая патология имеет место у пациента? 2. Какой вид гипертензии (эссенциальная или симптоматическая) возник у больного? 3. Каковы причины и патогенез данного вида гипертензии? 4. Объясните механизм значительного увеличения уровня систолического АД при дозированной физической нагрузке? 5. Объясните механизм значительного увеличения уровня диастолического АД при дозированной физической нагрузке? Задача Артериальная гипертензия Симптоматическая Увеличение размеров левого надпочечника и повышение в крови уровня катехоламинов могут указывать на феохромоцитому – опухоль из мозгового слоя надпочечников, продуцирующую катехоламины – адреналин и норадреналин, которые являются вазоконстрикторами и оказывают положительное хронотропное, инотропное воздействие на сердечную мышцу, вследствие чего повышается уровень артериального давления. Тахикардия, увеличение сердечного выброса. Синдром незавершенной диастолы. Билет № 17 Анафилактический (1 тип) аллергических реакций по Джеллу и Кумбсу. Механизмы развития. Примеры заболеваний. Лейкопении. Виды. Причины. Механизмы развития. Гематологические показатели. Какое нарушение сердечного ритма представлено на электрокардиограмме? 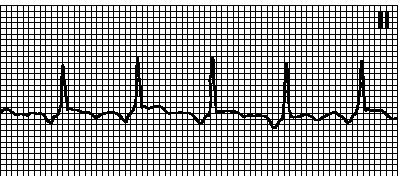 Аллергические реакции, формирующиеся по I типу иммунного повреждения, называют атопическими (реагиновыми, анафилактическими). Их развитие характеризуется следующими особенностями: I. Стадия иммунных реакций. Первичное попадание аллергена в организм через кооперацию дендритных клеток, Т- и В-лимфоцитов запускает сложные механизмы синтеза IgE, фиксирующихся на клетках-мишенях. Повторный контакт организма с этим аллергеном приводит к образованию комплекса АГ+АТ, связанного с поверхностью тучной клетки посредством молекул IgE. При этом условием, достаточным для активации и дегрануляции тучныхклеток, является связывание аллергена по крайней мере с двумя соседними молекулами IgE. II. Стадия биохимических реакций. В этой стадии основную роль играют тучные клетки и базофилы крови. Гранулы тучных клеток и базофилов крови содержат медиаторы: гистамин, гепарин, фактор хемотаксиса эозинофилов (ФХЭ), фактор хемотаксиса нейтрофилов (ФХН). В результате выделения из тучных клеток и базофилов факторов хемотаксиса нейтрофилов и эозинофилов последние скапливаются в очаге аллергического воспаления. III. Стадия клинических проявлений. В результате действия медиаторов повышается проницаемость сосудов микроциркуляторного русла, что сопровождается развитием отека и серозного воспаления. При локализации процесса на слизистых оболочках возникает гиперсекреция. В органах дыхания развивается бронхоспазм, который, наряду с отеком стенки бронхиол и гиперсекрецией мокроты, обусловливает резкое затруднение дыхания. Все эти эффекты клинически проявляются в виде приступов бронхиальной астмы, ринита, конъюнктивита, крапивницы (гиперемия и волдыри), кожного зуда, местного отека, диареи и др. В связи с тем что одним из медиаторов является ФХЭ, очень часто I тип аллергии сопровождается увеличением количества эозинофилов в крови, мокроте, серозном экссудате. Лейкопения - уменьшение общего количества лейкоцитов ниже 4,0-109/л. Наиболее часто развитие лейкопении связано с уменьшением абсолютного числа нейтрофилов (нейтропения). Лимфоцитопения может иметь место при лимфогранулематозе, пневмонии, сепсисе, коллагенозах и некоторых других заболеваниях, но редко является причиной лейкопении. В основе патогенеза лейкопении (нейтропении) лежат три механизма: 1) угнетение лейкопоэтической функции костного мозга; 2) повышенное разрушение нейтрофилов; 3) перераспределение нейтрофилов. Нейтропении, обусловленные угнетением лейкопоэтической функции костного мозга. Развитие их в основном связано: 1) с нарушением пролиферации и дифференцировки стволовых гемопоэтических клеток при «внутреннем» дефекте клеток предшественниц, при дефиците веществ, необходимых для деления и созревания кроветворных клеток (белки, аминокислоты, витамины В12, фолиевая кислота и др.), а также вследствие аутоиммунных механизмов, связанных с образованием антиКОЕ-ГМ антител и аутореактивных Т-лимфоцитов; 2) с разрушением клеток-предшественниц нейтрофилов в костном мозгу при действии токсических веществ и лекарственных препаратов; 3) с патологией гемопоэзиндуцирующего микроокружения, в том числе в случаях выпадения стимулирующей дифференцировку стволовых клеток функции Т-лимфоцитов (при аплазии тимуса), гипосекреции клетками ГИМ факторов роста; 4) с уменьшением площади гранулоцитопоэза в результате замещения кроветворной ткани костного мозга опухолевой (при лейкозах и карцинозах - метастазах рака в костный мозг), фиброзной, костной, жировой тканью. Нейтропении, обусловленные повышением разрушения нейтрофилов. Разрушение нейтрофилов в крови может происходить под влиянием антител типа лейкоагглютининов, которые образуются при переливании крови (особенно лейкоцитарной массы), при действии некоторых лекарственных препаратов, являющихся аллергенами-гаптенами (сульфаниламиды, амидопирин и др.), токсических факторов инфекционного происхождения (тяжелые инфекционные заболевания, обширные воспалительные процессы), при заболеваниях, сопровождающихся увеличением количества циркулирующих иммунных комплексов в крови (аутоиммунные заболевания, лимфомы, опухоли, лейкозы и др.). Нейтропения, связанная с перераспределением нейтрофилов, носит временный характер и, как правило, сменяется лейкоцитозом. Ее формирование отмечается при шоке, неврозах, острой малярии и некоторых других состояниях в результате скопления клеток в расширенных капиллярах органов-депо (легкие, печень, кишечник). Предсердная тахикардия. Задача Пациент Х., 34 лет, выкуривает ежедневно более 2 пачек сигарет в день в течение последних 12 лет. Жалуется на частые бронхиты и трахиты, постоянный кашель с мокротой, одышку во время физической нагрузки. При осмотре: пациент астенического типа сложения; грудная клетка бочкообразная; в дыхательных движениях участвует вспомогательная мускулатура. На рентгенограмме грудной клетки ослабление сосудистого рисунка лёгких, уплощенный купол диафрагмы, утолщение стенок бронхов. Результаты анализа крови: PaO2 - 83мм рт. ст.; Pa СO2 - 49 мм.рт. ст. Результаты спирометрии (% от должных величин): ОЕЛ – 119; ЖЕЛ – 80; резервный объём вдоха – 86; резервный объём выдоха – 88; ФОЕ – 112; ООЛ – 114; Коэффициент Тиффно – 85. Снижение диффузионной способности лёгких. Частота дыхания 20 в 1 мин. Введение бронхолитика (эуфиллина) увеличивает коэффициент Тиффно на 7%. Вопросы: 1. Имеются ли у пациента нарушения вентиляции легких? 2. Каков преимущественный тип данных нарушений? 3. Какова причина этих нарушений? 4. Имеются ли у больного признаки дыхательной недостаточности? 5. Назовите тип дыхательной недостаточности и опишите его механизмы. Задача Да. Рестриктивный тип альвеолярной гиповентиляции. Ограничение расправляемости легкого, увеличение эластического сопротивления. Да. Хроническая дыхательная недостаточность 2-й степени с преобладанием легочных нарушений; по этиологии – бронхолегочная; по типу нарушения – рестриктивная; по патогенезу – гипоксемическая. Билет № 18 Лихорадка. Определение понятия. Лихорадочные кривые. Значение лихорадки для организма. Постгеморрагические анемии. Виды. Причины. Механизмы. Гематологические показатели. Принципы патогенетической терапии. Поставьте диагноз по анализу гормонального статуса. Женщина 55 лет. ТТГ 4,2 (норма 1,9-3,1) мМЕ/л; Т3 0,9 (норма 1,4-1,8) нмоль/л; Т4 74 (норма 97-117) нмоль/л. Лихорадка - типовой патологический процесс, характеризующийся активной задержкой тепла в организме вследствие смещения на более высокий уровень «установочной точки» центра теплорегуляции под действием пирогенных факторов. В зависимости от размера суточных колебаний температуры во вторую стадию лихорадки ее подразделяют на несколько типов:. Постоянная лихорадка febris continua) характеризуется высоким подъемом температуры с суточными колебаниями не выше 1 °С (крупозная пневмония, сыпной тиф и др.). Послабляющая лихорадка f. remittens) - при ней суточные колебания температуры превышают 1 °С, но снижения до нормы не происходит; такой вид лихорадки наблюдается при большинстве вирусных и многих бактериальных инфекциях (экссудативный плеврит, туберкулез и др.). Перемежающаяся лихорадка (f. intermittens) характеризуется большими колебаниями суточной температуры с падением ее по утрам до нормы или ниже (гнойная инфекция, туберкулез, некоторые разновидности малярии, ревматоидный артрит, лимфомы и др.).Изнуряющая лихорадка f. hectica) - суточные колебания температуры достигают 3-4 °С; наблюдается при гнойных процессах, сепсисе, туберкулезе и других заболеваниях. Возвратная лихорадка (f. recurrens) характеризуется чередованием лихорадочных и безлихорадочных периодов, длительность которых колеблется от одних до нескольких суток (возвратный тиф, лимфогранулематоз, малярия и др.). Атипичная лихорадка f. athypica) отличается совершенно незакономерными колебаниями температуры, причем максимальный подъем ее происходит утром (некоторые формы туберкулеза, сепсис и др.). Защитно-приспособительное значение лихорадки подтверждается следующими наблюдениями: при лихорадке усиливается иммунный ответ организма вследствие активации Т- и В-лимфоцитов, усиливается образование антител; повышается образование интерферона; умеренная степень подъема температуры тела может активировать функцию фагоцитирующих клеток и NK-клеток; активируются ферменты, угнетающие репродукцию вирусов; замедляется размножение многих бактерий и снижается устойчивость микроорганизмов к лекарственным препаратам; возрастают барьерная и антитоксическая функции печени; гепатоциты усиленно продуцируют так называемые белки острой фазы; некоторые из этих протеинов связывают бивалентные катионы, необходимые для размножения микроорганизмов. Отрицательное воздействие лихорадки на организм выявляется главным образом при резко выраженном и длительном повышении температуры тела. Оно связано со стимуляцией функции сердца, которая может привести к развитию перегрузочной формы сердечной недостаточности, особенно у людей пожилого и старческого возраста, а также у пациентов, ранее уже имевших то или иное заболевание сердца. Различают острую и хроническую постгеморрагическую анемии. Первая является следствием быстрой потери значительного количества крови, вторая развивается в результате длительных постоянных кровопотерь даже в незначительном объеме. Острая постгеморрагическая анемия - состояние, развивающееся при скоротечной потере значительного объема крови в результате наружного или внутреннего кровотечения вследствие травм, желудочных, кишечных, маточных кровотечений, при разрыве фаллопиевой трубы при внематочной беременности и др. Острая кровопотеря, совместимая с жизнью (до 30% ОЦК), сопровождается последовательным включением защитно-приспособительных механизмов, направленных на восстановление ОЦК. Выделяют следующие фазы компенсаторных реакций: сосудисторефлекторную, гидремическую, костно-мозговую. Сосудисто-рефлекторная фаза длится 8-12 ч от начала кровопотери и характеризуется спазмом периферических сосудов вследствие выброса надпочечниками катехоламинов, что приводит к уменьшению объема сосудистого русла («централизации» кровообращения) и способствует сохранению кровотока в жизненно важных органах. В этот период содержание эритроцитов и гемоглобина в единице объема крови и величина гематокрита остаются близкими к исходным («скрытая» анемия). Гидремическая фаза развивается на 1-2-й день после кровопотери. Проявляется мобилизацией тканевой жидкости и поступлением ее в кровяное русло, что приводит к восстановлению объема плазмы. «Разбавление» крови сопровождается прогрессирующим снижением количества эритроцитов и гемоглобина в единице объема крови. Анемия носит нормохромный, нормоцитарный характер. Костно-мозговая фаза развивается на 4-5-й день после кровопотери. Определяется усилением процессов эритропоэза в костном мозгу в результате продукции клетками ЮГА почек в ответ на гипоксию эритропоэтина, стимулирующего активность КОЕ-Э в костном мозге. В крови повышаются молодые формы эритроцитов (ретикулоциты, полихроматофилы), что сопровождается изменением размеров эритроцитов (макроцитоз) и формы клеток (пойкилоцитоз). 3. Гипофункция щитовидной железы (первичная форма). Задача Из анамнеза известно, что больной Ю., 29 лет, поступил с жалобами на общую слабость, схваткообразные боли внизу живота, понос, сопровождающийся частыми позывами - “стул без счета”. При осмотре. Кожные покровы бледные, язык обложен. Западение стенки живота. Копрологическое исследование: каловые массы жидкие, слизисто-кровянистые с примесью гноя. Бактериологическое исследование: выделен возбудитель дизентерии. Показатели КЩР: рН – 7,26, рСО2 –36 мм рт.ст., ВВ – 24 ммоль/л, SB – 14 ммоль/л, ВЕ - - 8,0 ммоль/л. Больному поставлен диагноз: Дизентерия. Вопросы: 1. Какая типовая форма нарушения КЩР имеется у данного больного? 2. Объясните механизм развития данного нарушения КЩР? 3. Виды нарушения КЩР. Сдвиги основных показателей. Механизмы компенсации. 4. Как развивается компенсация данного нарушения КЩР? 5. Назовите возможные методы коррекции данного нарушения КЩР? Задача 1) Ацидоз метаболический. 2) При диарее из организма выводится большое количество щелочных метаболитов. 3) Ацидоз – снижение рН, алкалоз – повышение рН. И ацидоз и алкалоз может быть газовым и метаболическим, компенсированным (с изменением относительных показателей) и декомпенсированным (с изменением абсолютных показателей). Сдвиг рН на 0,1 влечет за собой тяжелые клинические проявления, на 0,2 – развитие коматозного состояния, на 0,3 – летальный исход. Механизмы компенсации: разбавление, буферные системы, ацидогенез, аммониогенез, реабсорбция бикарбанатов в почках, изменение легочной вентиляции. 4) Гипервентиляция легких, обмен избытка ионов Н+ на ионы калия эритроцитов, кальция костной ткани, реабсорбция бикарбоната в почках. 5) Устранение патологического фактора, нормализация гемодинамики, улучшение легочной вентиляции, коррекция электролитного обмена, улучшение почечного кровотока. Билет № 19 Цитотоксический (2 тип) аллергической реакции по Джеллу и Кумбсу. Механизмы развития. Примеры заболеваний. Мегалобластические анемии. Виды. Причины. Механизмы. Гематологические показатели. Принципы патогенетической терапии. Какое нарушение представлено на электрокардиограмме?  Реакции гиперчувствительности цитотоксического типа протекают следующим образом: Стадия иммунных реакций. В ответ на появление аутоаллергенов начинается выработка аутоантител IgG- и IgМ-классов. Они обладают способностью фиксировать комплемент и вызывать его активацию. Часть антител обладает опсонизирующими свойствами (усиливают фагоцитоз) и обычно не фиксирует комплемент. В ряде случаев после соединения с клеткой происходят конформационные изменения в области Fс-фрагмента антитела, к которому затем могут присоединяться клетки-киллеры (К-клетки). Стадия биохимических реакций. Выделяют 3 типа ее реализации: 1. Комплементзависимый цитолиз. Комплексы АГ+АТ, фиксированные на поверхности измененной клетки, присоединяют и активируют комплемент (по классическому пути). 2. Фагоцитоз. Фиксированные на измененных клетках организма IgG, IgM и СЗв-компоненты комплемента оказывают опсонизирующее действие, т.е. способствуют связыванию фагоцитов с поверхностью клеток-мишеней и их активации. Активированные фагоциты поглощают клетки-мишени и разрушают их при помощи лизосомальных ферментов. 3. Антителозависимая клеточная цитотоксичность. Реализуется путем присоединения клетки-киллера к Fc-фрагменту антител классов IgG и IgM, покрывающих измененные клетки-мишени с последующим их лизисом с помощью перфоринов и гранзимов. В12-дефицитные и фолиеводефицитные анемии. Витамин В12 и фолиевая кислота - кофакторы синтеза ДНК. Их дефицит сопровождается нарушением процессов пролиферации клеток с высоким кругооборотом - клеток крови, клеток кишечного эпителия и как следствие развитием анемии, характеризующейся наличием в костном мозгу мегалобластов, расстройствами пищеварения. Этиология. Дефицит витамина В12 чаще развивается в результате нарушения его всасывания при снижении секреции внутреннего фактора Касла (рис. 14-6) вследствие атрофии слизистой желудка либо после резекции желудка (агастрические анемии). У большинства больных с дефицитом витамина В12 обнаруживаются антитела, направленные против обкладочных клеток желудка и внутреннего фактора Касла. В12- и фолиеводефицитные состояния могут развиваться также при инвазии широким лентецом, поглощающим большое количество витамина В12, при беременности, нарушении всасывания витамина В12 в кишечнике, реже - при недостатке поступления с пищей. Патогенез. Расстройства пищеварения и переход на мегалобластический тип кроветворения обусловливаются резким снижением активности В12-зависимых энзимов, участвующих в метаболизме фолатов (соли фолиевой кислоты), необходимых для синтеза ДНК), что приводит к удлинению S-фазы клеточного цикла и патологии деления и созревания эпителиальных клеток желудочно-кишечного тракта и миелокариоцитов. В костном мозгу развивается мегалобластоз. Срок жизни эритроцитов сокращается до 30-40 дней (в норме - 90 дней). Часть клеток погибает на ранних стадиях развития. Распад мегалобластов в костном мозгу, наряду с их замедленной дифференциацией, и мегалоцитов в крови приводит к тому, что процессы кроветворения не компенсируют процессы кроверазрушения. Развивается мегалобластическая анемия. Картина крови. В периферической крови обнаруживаются гиперхромная анемия (цветовой показатель 1,2-1,5), явления пойкилоцитоза с тенденцией к овалоцитозу, анизоцитоза с выраженным макроцитозом и мегалоцитозом. Характерны явления анизохромии и гиперхромии эритроцитов; могут обнаруживаться полихроматофильные и оксифильные мегалобласты, эритроциты с тельцами Жолли, кольцами Кабо, азурофильной зернистостью. Средний диаметр эритроцитов увеличивается до 8,2-9,5 мкм, их средний объем превышает 100 фл (110-160 фл). Регистрируется умеренная лейкопения с нейтропенией при полном отсутствии малочисленных форм гранулоцитов - эозинофилов и базофилов (анэозинофилия, абазофилия). Встречаются гиперсегментно-ядерные нейтрофилы (дегенеративный ядерный сдвиг вправо), редко - гигантские формы нейтрофилов. Количество тромбоцитов уменьшается, часть их имеет крупные размеры (6-10 мкм и более). 3. Полная поперечная блокада. |
