|
|
Билет 1. Вопрос Ингалипт
Билет 31. Вопрос 1 . Инсулин применяют при сахарном диабете I типа — инсулинзависимым диабетом (ИЗСД)
В 70-е гг. 20 в. шло прогрессирующее улучшение степени очистки инсулинов, что уменьшило проблемы, обусловленные инсулиновой аллергией, нарушениями работы почек, расстройством зрения и иммунной резистентностью к инсулину. Со времени открытия и до начала 80-х гг. использовали инсулин, получаемый из поджелудочной железы КРС и свиней. Инсулин КРС отличается тремя аминокислотами, свиной -одной аминокислотой от инсулина человека. Наиболее эффективный гормон для заместительной терапии при сахарном диабете - гомологичный инсулин, т.е. инсулин человека.
В 1980 г. датская фармацевтическая компания «Novo» разработала метод превращения инсулина свиньи в инсулин человека ферментативным замещением аланина, последний является 30-й аминокислотой в цепи В, на остаток треонина с последующей хроматографической очисткой продукта, в результате был получен однокомпонентный инсулин человека 99% чистоты.
В Великобритании с помощью Е. coli синтезированы обе цепи человеческого инсулина, которые затем были соединены в молекулу биологически активного гормона. Чтобы одноклеточный организм мог синтезировать на своих рибосомах молекулы инсулина,
необходимо снабдить его нужной программой, т.е. ввести ему ген гормона. Химическим способом (операцию проводят специалисты биохимики) получают ген, программирующий биосинтез предшественника инсулина или два гена, программирующие в отдельности биосинтез цепей А и В. инсулина. Следующий этап — включение гена- предшественника инсулина (или гены цепей инсулина порознь) в геном Е. coli — особого штамма кишечной палочки, выращенного в лабораторных условиях; эту задачу выполняет генная инженерия. Из Е. coli вычленяют плазмиду соответствующей рестриктазой. Синтетический ген встраивается в плазмиду (клонированием с функционально активной С-концевой частью Р-галактозидазы Е. coli). В результате Е. coli приобретает способность синтезировать белковую цепь, состоящую из галактозидазы и инсулина. Синтезированные полипептиды отщепляют от фермента химическим путём, затем проводят их очистку. В бактериях синтезируется около 100000 молекул инсулина на бактериальную клетку.
Природа гормонального вещества, продуцируемого Е. coli, обусловлена тем, какой ген встраивается в геном одноклеточного организма. Если клонирован ген предшественника инсулина, бактерия синтезирует предшественник инсулина, который подвергается затем обработке рестриктазами для отщепления препептида с вычленением С-пептида, вследствие чего получается биологически активный инсулин. Для получения очищенного инсулина человека выделенный из биомассы гибридный белок подвергают химико-ферментативной трансформации и соответствующей хроматографической очистке (фронтальной, гель-проникающей, анионообменной).
В Институте биоорганической химии РАН получен рекомбинантный инсулин с использованием генно-инженерных штаммов Е. coli. Из выращенной биомассы выделяется предшественник, гибридный белок, экспрессируемый в количестве 40% от всего клеточного белка, содержащий препроинсулин. Превращение его в инсулин in vitro осуществляется в той же последовательности, что и in vivo - отщепляется лидирующий полипептид, препроинсулин превращается в инсулин через стадии окислительного сульфитолйза с последующим восстановительным замыканием трёх дисульфидных связей и ферментативным вычленением связывающего С
пептида. После ряда хроматографических очисток, включающих ионообменные, гелевые и ВЭЖХ, получают человеческий инсулин высокой чистоты и природной активности.
Использование аффинной хроматографии значительно снизило содержание в препарате загрязняющих белков с более высокой м.м., чем у инсулина. К таким белкам относятся проинсулин и частично расщепленные проинсулины, которые способны индуцировать выработку антиинсулиновых антител. Стандартизация инсулина по загрязнению классифицирует препараты на обычные, содержащие проинсулина более 1 %, монопиковые — менее 0,3% п, улучшенные монопиковые — менее 0,005% и монокомпонентные, содержащие менее 0,001% проинсулина.
Использование человеческого инсулина с самого начала терапии сводит к минимуму возникновение аллергических реакций, Наиболее частые осложнения инсулиновой терапии -гипогликемические состояния, основными признаками избытка инсулина являютсянарушения функции ЦНС (спутанность сознания, странное поведение, кома).
Компания «Eli Lilly» в массовом производстве человеческого инсулина использует технологию рекомбинантных ДНК, помещая кДНК гена человеческого проинсулина в Е. coli или S. serevisae и гидролизуя наработанный проинсулин до молекулы инсулина. Человеческий инсулин быстрее абсорбируется и независимо от формы препарата имеет более короткую длительность действия, чем животные инсулины. Человеческие инсулины менее иммуногениы, чем свиные, особенно смешанные бычьи и свиные инсулины.
Контроль качества генноинженерного инсулина предполагает контроль дополнительных показателей, характеризующих стабильность рекомбинантного штамма и плазмиды, отсутствие постороннего генетического материала в препарате, идентичность экспрессируемого гена и др. (всего 22 показателя).
В настоящее время в медицинской практике используют инсулины трех типов:
короткодействующие с быстрым началом эффекта; средней продолжительности действия; длительного действия с медленным проявлением эффекта. Инсулин короткого действия — регулярный инсулин — представляет собой короткодействующий растворимый при нейтральном значении рН кристаллический цинк-инсулин, эффект которого развивается в течение 15 мин после подкожного введения и продолжается 5—7 ч.
С целью увеличения длительности действия все другие препараты инсулина модифицированы и при растворении в нейтральной среде образуют суспензию. Они содержат протамин в фосфатном буфере - протамин-цинк-инсулин и НПХ (нейтральный протамин Хагедорна) -НПХ-инсулин или различные концентрации цинка в ацетатном буфере -инсулины ультраленте, ленте, семженте. Изменяя порядок смешивания и длительность перемешивания, можно осадить две физические фракции цинк-инсулина: аморфную и кристаллическую.
Препараты инсулина средней длительности действия содержат протамин, представляющий белок средней м.м. 4400. богатый аргинином и получаемый из молок радужной форели. Для образования комплекса требуется соотношение протамина и инсулина 1:10. После подкожного введения протеолитические ферменты разрушают протамин. позволяя инсулину всасываться.
НПХ-инсулин не изменяет фармакокинетический профиль смешиваемого с ним регулярного инсулина. НПХ-инсулин предпочтительнее инсулина ленте в качестве компонента средней длительности действия в терапевтических смесях, содержащих регулярный инсулин.
В фосфатном буфере все инсулины (свиной, бычий, человеческий) легко образуют кристаллы с цинком.
Сырьем для получения инсулина из животного сырья является поджелудочная железа рогатого скота и свиней.
Основные стадии:
]. Очистка сырьяпри значении рН 6,5 перемешивают 2 ч; при значении рН 6.2 и 6.0 перемешивают 2 ч и отстаивают 18—20 ч и при значении рН 5,8 перемешивают 2 ч и отстаивают 48—96 ч при температуре 5 °С. Выпавшие кристаллы инсулина отделяют центрифугированием, промывают на воронке Бюхнера ледяной водой дистиллированной, ацетоном и эфиром. Досушивают инсулин на воздухе, в вытяжном шкафу и эксикаторе.
Активность инсулина определяют биологическим путем: по способности понижать содержание сахара в крови у здоровых кроликов. За единицу действия принимают активность 0,04082 мг кристаллического инсулина (стандарта), она должна быть 24—26 ЕД в 1 мг.
Ионно-обменная хроматография основана на различии в кислотно-основных свойствах белков
Адсорбционная хроматография основа на различии в сродстве белков к неполярному адсорбенту
Гель-хроматография основана на различии в молекулярной массе белков
Аффинная хроматография основана на специфичности связывания белков с лигандами
Электрофорез основан на различии в знаке и величине заряда белков.
Вопрос 2. Carbutamide — карбутамид (Букарбан)
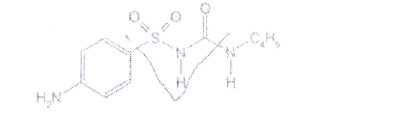
Ы-(п-аминобензолсульфонил)-Н-бутилмочевина
Белый кристаллический порошок, практически нерастворим в воде, растворим в этаноле. Ввиду наличия в молекулах сульфамидной группы, растворы в этаноле и диметилформамиде проявляют кислотные свойства. Растворим в растворах щелочей.
Подлинность производных сульфонилмочевины можно установить методом спектрофотометрии в УФ-области по расположению максимумов поглощения и по удельному показателю поглощения. Раствор карбутамида в этаноле имеет максимум при 269 нм, в 0,1 М растворе хлороводородной кислоты — при 266 и 272 нм, а в 0,1 М растворе гидроксида натрия — при 255 нм.
ПОДЛИННОСТЬ производных сульфонилмочевины устанавливают также с помощью химических реакций.
При нагревании карбутамида в растворе гидроксида калия происходит гидролиз с образованием аммиака, который можно обнаружить по запаху или по изменению окраски лакмусовой бумаги:
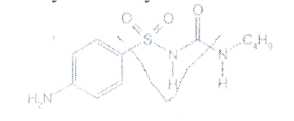
Реакция гидролиза происходит также при кипячении производных сульфонилмочевины с разбавленной серной кислотой. Последующее добавление 30%-пого раствора гидроксида2. Измельчение
3. Экстрагирование
4. Очистка вытяжки от белкрв
5. Очистка от жиров
6. Стандартизация
7. Получение лек.формы
Свежие или замороженные ткани железы измельчают на мясорубке-волчке и экстрагируют способом бисмацерации в эмалированном реакторе с мешалкой. В качестве экстрагента для первой мацерации используют 80—85 % этанол, для второй — 57 % этанол, подкисленный кислотой ортофосфорной (серной, хлороводородной) до значения рН 2,8— 3,0. Экстракцию проводят 1.5—4 ч при перемешивании. Экстракты отделяют фильтрованием или центрифугированием, объединяют и проводят очистку.
Предварительная, грубая очистка экстракта одинакова по всем технологиям, она сводится к удалению анионов кислот. Так, анион кислоты ортофосфорной (РОГ3) удаляют раствором кальция хлорида при значении рН 3,3—-3,8. Затем осуществляют депротеинизацию — последовательное отделение балластных белковых веществ при значении рН 4,5—5,1 и 3,5 при температуре 0 °С. Выпадающие осадки отделяют центрифугированием. Прозрачный экстракт концентрируют выпариванием на вакуум-дистилляционной установке пленочного типа при температуре не выше 30 °С до содержания этанола 10—25% в возможно более короткий срок, при строгом соблюдении температурного режима, так как длительное нагревание приводит к инактивации инсулина. Концентрированный остаток очищают от липидов и балластных белков отстаиванием на холоду (0—4 °С) при значении рН 3,0—3,3. От всплывшего слоя липидов и осадка балластных белков экстракт отделяют фильтрованием. Из сгущенного, очищенного экстракта инсулин-сырец выделяют двукратным высаливанием 25 % раствором натрия хлорида или 40 % раствором аммония сульфата. Этот способ используется на некоторых заводах с 1928 г. по настоящее время.
Наиболее прогрессивным является способ выделения инсулина ионообменной хроматографией. По этому способу операцию упаривания исключают, а осуществляют сорбцию Для удаления жира катионит промывают 65—67 % этанолом, а для отделения балластных белков —- 0,3 М раствором ацетатного буфера (рН 5,3). Десорбцию инсулина проводят 0.01—0,05 М раствором аммонийного буфера (рН 9,8—10,0). Инсулин неустойчив в щелочной среде, поэтому десорбируют его быстро, элюат немедленно подкисляют кислотой хлороводородной до значения рН 4,1—4Г5 и добавляют ацетон. Осадок балластных веществ удаляют. Инсулин осаждают в виде цинк-инсулина раствором цинка ацетата (рН 6,1—6,2), очищают кристаллизацией. Цинк-инсулин растворяют в воде, подкисленной кислотой лимонной до значения рН 2,6—2,8. Раствор отстаивают в течение 1 ч и выпавший осадок балластных белков удаляют фильтрованием через кизельгур. Фильтрат смешивают с ацетоном, добавляют цинк хлористый и фенол, охлаждают до температуры 0 °С, создавая условия для медленной кристаллизации инсулина. Раствор подщелачивают до значения рН 8,0—8,5; оставляют на 2—3 мин, затем создают значение рН 6,7—6,8 н перемешивают 1 ч;натрия приводит к выделению жирных капель аминов, имеющих характерный запах. После более продолжительного нагревания (10-30 мин) в присутствии 50%-ной серной кислоты (с обратным холодильником), последующего охлаждения и нейтрализации выделяется осадок сульфамида.
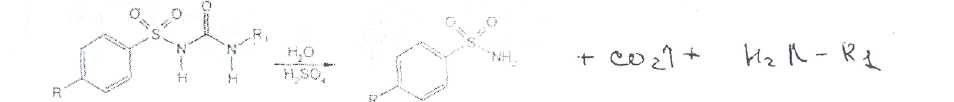
Наличие серы устанавливают после спекания со смесью карбоната и нитрата калия. Затем плав растворяют в хлороводородной кислоте и в фильтрате открывают сульфат-ион.
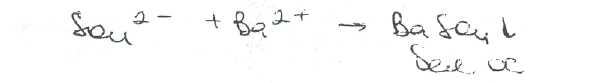
Сульфамидную группу в глибенкламиде обнаруживают по образованию комплексного соединения с ионом меди (II), выпадающего в виде осадка зеленовато-голубого цвета.

Карбутамид дает ряд других реакций, подтверждающих его подлинность. При пиролизе его кристаллов выделяется аммиак, а плав приобретает фиолетово-красный цвет. После обработки плава этанолом раствор окрашивается в красновато-фиолетовый цвет. При нагревании кристаллов карбутамида и резорцина с 1 мл серной кислоты смесь окрашивается в темно-красный цвет, после разбавления водой и добавления щелочи появляется желто-зеленая флуоресценция.
Карбутамид отличается от других производных сульфонилмочевины наличием первичной ароматической аминогруппы в молекуле.
Реакцию диазотирования и азосочетания с в-нафтолом в щелочной среде. Появляется красное окрашивание.

Реакция образования оснований Шиффа.
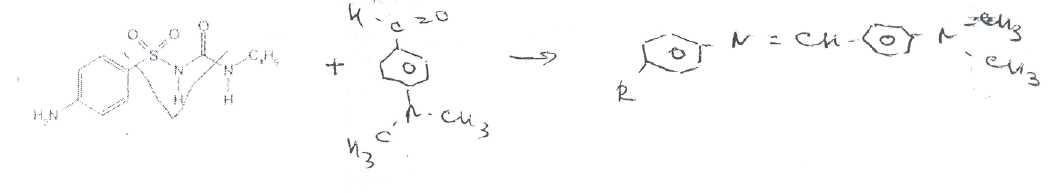
Количественное определение карбутамида выполняют по первичной ароматическойаминогруппе нитритометрическиы методом, устанавливая точку эквивалентности с помощью потенциометра, внешнего или внутренних индикаторов.

Хранят букарбан в сухом, защищенном от света месте, при температуре до 25 °С во избежании процессов гидролиза, окисления препарата. Список Б.
Производные сульфонилмочевины стимулируют образование инсулина в-клетками поджелудочной железы, понижая при этом содержание сахара в крови. Назначают при различных формах сахарного диабета в виде таблеток; карбутамид по 0,5 г, 43.13.
Вопрос 3. Rhizomata et radices Inulae (Rhizomata et radices Inulae
helenii) — корневища и корни девясила (Inulae rhizoma et radix — девясила корневище и корень)
Дикорастущего многолетнего травянистого растения девясила высокого (lnulahelenium ' L.) из сем. сложноцветных —Asteraceae( Compoitae); используют в качестве лекарственного средства и лекарственного сырья.
Девясил высокий — крупное растение высотой 60-350 см. Корневище толстое, короткое, многоглавое, корни до 20 см длиной и 2-3 см толщиной. Листья продолговато-эллиптические, неравнозубчатые, снизу густоопушенные, бархатистые. Цветки желтые, краевые — ложноязычковые и срединные — трубчатые, собраны в крупные корзинки 6-7 см в диаметре. Плод — четырехгранная бурая семянка с хохолком. Цветет в июле — августе, плоды созревают в августе — сентябре.
Химический состав. Корневища и корни девясила содержат 1-3 % эфирного масла, основными компонентами которого являются сапонины и бициклические сесквитерпеновые лактоны с преобладанием алантолактона и изоалантолактона. Богаты инулином (до 40 %)г*
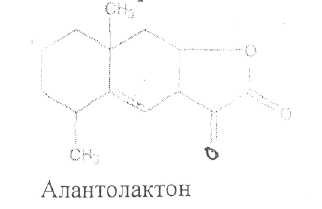
Химические методы определения подлинности. Качественные реакции. При нанесении на поперечный срез корневища 2—3 капель раствора йода не должно наблюдаться синего окрашивания (крахмал).
При нанесении на поперечный срез 2—3 капель 20 % спиртового раствора а-нафтола или тимола и 1 капли концентрированной серной кислоты должно наблюдаться красно-фиолетовое или оранжево-красное окрашивание соответственно (инулин).
Заготовка сырья, первичная обработка и сушка. Сырье от дикорастущих растений заготавливают вручную, выкапывая лопатами. Для возобновления зарослей оставляют один вполне развитый плодоносящий экземпляр на 10 м2. Повторные заготовки на этой же заросли возможны через 8 лет. Для восстановления зарослей несколько кусочков корневища, на верхушках которых имеются почки возобновления, закапывают в почву, не заглубляя их.
Выкопанное сырье отряхивают от почвы, быстро промывают в холодной воде, удаляют остатки стеблей (срезая их при основании), а также тонкие корешки и почерневшие или поврежденные корни. Корневища и толстые корни разрезают на куски длиной 3-20 см и расщепляют продольно с толщиной слоя 1-3 см.
Корневища и корни провяливают в течение 2-3 дней на открытом воздухе, а в сырую погоду — под навесом. Затем сушат в теплых, хорошо проветриваемых помещениях или в сушилках при температуре не выше 40 °С. В сухую погоду допускается сушка на солнце.
Хранение. На складах сырье хранят отдельно от других видов сырья. Срок годности сырья 3 года.
Использование. Корневища и корни девясила в аптеки поступают в измельченном виде и в форме брикета. Отвар из сырья девясила применяют как отхаркивающее средство при заболеваниях верхних дыхательных путей. Они также входят в состав противокашлевых сборов; используются для получения представляющего собой сумму сесквитерпеновых лактонов препарата «Алантон», который обладает противовоспалительным действием; применяют при язвенной болезни желудка и двенадцатиперстной кишки.
Используется в гомеопатии как маточное средство. Пряность.
Вопрос 4. Рецепт выписан верно. Срок действия рецепта - 2 мес. Рецепт отдается больному с указание на обороте количества отпущенного препарата и даты отпуска и не хранится в аптеке. По истечении срока действия рецепт гасится штампом «Рецепт не действителен».
Способ применения ЛС обозначается на русском или русском и национальном языках с указанием дозы, частоты, времени приема и его длительности, а для ЛС,
В защите от действия пониженной температуры нуждаются растворы инсулина. Препараты инсулина разрушаются при замерзании.
Хранят при Т от +2 до +8С
Сроки годности см билет №24Билет 32. Вопрос 1.
Пенициллины
Структурной основой лекарственных веществ полусинтетических пенициллинов является 6-аминопенициллановая кислота, которая включает конденсированные тиазолидиновый (А) и лактамный (В) циклы:
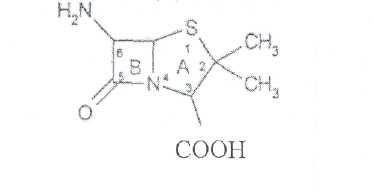
Лактамный цикл впервые обнаружен в природных пенициллинах и отличается большой лабильностью к воздействию различных факторов.
Пенициллин получают путем микробиологического синтеза. Процесс биосинтеза пенициллинов происходит в асептических условиях при непрерывной аэрации воздухом, температуре около 24°С, рН 6,0-6,5 и должен сопровождаться постоянным перемешиванием. Наличие жира в питательной среде оказывает пеногасящее действие и одновременно стимулирует процесс биосинтеза пенициллинов.
Выделение пенициллина из культуральной жидкости осуществляют фильтрованием или центрифугированием. Вначале мицелий и нерастворимые минеральные соли отделяют от культуральной жидкости. Очистку культуральной жидкости и выделение из нее пенициллина последовательно проводят способом замены растворителя
Отделяют пенициллины друг от друга различными способами: адсорбционной хроматографией (на активированном угле или оксиде алюминия); распределительной хроматографией (на. силикагеле) или противоточным распределением. Воду из растворов удаляют при температуре от -20 до -30°С и глубоком вакууме (лиофильная сушка) или пользуясь распылительной сушилкой, что позволяет предотвратить разложение. Кристаллические соли высокой степени чистоты получают перекристаллизацией из органических растворителей.
Ацилирование 6-АПК (6-аминопенициллановой кислоты) хлор ангидридам и кислот можно получить полусинтетические пенициллины (ампициллин)
Биологические свойства полусинтетических пенициллинов зависят от характера заместителя в положении 6. Устойчивость к b-лактамазам обеспечивают заместители, создающие стерические препятствия разрыву b-лактамного цикла. Поэтому синтетические пенициллины с аминогруппой и карбоксилом в боковой цепи (в положении 6), как правило, обладают более широким спектром антибактериального действия, чем природные пенициллины. В результате разработаны и внедрены в производство такие полусинтетические пенициллины, как ампициллин.
[ Лекарственное вещество Химическая структура Описание
1 СП
|
|
|
 Скачать 11.63 Mb.
Скачать 11.63 Mb.