Патфиз ч.1. Патфиз ч. Гл. 1 Введение в предмет Гл. 2 Общая нозология
 Скачать 9.21 Mb. Скачать 9.21 Mb.
|
|
ПРЕДОТВРАЩЕНИЕ ДЕЙСТВИЯ ФАКТОРОВ, ВЫЗЫВАЮЩИХ ИЗМЕНЕНИЯ В ГЕНЕТИЧЕСКОМ АППАРАТЕ КЛЕТОК Для предотвращения действия факторов, вызывающих изменения в генетическом аппарате клеток: • проводят специальные организационные и гигиенические мероприятия (одевают спецодежду, экранизируют источники радиоактивного излучения); • применяют ЛС, повышающие устойчивость клеток организма к действию мутагенных факторов, главным образом ионизирующего излучения. Эти вещества получили название радиопротекторов (радиозащитных или противолучевых препаратов). Радиопротекторы (в зависимости от их происхождения и механизма действия) подразделяют на биологические и фармакологические. † Биологические радиопротекторы повышают радиорезистентность клеток организма за счёт активации неспецифических механизмов и снижения чувствительности клеток к мутагенным факторам. В связи с этим их применяют в основном с профилактической целью. В качестве биологических радиопротекторов используются витамины C, PP, гормоны, коферменты, адаптогены (экстракты и настойки элеутерококка, женьшеня, китайского лимонника и др.). † Фармакохимические радиопротекторы оказывают защитное действие благодаря стимуляции механизмов репарации ДНК, торможения репликации (когда структура ДНК максимально уязвима), а также инактивации продуктов свободнорадикальных и перекисных реакций. К числу широко применяемых фармакохимических радиопротекторов относятся аминотиолы (например, цистамин, пропамин), индолилалкиламины (мексамин, серотонин), биогенные амины (гистамин, тирамин, адреналин), полисахариды. Обнаружению и устранению мутаций способствуют также воздействия, направленные на защиту мембран и ферментов клеток (см. табл. 4–4), в том числе ферментов репаративного синтеза ДНК. КОРРЕКЦИЯ РЕГУЛЯТОРНЫХ ВЛИЯНИЙ НА КЛЕТКИ Для коррекции регуляторных влияний на клетки применяют препараты гормонов, нейромедиаторов, циклических нуклеотидов и др. Методы и схемы их применения различны в зависимости от характера повреждения и развивающегося в связи с этим патологического процесса. ЛЕКАРСТВЕННЫЕ СРЕДСТВА ПРИ ПОВРЕЖДЕНИИ КЛЕТКИ Применение ЛС при различных болезнях и патологических процессах может сопровождаться существенными изменениями фармакокинетики (всасывания, распределения в органах и тканях, метаболизма и экскреции) и фармакодинамики (эффектов и механизмов действия). Эти обстоятельства требуют текущего контроля за характером и выраженностью действия ЛС и при необходимости — коррекции или изменения схем их применения. Наиболее частые причины изменения фармакокинетики и фармакодинамики ЛС при повреждении клеток — нарушения превращений препаратов в процессе метаболических реакций (биотрансформация) или в результате соединения с различными химическими группами и молекулами (конъюгация). Например, снижение активности ферментов микросом клеток, в частности печени, в которой трансформируются и инактивируются многие ЛС, может сопровождаться увеличением продолжительности или выраженности эффекта ЛС. Нарушение превращений ЛС в повреждённых клетках может привести к разным последствиям. • Образование соединений высокой токсической активности (например, фенетидина из фенацетина). • Изменение характера действия ЛС (например, метаболит антидепрессанта ипразина — изониазид обладает противотуберкулёзной активностью). • Накопление (кумуляция) препарата в органах и тканях. Существенным фактором, влияющим на эффекты ЛС, является изменение реактивных свойств клеток, повреждённых в результате болезни или патологического процесса. Так, эффекты дыхательных аналептиков (лобелина, цититона), проявляющиеся на фоне нормального дыхания или при умеренной гипоксии углублением и учащением дыхания, существенно снижаются по мере нарастания степени гипоксии. Более того, применение высоких доз этих средств на этапах, предшествующих клинической смерти, нередко вызывает угнетение дыхательного центра. Повторное применение ЛС в условиях повреждения клеток при различных патологических процессах и заболеваниях может вызвать: • повышение чувствительности к ЛС (сенсибилизация); • ускорение привыкания к препарату (толерантность); • формирование состояний, характеризующихся выраженным или даже непреодолимым желанием повторного приёма данного ЛС (лекарственная зависимость); • развитие тяжёлых состояний как результате приёма ЛС (лекарственная непереносимость). Некоторые ЛС оказывают действие лишь на изменённые или повреждённые клетки (например, сердечные гликозиды наиболее эффективны в условиях сердечной недостаточности; жаропонижающие средства оказывают более выраженное влияние при лихорадке). Это обусловлено тем, что действие указанных и некоторых других средств связано в основном с подавлением звеньев патогенеза, формирующихся при данном заболевании или патологическом процессе. Например, при сердечной недостаточности нарушается транспорт Ca2+ в кардиомиоциты. В этих условиях сердечные гликозиды, тормозя активность Na+,K+АТФазы, препятствуют выходу Ca2+ из клеток, что способствует активации актомиозинового взаимодействия и, как следствие — повышению сократительной функции миоцитов. Ацетилсалициловая кислота (аспирин) тормозит или блокирует развитие лихорадки, снижая или подавляя активность циклооксигеназы (повышенную при лихорадке). В результате аспирин уменьшает образование Пг группы E (ПгЕ), являющихся одним из медиаторов развития лихорадочной реакции.
ТЕРМИНОЛОГИЯ Для обозначения воспаления в какойлибо ткани или органе используют их латинское или греческое название и добавляют терминологический элемент «ИТ» (в сочетании с греколатинским названием ткани или органа — itis). Например, воспаление кожи — дерматит, печени — гепатит, почки — нефрит, оболочек мозга — менингит, миокарда — миокардит, стенки вены — флебит и т.д. Отдельные разновидности воспаления имеют специальные названия: воспаление лёгких — пневмония; локальное гнойное воспаление — абсцесс; разлитое гнойное воспаление — флегмона. ЭТИОЛОГИЯ Воспаление — результат взаимодействия организма с патогенными факторами различного генеза (причинами воспаления) в определенных условиях. ПРИЧИНЫ ВОСПАЛЕНИЯ Виды причин воспаления в зависимости от их природы и происхождения приведены на рис. 5–1. 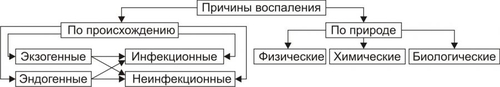 Рис. 5–1. Причины воспаления. ПРИРОДА ФЛОГОГЕННОГО ФАКТОРА Природа флогогенного фактора может быть физической, химической и биологической. Физические факторы. Наиболее частые физические факторы: механическая травма тканей, чрезмерно высокая или низкая температура, воздействие электрического тока или лучистой энергии, внедрение в ткань инородного тела и т.п. Химические факторы: экзо и эндогенные органические или неорганические кислоты и щелочи в высоких концентрациях; избыток в тканях органических соединений: продуктов метаболизма, экскретов, компонентов биологических жидкостей (молочной, пировиноградной и других кислот, а также их солей; жёлчи; мочи; мочевины; солей кальция и др.); ЛС, вводимые в ткани (в частности — гипертонические растворы хлористого кальция, хлорида калия, натрия, карбонатов; камфора; некоторые витамины) и др. Биологические агенты — одна из наиболее распространённых причин воспаления: инфекционные (вирусы, риккетсии, бактерии, а также одно и многоклеточные паразиты, грибы); иммуноаллергические (комплексы АгАТ; антигенно и генетически чужеродные структуры, например, денатурированные белки или погибшие участки ткани; инфицированные вирусом или опухолевые клетки; аутоантитела); токсины насекомых, животных, растений. ГЕНЕЗ ФЛОГОГЕННОГО ФАКТОРА В зависимости от происхождения флогогенные факторы подразделяют на экзогенные и эндогенные. В свою очередь в каждой из этих групп выделяют инфекционные и неинфекционные агенты. Экзогенные воспалительные факторы • Биологические агенты, инфекционнопаразитарные возбудители (бактерии, риккетсии, вирусы, паразиты, микоплазмы, патогенные грибы), токсины и яды растений, насекомых и животных. • Чужеродная плазма, сыворотка (например, при вакцинации) или цельная кровь; взвеси клеток; трансплантированные ткани или органы. Эндогенные факторы Биологические агенты (продукты деструкции повреждённых или погибших тканей, например, в результате их ушиба, ожога, отморожения или нарушения кровотока в них; активировавшаяся условно-патогенная микрофлора; иммуноаллергические комплексы «Аг+АТ+комплемент» и др.). Эндогенные химические агенты (в частности — продукты нормального или нарушенного метаболизма, если они не выводятся из организма с экскретами). Так, при почечной недостаточности в некоторых тканях накапливается мочевая кислота и её соли, мочевина и другие продукты азотистого обмена, что сопровождается развитием воспаления — возникают бронхиты, пневмонии, гастриты, энтероколиты, дерматиты. При нарушении функции печени, расстройстве обмена жёлчных пигментов, последние, а также другие компоненты жёлчи, могут в избытке накапливаться в различных тканях, приводя к развитию в них воспаления. Выраженность воспалительного эффекта флогогенных факторов зависит не только от его природы или происхождения, но и от интенсивности действия: чем она выше, тем, как правило, более остро протекает воспалительная реакция. УСЛОВИЯ, ВЛИЯЮЩИЕ НА ВОЗНИКНОВЕНИЕ И ОСОБЕННОСТИ РАЗВИТИЯ ВОСПАЛЕНИЯ. Возможность возникновения и характер развития воспаления определяется также и рядом условий, при которых реализуется действие причинного фактора. К числу наиболее значимых условий относят реактивность организма и регионарные особенности тканей. РЕАКТИВНОСТЬ ОРГАНИЗМА Реактивность организма может быть нормальной, повышенной и пониженной. Нормальная реактивность. При этом характер воспаления адекватен по выраженности, масштабу и другим особенностям течения фактору, вызвавшему его. В этом случае говорят о нормергическом течении воспаления. Повышенная или качественно изменённая реактивность (например, при сенсибилизации аллергеном). В этих условиях часто наблюдается бурная воспалительная реакция со значительным повреждением тканей. Такой характер воспаления обозначают как гиперергический. Пониженная реактивность (например, у детей первых месяцев и лет жизни; у лиц, перенесших хронические заболевания; у людей преклонного возраста). При этом воспалительная реакция может быть выражена незначительно. В таком случае её называют гипоергической. РЕГИОНАРНЫЕ ОСОБЕННОСТИ Регионарные особенности тканей или органов, подвергшихся воздействию флогогенного агента, важны для возникновения и характера развития воспаления. Так, хроническая локальная травматизация тканей, дистрофические процессы, нарушения кровообращения, пониженная активность механизмов иммунной и неиммунной резистентности облегчают реализацию действия патогенного фактора и нередко усугубляют повреждение тканей в очаге воспаления. МЕХАНИЗМЫ РАЗВИТИЯ ВОСПАЛЕНИЯ Возникнув под влиянием повреждающего фактора, воспаление характеризуется развитием, как правило, более или менее стереотипного и динамичного комплекса изменений в очаге воспаления и в организме в целом. Вместе с тем (учитывая, что воспаление в большинстве случаев является звеном патогенеза разных болезней) характер и динамика воспалительных изменений при разных заболеваниях и у различных пациентов имеют специфику. КОМПОНЕНТЫ ВОСПАЛЕНИЯ Закономерная динамика воспаления, как типового патологического процесса, определяется тем, что в основе его развития находится несколько общих и взаимосвязанных компонентов. Каждый из компонентов воспаления, в свою очередь, — сложный динамический комплекс взаимозависимых реакций, процессов и факторов. Как правило, по ходу воспаления, преимущественно альтеративные изменения в очаге воспаления закономерно сменяются преимущественно экссудативными и далее — преимущественно пролиферативными. Однако, в большинстве случаев, особенно при значительной площади воспаления и/или при его хроническом течении, даже в соседних участках очага воспаления одновременно выявляются признаки различных компонентов воспалительной реакции — и альтерации, и экссудации, и пролиферации. Определённая пространственная и временная мозаика этих компонентов в очаге воспаления обусловливает, с одной стороны, закономерный характер развития и проявлений воспаления, а с другой — своеобразие его течения у каждого конкретного пациента. Выделяют следующие компоненты воспаления: альтерация, сосудистые реакции и изменения крово и лимфообращения, экссудация, эмиграция лейкоцитов и выход других форменных элементов крови в ткань, фагоцитоз, пролиферация (рис. 5–2). 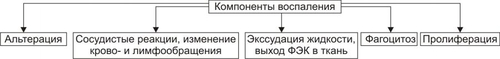 Рис. 5–2. Компоненты воспаления. ФЭК — форменные элементы крови. АЛЬТЕРАЦИЯ Альтерация — первое и непосредственное следствие повреждающего действия флогогенного фактора и инициальное звено механизма развития воспаления. Альтерация, как первичная, так и вторичная, — сложный комплекс изменений (рис. 5–3). 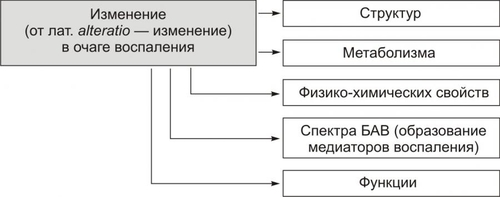 Рис. 5–3. Альтерация как компонент воспаления. ПЕРВИЧНАЯ И ВТОРИЧНАЯ АЛЬТЕРАЦИЯ В очаге воспаления выделяют зоны первичной и вторичной альтерации, их характеристики названы в табл. 5–1 и рассмотрены ниже. Таблица 5–1 Характеристики зон первичной и вторичной альтерации в очаге воспаления
ЗОНА ПЕРВИЧНОЙ АЛЬТЕРАЦИИ Причина формирования: флогогенный фактор, действующий на ткань. Локализация: место прямого контакта причины воспаления с тканью (эта зона — эпицентр очага воспаления). Основные механизмы Повреждение мембранных структур и внутриклеточных ферментов, а также структур межклеточного вещества. Расстройства энергетического обеспечения функций и пластических процессов в повреждённой ткани. Нарушения трансмембранного переноса и градиента ионов, соотношения их между собой, содержания жидкости внутри и за пределами клетки и в зоне альтерации в целом. Проявления Расстройства функции повреждённых, но ещё жизнеспособных участков ткани вне зоны некроза. Некроз. Значительные физикохимические изменения. Различные формы дистрофии. Время начала развития вышеуказанных изменений колеблется в широком диапазоне и определяется особенностями флогогенного фактора, ткани или органа, подвергшегося его воздействию; реактивности организма. Тем не менее, первые изменения выявляются сразу после воздействия причины воспаления на ткань. ЗОНА ВТОРИЧНОЙ АЛЬТЕРАЦИИ Причины • Эффекты флогогенного агента (хотя за пределами эпицентра очага воспаления эффективность его патогенного воздействия значительно ниже). • Влияние факторов, вторично формирующихся в зоне первичной альтерации в связи с образованием медиаторов воспаления, развитием метаболических, физикохимических и дистрофических изменений. Локализация • Частично в месте контакта флогогенного агента с тканью (там, где сила его воздействия была минимальной). • В основном — вокруг области первичной альтерации. Обычно площадь этой зоны значительно больше площади первичной. Механизмы развития • Расстройства местных механизмов нервной регуляции в связи с повреждением тел нейронов, нервных стволов и/или их окончаний, синтеза, накопления и высвобождения из них нейромедиаторов. • Нарушение выброса нейромедиаторов (норадреналина, ацетилхолина и др.) из нервных терминалей симпатической и парасимпатической системы в очаге воспаления и стадийные изменения чувствительности тканей к нейромедиаторам в этом очаге. • Расстройства аксонного транспорта трофических и пластических факторов (углеводов, липидов, белков, адениннуклеотидов, нуклеиновых кислот, БАВ, ионов и других агентов) от тел нейронов к соматическим клеткам. • Стадийные изменения тонуса сосудов микроциркуляторного русла и в связи с этим — расстройства кровообращения • БАВ, поступающие в зону вторичной альтерации из зоны первичной альтерации, а также образуются за пределами очага воспаления. В совокупности эти изменения обусловливают расстройства обмена веществ, значительные физикохимические сдвиги в зоне вторичной альтерации, развитие различных видов дистрофий и даже — некроза. Проявления Изменения структуры клеток и межклеточного вещества тканей, обычно обратимые (например, признаки повреждения клеток, архитектуры ткани и др.) Расстройства метаболизма (выражается различными отклонениями в обмене веществ и развитии). Умеренные отклонения физикохимических параметров (например, рН, осмоляльности жидкости, температуры тканей, трансмембранного распределения ионов). Обратимые изменения функции тканей и органов. | ||||||||||||||||||||||||||||
