Патфиз ч.1. Патфиз ч. Гл. 1 Введение в предмет Гл. 2 Общая нозология
 Скачать 9.21 Mb. Скачать 9.21 Mb.
|
|
Построенные из аминокислотных остатков молекулы пептидов и полипептидов, а также макромолекулы белка и их комплексы выполняют в организме такие важные функции как информационная (например, в качестве гормонов), рецепторная (белки — необходимый компонент рецепторов), каталитическая (ферменты), структурная и другие. Отсюда следует, что нарушения обмена аминокислот и белка приводят к существенным расстройствам функций органов, их систем и организма в целом. При анализе нарушений аминокислотного и белкового обмена необходимо помнить следующие важные положения. Белок в организме не депонируется. При его дефиците мобилизуются белки мышц, кожи, костей, а при более тяжeлых состояниях — паренхиматозных органов (мозга — в последнюю очередь). Обмен белка отличается высокой интенсивностью. Время полужизни многих белковых молекул колеблется от нескольких часов до нескольких суток. За 24 часа обновляется около 1 г/кг белка организма. Цикл полной замены молекул белка в организме взрослого человека составляет 130–160 сут. БАЛАНС АЗОТА Интегральный показатель общего уровня белкового обмена — азотистый баланс: суточная разница между поступающим в организм азотом, и количеством азота, выделяемого из организма (в том числе с мочой и калом в составе мочевины, мочевой кислоты, креатина, солей аммония, аминокислот и т.д.) Виды азотистого баланса • Нулевой (количество поступающего и выводящегося азота совпадает). • Положительный (количество азота, поступающего в организм, выше, чем выводящегося). Наблюдается как в норме (например, при регенерации тканей или беременности), так и в патологии (например, при гиперпродукции соматотропного гормона или полицитемии). • Отрицательный (количество азота, поступающего в организм меньше, чем выводящегося). Выявляется, например, при голодании, стрессреакциях, тяжёлом течении СД, гиперкортицизме. ТИПОВЫЕ НАРУШЕНИЯ БЕЛКОВОГО ОБМЕНА Типовые нарушения белкового обмена представлены на рис. 9–1. 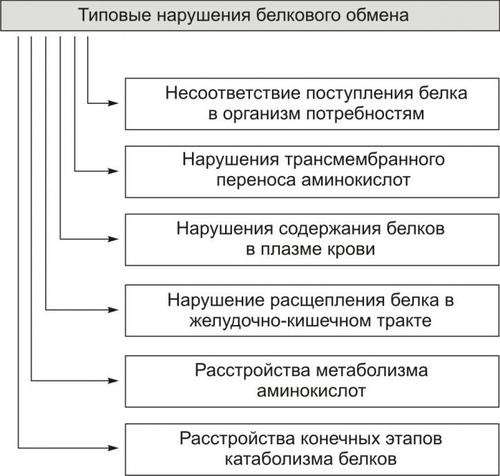 Рис. 9–1. Типовые нарушения белкового обмена. НЕСООТВЕТСТВИЕ КОЛИЧЕСТВА И АМИНОКИСЛОТНОГО СОСТАВА БЕЛКА, ПОСТУПАЮЩЕГО В ОРГАНИЗМ, ПОТРЕБНОСТЯМ В БЕЛКЕ Оптимальное общее количество белка, которое должно поступить в организм, колеблется в диапазоне 1,5–2,5 г на кг массы тела в сутки. Белок, поступающий в организм, должен восполнять как общий его расход, так и потребность в незаменимых аминокислотах, которые не синтезируются в организме и поступают только с пищей. Виды несоответствия количества и состава белка потребностям организма перечислены на рис. 9–2.  Рис. 9–2. Виды несоответствия количества и состава белка потребностям организма. НЕДОСТАТОЧНОЕ ПОСТУПЛЕНИЯ БЕЛКА Основная причина недостаточного поступления белка в организм (алиментарная недостаточность белка, белковокалорическая недостаточность) — голодание. Голодание Виды голодания. Различают несколько видов голодания • Абсолютное (прекращение поступления в организм пищи и воды). • Полное (прекращение поступления в организм пищи, но не воды). • Неполное (недостаточное количество принимаемой пищи, в том числе белка). • Частичное (недостаток в пище отдельных её компонентов — белков, липидов, углеводов, химических элементов, витаминов). Проявления белкового голодания Примерами белкового голодания могут быть квашиоркор и алиментарная дистрофия. • Квашиоркор — заболевание, характеризующееся несбалансированной алиментарной белково-энергетической недостаточностью. Вызывается рационом с избытком калорийных небелковых продуктов (крахмала, сахара), при недостатке белка и незаменимых аминокислот. Для этого заболевания характерны: † Сниженная масса тела (в связи с дефицитом белка и других компонентов пищи). † Выраженная гипопротеинемия (преимущественно за счёт гипоальбуминемии). † Гиполипопротеинемия (в результате дефицита белка и липидов в пище, нарушениях их образования в организме). † Отрицательный азотистый баланс (на 20–30% ниже нормального). † Тотальные отёки, асцит (в результате гипоонкии крови за счет альбуминов). † Иммунодефициты (часто комбинированные: T и Взависимые). † Гиперальдостеронизм (в основном в связи с гиповолемией). † Гипернатриемия, гипокалиемия (в результатет гиперальдостеронизма), гипофосфатемия, гипомагниемия. † Апатия, гиподинамия. † Задержка физического и умственного развития. Прогноз при квашиоркоре неблагоприятный (в связи со значительной атрофией тонкого кишечника и ахилией), а смертность высокая (в основном, от инфекций в связи с выраженным иммунодефицитом). • Алиментарная дистрофия Алиментарная дистрофия, или алиментарный маразм — сбалансированная белково-калорическая недостаточность. Полное или частичное белковое голодание приводит к мобилизации белка костей, мышц, кожи, в значительно меньшей мере — из внутренних органов. Проявления: † Снижение массы тела. † Содержание белка крови либо на нижней границе нормы, либо часто — гипопротеинемия и гиполипопротеинемия. † Отрицательный азотистый баланс (на 15–25% ниже нормы). † Гипогликемия (в связи с дефицитом в пище углеводов). † Кетонемия, кетоацидоз (в результате интенсивного катаболизма липидов). † Гиперкортицизм (в основном за счёт глюкокортикоидов). † Повышенные уровни глюкагона и соматостатина. † Гиперкалиемия (при тяжёлом течении). † Иммунодефицит (в основном T-клеточный). † Задержка физического и умственного развития. Для алиментарного маразма не характерны выраженные гипопротеинемия, отёки, расстройства электролитного обмена. Прогеоз при своевременном и правильном лечении, как правило, благоприятен. ИЗБЫТОЧНОЕ ПОСТУПЛЕНИЕ БЕЛКА Причины • Переедание. • Несбалансированная диета (длительный приём пищи с высоким содержанием белка). • Активация протеосинтеза (например, при СД или гиперпродукции СТГ). Проявления • Положительный азотистый баланс. • Повышенное (нередко — до верхней границы нормы) содержание белка в крови. • Диспептические расстройства (поносы, запоры). • Дисбактериоз с развитием кишечной аутоинфекции и аутоинтоксикации. • Отвращение к пище, особенно богатой белком. НАРУШЕНИЯ АМИНОКИСЛОТНОГО СОСТАВА ПОТРЕБЛЯЕМОГО БЕЛКА Белки пищи содержат 22 аминокислоты, из них 8 — незаменимых. К ним относятся валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан, фенилаланин. Незаменимые аминокислоты не могут быть синтезированы в необходимом объёме в организме человека. Для этого требуется поступление с пищей Дефицит незаменимых аминокислот • Общие проявления. Недостаток отдельных незаменимых аминокислот приводит к появлению сходных (хотя и не идентичных) общих проявлений. † Отрицательный азотистый (баланс вследствие усиления катаболизма эндогенных белков для компенсации недостатка aaoeoeoiie aieiieeneiou). † Замедление роста и нарушения развития у детей. † Снижение регенераторной активности тканей и органов. † Уменьшение массы тела. † Снижение аппетита и усвоения белка пищи. • Специфические проявления характерны для дефицита конкретной незаменимой аминокислоты. Дефицит фенилаланина характеризуется: † Гипотиреозом. † Гипокатехоламинемией (как результат низкой продукции адреналина и норадреналина хромаффинной тканью надпочечников). Дефицит триптофана проявляется: † Пеллагрой. † Анемией. † Помутнением роговицы, катарактой. † Гипопротеинемией. Дефицит метионина сопровождается: † Потенцированием развития атеросклероза. † Ожирением. † Гипокортицизмом. † Гипокатехоламинемией. Избыток отдельных аминокислот • Общие проявления. Избыточное поступление и/или образование аминокислот в организме приводит к нарушению вкуса, снижению аппетита, уменьшению массы тела, расстройствам обмена других аминокислот (например, избыток лейцина подавляет обмен валина), нарушениям функций органов и тканей (например, избыток метионина и тирозина может привести к гиперкатехоламинемии и/или гиперкортицизму). • Специфические проявления характерны для избытка конкретной аминокислоты. Избыток фенилаланина характеризуется: † Задержкой психомоторного развития ребёнка. † Слабоумием. † Частым развитием экземы. Избыток метионина сопровождается: † Анемией (гемолитической). † Сердечной недостаточностью (в результате кардиомиодистрофии). † Печёночной недостаточностью (в связи с дистрофией гепатоцитов). РАССТРОЙСТВА ПИЩЕВАРЕНИЯ В ЖЕЛУДКЕ И КИШЕЧНИКЕ К расстройствам пищеварения, приводящим к нарушению обмена белка, относят нарушения расщепления белка в желудке и переваривания его в тонком кишечнике. НАРУШЕНИЯ РАСЩЕПЛЕНИЯ БЕЛКА В ЖЕЛУДКЕ • Причины † Гипоацидные состояния (например, при атрофии слизистой оболочки). † Снижение содержания и/или активности пепсина. † Резекция части желудка. • Последствия и проявления † Нарушения набухания белка. † Торможение переваривания коллагенового компонента продуктов. † Недостаточное расщепление белков мышечных волокон. † Замедление эвакуации пищи в двенадцатиперстную кишку. НАРУШЕНИЯ ПЕРЕВАРИВАНИЯ БЕЛКА В ТОНКОМ КИШЕЧНИКЕ • Причины: факторы (в том числе наследственные), вызывающие расстройства пищеварения в кишечнике, включая синдромы мальабсорбции (синдромы нарушенного всасывания). • Проявления † Креаторея † Целиакия глютеновая — синдром, характеризующийся нарушением полостного и мембранного переваривания белков, а также торможением всасывания аминокислот. † Недостаточность энтерокиназы (причина — мутация гена) приводит к существенному снижению протеолитической активности кишечного сока. † Расстройства пищеварения в тонком кишечнике. НАРУШЕНИЯ ТРАНСМЕМБРАННОГО ПЕРЕНОСА АМИНОКИСЛОТ Различные нарушения трансмембранного переноса аминокислот встречаются в общей популяции в 0,3–0,6%. Их причины: мембранопатии различного генеза (первичные — моногенные дефекты и вторичные). Мембранопатии приводят к нарушениям транспорта аминокислот на нескольких этапах: • из кишечника в кровь, • из крови в гепатоциты, • из первичной мочи в кровь, • из крови в клетки органов и тканей. Примеры: синдром Фанкони, цистинурия, цистиноз нефропатический, отравления солями тяжёлых металлов (например, меди, кадмия, свинца, ртути), эндотоксинемии (например, интоксикация избытком соединений меди). РАССТРОЙСТВА МЕТАБОЛИЗМА АМИНОКИСЛОТ Нарушения обмена аминокислот, как правило, существенно изменяют метаболизм белков и приводят к расстройствам обмена нуклеиновых кислот, липидов, витаминов, углеводов, электролитов и воды. Различают первичные (наследственные, врождённые) и вторичные (приобретённые, симптоматические) расстройства метаболизма аминокислот. Примеры первичных расстройств: фенилкетонурия, тирозинопатии (альбинизм, тирозинемии, тирозинозы), алкаптонурия, ацидемия изовалериановая, лейциноз, гомоцистинурия и другие). НАРУШЕНИЕ СОДЕРЖАНИЯ БЕЛКОВ В ПЛАЗМЕ КРОВИ Уровень протеинемии является результатом соотношения процессов протеосинтеза и протеолиза в различных тканях и органах, В норме содержание белков в плазме крови составляет 7% её массы (альбумины около 56%, а четыре фракции глобулинов [ Типовые формы нарушения содержания белков в плазме крови — диспротеинемии — перечислены на рис. 9–3).  Рис. 9–3. Типовые нарушения содержания белков в плазме крови. ГИПЕРПРОТЕИНЕМИИ Различают следующие виды увеличения общего содержания белков в плазме крови: • Гиперсинтетический (истинный, протеосинтетический). Гиперпротеинемия является результатом гиперпродукции белка (например, Ig), парапротеинов (например, при B-лимфоцитарных лейкозах, плазмоцитомах, миеломной болезни); • Гемоконцентрационный (ложный). Гиперпротеинемия этого вида развивается в результате гемоконцентрации без усиления протеосинтеза (например, при ожоговой болезни, диарее, повторной рвоте, длительном усиленном потоотделении). ГИПОПРОТЕИНЕМИИ Известны следующие виды уменьшения общей концентрации белков в плазме крови: • Гипосинтетическая (истинная) гипопротеинемия может быть двух видов. † Первичной (наследственной или врождённой; например, гипопротеинемия при болезни Брутона). † Вторичной (приобретённой, симптоматической; например, при печёночной недостаточности, белковом голодании, почечной недостаточности, гипоаминоацидемии различного генеза, ожоговой болезни). • Гемодилюционный (ложный). Гипопротеинемия обусловлена гиперволемией (например, при гиперальдостеронизме или почечной недостаточности). ПАРАПРОТЕИНЕМИИ Парапротеинемии наблюдают при: • миеломной болезни: опухолевые плазмоциты продуцируют аномальные лёгкие или тяжёлые цепи молекулы Ig; • лимфомах (лимфоцитарных или плазмоцитарных): синтезируются аномальные IgM, обладающие повышенной агрегируемостью. РАССТРОЙСТВА ФИНАЛЬНЫХ ПРОЦЕССОВ КАТАБОЛИЗМА БЕЛКА Расстройства конечных стадий катаболизма белка характеризуются нарушением образования и дальнейших изменений мочевины, мочевой кислоты, аммиака, креатинина, индикана, а также их выведения из организма. ОСТАТОЧНЫЙ АЗОТ Интегративный параметр белкового обмена в организме — содержание небелкового (остаточного) азота крови. Его нормальная концентрация колеблется в диапазоне от 14,3 до 28,5 ммоль/л (табл. 9-1). Таблица 9–1. Содержание небелкового (остаточного) азота в крови (в ммоль/л)
Аммиак Из всех компонентов остаточного азота наиболее выраженными патогенными (цитотоксическими) свойствами обладает аммиак. Он беспрепятственно проникает через мембраны клеток, оказывая альтерирующее действие на ферменты, компоненты цитозоля и мембран. Мочевина Мочевина сама по себе не обладает токсическим действием. Она образуется в печени (в орнитиновом цикле, или цикле мочевины) и в существенно меньшей мере — в других органах и тканях. Выводится мочевина из организма почками и потовыми железами. В условиях патологии (например, при почечной недостаточности) большое количество мочевины удаляется из организма через кишечник. Там она подвергается катаболизму кишечной флорой с образованием высокотоксичного аммиака. Именно он и является одним из значимых (но не единственных) звеньев патогенеза почечной недостаточности и уремии. Расстройства, возникающие при недостаточности ферментов орнитинового цикла, изложены в статье «Недостаточность ферментов цикла мочевины» (приложение «Справочник терминов» на компакт диске). Креатин и креатинин Уровни креатина и креатинина в крови и моче, как правило, существенно меняются при почечной недостаточности, гипотрофии мышц, миозитах и миастении, длительном голодании, СД. ДИСПРОТЕИНОЗЫ Диспротеинозы — патологические состояния, характеризующиеся изменением физикохимических свойств белков и расстройством их ферментативной, структурной, рецепторной и информационной функций. По преимущественной локализации патологического процесса различают клеточные и внеклеточные диспротеинозы. • Клеточные диспротеинозы рассмотрены в разделе «Дистрофии» главы 3 и в «Справочнике терминов» на компакт диске . • К внеклеточным диспротеинозам относят амилоидоз, гиалиноз, а также мукоидное и фибриноидное набухание. Амилоидоз — состояние, характеризующееся накоплением избытка аномальных комплексов белков и полисахаридов (гликопротеинов) в межклеточном пространстве, вокруг сосудов и в их стенках. Это приводит к существенным нарушениям функций органов и тканей, а нередко — к гибели организма. Основные проявления амилоидоза: † альбуминурия (результат нарушения реабсорбции альбуминов в почках). † гипопротеинемия (следствие печёночной недостаточности и альбуминурии). † артериальная гипотензия (развивается в результате гиповолемии и надпочечниковой недостаточности). † азотемия, уремия (следствие почечной недостаточность). Гиалиноз — состояние, сопровождающееся накоплением в соединительной ткани органов и тканей неамилоидного белка. Наиболее частые причины: хронические воспалительные процессы, состояния иммунной аутоагрессии и пропитывание соединительной ткани белками плазмы (например, при хронической артериальной гипертензии, СД, артериосклерозе). НАРУШЕНИЯ ОБМЕНА НУКЛЕИНОВЫХ КИСЛОТ Нарушения обмена нуклеиновых кислот характеризуются расстройствами синтеза и деструкции пиримидиновых и пуриновых оснований. ПИРИМИДИНЫ Урацил, тимин, цитозин, метил и оксиметилцитозин играют ключевую роль в обмене и функционировании ДНК, РНК, нуклеотидтрифосфатов и нуклеотидпирофосфатов. Два последних класса соединений являются поставщиками энергии в ряде метаболических реакций (например, при синтезе липидов и трансмембранном переносе веществ). ПУРИНОВЫЕ ОСНОВАНИЯ Аденин, гуанин, метиладенин, метилгуанин являются одним из основных компонентов нуклеиновых кислот, составной частью макроэргических соединений — аденинди и трифосфата, гуанинди и трифосфата и поставщиком мочевой кислоты — финального метаболита обмена пуринов. Мочевая кислота образуется, главным образом, в гепатоцитах и энтероцитах с участием ксантиноксидазы, а разрушается в кишечнике при участии бактерий с образованием глиоксалевой кислоты и аммиака. РАССТРОЙСТВА МЕТАБОЛИЗМА ПИРИМИДИНОВЫХ ОСНОВАНИЙ К расстройствам, сопровождающимся нарушением метаболизма пиримидиновых оснований, относятся оротацидурия, гемолитическая анемия и аминоизобутиратурия вследствие недостаточности 3-гидроксиизобутират дегидрогеназы. НАРУШЕНИЯ ОБМЕНА ПУРИНОВЫХ ОСНОВАНИЙ К основным проявлениям, вызванным нарушениями обмена пуриновых оснований, относят подагру, гиперурикемию, синдром Леша–Найена и гипоурикемию. ГИПЕРУРИКЕМИЯ Гиперурикемия — состояние, проявляющееся повышенной концентрацией мочевой кислоты в крови и, как следствие — в моче (см. статью «Гиперурикемия» в приложении «Справочник терминов» на компакт диске). ПОДАГРА
|
