УЧЕБНИК Инфекционные и паразитарные болезни. Том 1. Возианова Ж.И. (в word). УЧЕБНИК Инфекционные и паразитарные болезни. Том 1. Возианова Ж.. Инфекционные и паразитарные болезни в трех томах Том первый
 Скачать 6.07 Mb. Скачать 6.07 Mb.
|
|
Продром ж Клинические проявления Желтуха 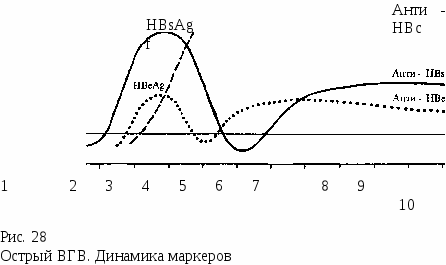 Пороговый уровень в крови Месяцы после заражения Основным недостатком всех вышеперечисленных методов является недостаточная чувствительность тест-систем, позволяющих определять соответствующие маркеры лишь при достаточно высокой их концентрации в крови. В последние годы все более широкое распространение получает ПЦР-полимеразная цепная реакция (PCR — polymerase chain reaction), отличающаяся не только очень высокой чувствительностью, но и очень высокой специфичностью. Это — маркер активной репликации вируса, позволяющий определять вирусную ДНК даже при отсутствии других маркеров в крови. Еще одним маркером активности процесса является фермент ДНК-полимераза, который информативен при исследовании больных с острым и хроническим ВГВ. Если раньше пункционную биопсию печени производили редко, главным образом с целью уточнения этиологии гепатита при хронической патологии печени, то сейчас это — одно из обязательных исследований, помогающих решить вопрос об активности процесса при хронических гепатитах. Так, гистологический индекс активности Knodell (HAI) рассчитывают по соотношению частоты перипортальных мосто-видных некрозов, фокальных некрозов, портального воспаления и фиброза. Такой метод дает значительно более надежную информацию о характере процесса в печени, тем более что полученные данные не всегда коррелируют с биохимическими показателями. Примерная формулировка диагноза. 1. Острый вирусный гепатит В (HBsAg+ ), желтушная форма, циклическое среднетяжелое течение.
4. Фульминантный острый ВГВ. ОПЭ III степени. Профилактика. Общая профилактика ВГВ включает :
Специфическая профилактика ВГВ делится на активную и пассивную. Активная профилактика заключается в проведении вакцинации. Многие вакцины созданы еще в 70-е годы. Используют два типа вакцин — плазменную и рекомбинантную. Плазменную вакцину готовят из высокоочищенного HBsAg, полученного из крови вирусоносителей с высоким его содержанием. Рекомбинантная вакцина произведена на основе HBsAg из рекомби-нантных штаммов, культивируемых на дрожжах. Наиболее известны Recombivax НВ, Engerix-B. Взрослых (группы риска) вакцинируют троекратно: вторую дозу вводят через 1 мес после первой, третью — через 6 мес после первой. Дозировки приводятся в соответствующих инструкциях, так как свойства вакцин различны. Если после окончания полного курса вакцинации контрольные исследования показывают, что уровень антител ниже 100 МЕ/л, вводят еще одну бустерную дозу. При правильно проведенной вакцинации и хорошей реактивности организма уровень антител 100—1000 МЕ/л сохраняется до 2 лет, затем постепенно начинает снижаться. Полагают, что бустерная доза должна быть назначена, если уровень антител падает ниже 10 МЕ/л. В большинстве случаев такая необходимость возникает через 4 года — 6 лет, иногда — позже. Особого внимания заслуживает вакцинация детей, особенно в регионах с высоким уровнем заболеваемости ВГВ. Таких детей вакцинируют троекратно (на первом месяце жизни, через 1 мес, а затем через 6 мес после первой вакцинации). Дети, родившиеся от матерей — носителей HBV или больных ВГВ, подвержены высокой степени риска заболеть ВГВ. Поэтому такому ребенку профилактические мероприятия (активно-пассивная иммунизация) проводят еще в родзале: сразу после рождения или в течение первого часа вводят 0,5 мл иммуноглобулина против ВГВ (HBIg) с высокой концентрацией антител. С интервалом в несколько часов вводят HBV-вакцину. В дальнейшем вакцину вводят через 1 и 6 мес после первой дозы, но существует мнение, что эффективность профилактических мероприятий у детей, рожденных от инфицированных матерей, повышается, если специфический иммуноглобулин будет введен не только при рождении ребенка, но и в трех- и шестимесячном возрасте. В Украине вакцинация детей против ВГВ была включена в график вакцинопрофилактики в 1996 г. Однако контингента для вакцинации и предложенные схемы введения вакцин нуждаются в уточнении. Отношение к вакцинации пока неоднозначное, несмотря на отчетливо выраженный протекторный иммунитет. Существуют, например, данные, что у привитых чаще обнаруживается мутантный HBV, а мутация может быть причиной того, что не вырабатывается иммунитет после прививки. Показана вакцинация:
— медицинскому персоналу, имеющему контакт с кровью и другими биологическими жидкостями различных больных, в том числе с ВГВ. Для пассивной иммунизации используют гипериммунный иммуноглобулин, получаемый из плазмы крови доноров с высоким уровнем антител к HBsAg. Контактным из групп риска его вводят в дозе 0,06 мл/кг массы тела, желательно в течение первых 24—48 ч после контакта. Эффективность действия иммуноглобулина сомнительна при его введении через 7 дней и позже после предполагаемого инфицирования. Порядок выписки из стационара. Реконвалесцентов выписывают из стационара не ранее чем через 3 нед от начала заболевания при условии клинического выздоровления. Умеренная гепатомегалия может сохраняться, но желтуха должна отсутствовать (у некоторых больных уровень билирубина в крови может превышать норму не более чем в 1,5—2 раза). НВеАд в крови не должен определяться, уровень цитоли-тических ферментов не должен превышать норму более чем в 1,5—2 раза. В течение 1-го месяца после выписки реконвалесцента наблюдает врач стационара (1 раз в 10—14 дней), затем — врач КИЗа. Контрольные осмотры проводят каждые 3 мес, при необходимости чаще. С диспансерного учета больного можно снимать при отсутствии HBsAg в крови и признаков хронизации. Реконвалесцентов допускают к работе не ранее чем через 4—5 нед после выписки из стационара, независимо от тяжести течения. Все реконвалесценты освобождаются от тяжелых работ и физкультуры на 6—12 мес. В течение 6 мес противопоказаны любые прививки, плановые операции. Сочетанное течение ВГА и ВГВ. В последнее время участились случаи, когда у больного одновременно диагностируют ВГА и ВГВ. Особенности течения такого сочетанного патологического процесса изучают, но уже в настоящее время существуют разные точки зрения на патогенез гепатитов-микст. Основные гипотезы оппонентов такие:
Для того чтобы достоверно можно было судить о характере взаимного влияния HAV и HBV, нужно знать, одновременно произошло заражение или речь идет о суперинфекции HAV, произошло инфицирование HAV носителя HBsAg или больного с активным процессом (возможны и другие варианты). Достоверные сведения могут быть получены только при использовании во время обследовния больных всех маркеров HAV и HBV в динамике. вирусный гепатит d Вирусный гепатит D, син. — дельта-гепатит (англ. — hepatitis D). Этиология. Возбудитель — HDV ■— представитель нового вида вирусов. Он занимает промежуточное положение между вирусами и вирои-дами, его классифицируют как рибозим. Это — дефектный «голый» вирус, не имеющий оболочки. HDV —простая частица, имеющая размеры 35—37 нм, содержащая в ядре кольцевидную одноцепочечную РНК. Свою оболочку вирус строит из HBsAg HBV. Эта оболочка необходима для проникновения вируса через мембрану гепатоцита. В настоящее время вирус активно изучают, благодаря чему постоянно поступает новая информация. Доказано, что HDV существует в двух формах •— малой и большой, которые различаются по активности репликации, степени патогенности. Малая форма обладает большей пато-генностью. Течение ВГО в значительной мере определяется генотипом вируса. В настоящее время-определяется три генотипа HDV: I (субтипы 1а и lb), И, III. I генотип встречается у жителей России, он нередко сочетается с гепатоцеллюлярной карциномой и циррозом печени. У жителей Южной Америки чаще обнаруживают HDV III генотипа. Второй генотип чаще встречается у жителей Тайваня. Он вызывает менее тяжелое течение заболевания, реже возникает и хронизация процесса. Не случайно, по-видимому, более чем у 40% больных, у которых возникали фульминантные формы ВГВ, обнаруживают и HDV. Особенностью HDV является способность неблагоприятно воздействовать на CD4 клетки и Т-лимфоциты. Вирус устойчив к действию высоких температур и кислот, но разрушается в щелочной среде. Эпидемиология. Источником инфекции является больной острым или хроническим ВГО или носитель HDV. Основной путь передачи — парентеральный, как и при ВГВ. Вертикальный путь существенной роли не играет. Не исключают возможности передачи вируса с помощью кровососущих насекомых. Часто вирус выявляют у больных болезнью Дауна, убедительного объяснения этому феномену пока нет. Факторы передачи HDV — кровь и другие биологические жидкости. Широкое использование иммуноглобулинов увеличивает риск распространения ВГО. Группы риска по BTD те же, что и при ВГВ. Но заболевание развивается лишь у лиц, имеющих HBsAg (больных или носителей), хотя вирус инфицирует и HBsAg-отрицательных лиц. Наиболее распространено носительство HDV в некоторых регионах Среднего Востока, в Венесуэле, на юге Италии, в Сибири. Во многих странах не предусмотрена обязательная регистрация ВГО, поэтому об истинной распространенности этой патологии судить трудно. Тем не менее, есть регионы, где ВГО встречается даже в виде эпидемий с высокой летальностью (лабрийская лихорадка в Бразилии, гепатит Сан-Марта в Колумбии). Как выяснилось в последние годы, ВГО не относится к числу «новых» заболеваний: в США антитела к HDV обнаружены в препаратах иммуноглобулинов, приготовленных еще в 1944 г. Патогенез. Путь внедрения вируса в организм такой же, как при ВГВ. Током крови вирус заносится в печень, где проникает в ядро гепатоцита. РНК вируса имеет кольцевую или нитчатую структуру, однако репликация 'полноценного вируса возможна только при наличии HBsAg, то есть только при острой или хронической ВГВ-инфекции, при которой HBsAg синтезируется в цитоплазме гепатоцита, попадая затем в кровь. HDV ингибирует синтез генома и генетических продуктов HBV в ядре, но использует HBsAg для построения своей оболочки. Таким образом, при ВГО угнетается репликация HBV. Образование новых вирусных частиц идет до тех пор, пока есть «строительный материал» — HBsAg. HDV без HBsAg не способен вызвать заболевание, но он может сохраняться в ядре гепатоцита и даже реплицироваться в небольших количествах за счет своего HBsAg. Аутоиммунными процессами сопровождается лишь 50% случаев хронического ВГО. Отсутствие эффекта от применения иммуносупрессивных препаратов при ВГО можно объяснить отсутствием иммунного воспаления. В результате непосредственного цитопатогенного действия вируса в печени возникают обширные поля некроза уже в начальный период заболевания в сочетании с признаками портального и лобулярного воспаления. В ходе болезни формируются и имунные реакции — появляются специфические антитела — анти-HDV. При одновременном инфицировании HBV и HDV чаще возникает острая инфекция. Это обусловлено действием на клетку одновременно двух вирусов с различным механизмом повреждения, это же является причиной частого развития тяжелых и фуль-минантных форм. При суперинфицировании HDV чаще формируются хронические формы. ВГО, таким образом, по своей сути — инфекция-микст. Иммунные к ВГВ лица, у которых в сыворотке обнаруживают ан-ти-HBs и анти-НВе, невосприимчивы к HDV, как и те, у кого отсутствуют все маркеры HBV. Клиника. Течение острогоВГИпротекает в двух вариантах. Первый вариант (коинфекция) возникает при одновременном заражении HBV и HDV. От ВГВ возникшее при этом заболевание отличается прежде всего более коротким инкубационным периодом. Уже в преджелтушный период у 60% больных бывает повышение температуры (иногда до высокой), у 30% больных лихорадка сохраняется и в желтушный период. Возможно и постепенное начало с выраженным диспепсическим синдромом (тошнота, рвота), артралгиями. Характерным признаком этого варианта течения острого ВГО является рано появляющаяся боль в правом подреберье и надчревной области, сохраняющаяся иногда в течение всего периода болезни. Остальные клинические проявления и течение заболевания типичны для ВГВ, но при сочетании с ВГО обычно наступает вторая волна клинических проявлений заболевания, которая, как правило, без проведения специальных исследований с использованием маркеров расценивается как рецидив ВГВ. Кроме того, в желтушный период может длительно (до 2 нед) сохраняться субфебрилитет, нередко появляется полиморфная сыпь. Почти у половины больных заболевание протекает тяжело, чаще, чем при других ВГ, возникают фульминантные формы с высокой летальностью. Чаще, чем при других способах заражения, фульминантные формы развиваются при внутривенном инфицировании (при переливании крови и ее компонентов), что, вероятно, связано с поступлением большого количества HBV и HDV. Длительность антигенемии коррелирует с тяжестью течения ВГО. Затяжное течение для коинфекции, однако, не характерно, хронический гепатит после перенесенного заболевания формируется редко. Второй вариант (суперинфекция) характеризуется наслоением HDV-инфекции на ВГВ, протекающий в форме острого или хронического гепатита, а также в форме носительства. Тяжесть течения заболевания обусловлена при этом главным образом длительностью предшествовавшего самостоятельного воздействия на печень HBV. Обычно начинается заболевание как ВГВ, но в дальнейшем болезнь характеризуется волнообразным течением (периодические клинические и ферментативные обострения) и быстрым нарастанием неблагоприятных признаков, свидетельствующих о хронизации: плотная печень, "сосудистые звездочки", пальмарная эритема и т.д. Часто развивается отечно-асцитическая форма. Для этого варианта течения острого ВГО характерна триада симптомов: озноб, повышение температуры, отечно-асцитический синдром. Ему свойственен и быстрый исход в хронический гепатит, а затем в цирроз печени (ранний). Выздоровление без остаточных явлений наблюдается лишь у 10 % больных. Фульминантные формы возникают нередко. Примерно у 6—7 % больных острый ВГО протекает в безжелтушной форме, а у отдельных больных может проявляться только повышением активности цитолитических ферментов. При легком течении ВГВ HDV выявляют примерно у 1—2 % больных, среднетяжелом — у 3—5 %, тяжелом — до 30 %, при фульминант-ных формах — наиболее часто. HDV-суперинфекция у здоровых носителей HBV может привести к тяжелому поражению печени. ХроническийВГИклинически полиморфен, похож на хронические гепатиты другой этиологии. У 1/3 больных длительно сохраняются желтуха, астеновегетативный синдром. Характерно снижение аппетита, прогрессирующее снижение массы тела. Рано обнаруживаются вторичные печеночные знаки (пальмарная эритема, "сосудистые звездочки"). Нередко возникают геморрагический и отечно-асцитический синдромы. Основная особенность хронического ВГО — быстрое (в течение 1 года — 2 лет) прогрессирование с исходом в цирроз печени. Процесс протекает волнообразно, с короткими неполными ремиссиями, периоды обострений характеризуются выраженной диспротеине-мией, гиперферментемией, повышенной тимоловой пробой, но даже в короткие периоды ремиссий полная нормализация этих показателей не наступает. Возможны кратковременные повышения температуры, желтуха. Увеличение селезенки может быть значительным и сочетаться с признаками гиперспленизма. Особенно активно хронический процесс протекает в первые месяцы и годы после инфицирования HDV. Осложнения, исходы. Осложнения, исход при ВГО такие же, как и при ВГВ, что не случайно, так как, по существу, имеет место инфекция-микст (ВГВ + ВГО), HDV усиливает некрогенное действие HBV. Чаще при такой микст-патологии возникает цирроз печени. Специфическая диагностика. Для выявления антигенов HDV используют те же методы, что и при ВГВ. В течение 1-й недели заболевания в сыворотке крови можно обнаружить HDV, затем быстро наступает сероконверсия. HDV длительно (пока больной жив) обнаруживают в крови лишь при фульминантных формах. Анти-HDV класса IgM в крови появляются сразу после исчезновения HDV и сохраняются обычно до 4 нед. Более длительное выявление IgM обычно свидетельствует о явной угрозе хронизации, так как иммуноглобулины этого класса отражают активность вирусной репликации. Анти-HDV класса IgG появляются несколько позже, а после 4—5 нед полностью сменяют IgM. Но при суперинфекции в крови довольно длительное время можно обнаружить иммуноглобулины обоих классов одновременно. При хроническом ВГО длительное время (годы) обнаруживают в высоких титрах анти-HDV IgG, а при обострениях одновременно появляются и анти-HDV IgM. При ВГО в крови могут одновременно обнаруживаться и различные маркеры HBV — HBsAg, НВеАд, анти-НВс и другие (их сочетание оп ределяется периодом и тяжестью болезни). При всех вариантах течения BTD в период активной репликации вируса методом ПЦР можно обнаружить HDV — РНК. Поэтому этот метод может использоваться для контроля эффективности лечения и прогнозирования исходов. При сочетании ВГВ с ВГО из крови может исчезать HBsAg. Поэтому во всех случаях, когда у больного с явными признаками ВГВ отсутствует HBsAg или обнаруживается только анти-НВс, необходимо исключить наличие сопутствующей D-инфекции либо pre-S-мутант ВГВ. Маркеры HDV следует искать в сыворотке крови и у всех больных с фульминантными формами ВГВ. У больных с циррозом персистирование HDV и HBV свидетельствует о большой вероятности возникновения гепатоцеллюлярной карциномы в ближайшие годы. |
