Издательский дом Питер
 Скачать 5.79 Mb. Скачать 5.79 Mb.
|
|
12.1.5. Полифункциональные (комплексные) препараты К комплексным кровезаменителям относят препараты, одновременно или последовательно обеспечивающие два или несколько эффектов: они могут оказывать нормализующее действие не только на гемодинамику, но и на другие функции организма: корректировать водно-солевой обмен и кислотно-основное состояние, уменьшать содержание токсических веществ в крови, повышать энергопродукцию в условиях ограниченного снабжения тканей кислородом. Плазмозамещающие растворы ___________________549 Мафусол — раствор солей (хлорида натрия, хлорида калия и хлорида магния) и фумарата натрия. Он оказывает гемодинамический эффект, уменьшает проявления гипоксии, повышает диурез. Гиперосмолярность препарата препятствует дегидратации тканей, вызывает аутогемодилюцию, уменьшает вязкость крови. При шоке легкой и средней степени тяжести (геморрагическом, ожоговом, травматическом, операционном) начинают со струйного введения препарата, постепенно переходя на капельные инфузии (до 2-2,5 л). При тяжелых интоксикациях (перитонит, сепсис, кишечная непроходимость и др.) показано введение 2-3 л раствора мафусола в сутки, возможно, в комбинации с де-зинтоксикационными кровезаменителями. Б. А. Барышев (2001) наряду с мафусолом относит полиоксифумарин (содержит фумарат) и реамберин (содержит сукцинат) к группе инфузи-онных антигипоксантов. Инфузионные антигипоксанты предназначены для повышения энергетического потенциала клетки. За счет введенного в растворы фумарата или сукцината они: — восстанавливают клеточный метаболизм, активируя адаптацию клетки к недостатку кислорода, за счет участия в реакциях обратимого окисления и восстановления в цикле Кребса; — способствуют утилизации жирных кислот и глюкозы клетками; — нормализуют кислотно-основной баланс и газовый состав крови. Полифер — 6 % раствор частично гидролизованного декстрана с 0,15-0,2 % комплексом железа. Эффективность полифера при острой кровопоте-ре аналогична таковой инфузированного полиглюкина и способствует улучшению гемодинамики, снижению вязкости крови и агрегации эритроцитов. Наличие в его составе ионов железа усиливает эритропоэз и синтез гемоглобина. Наиболее целесообразно использовать полифер при оперативных вмешательствах у больных с исходной анемией, обусловленной опухолями или длительно текущими гнойно-деструктивными процессами. Реоглюман — 10 % раствор декстрана с добавлением 5 г маннита и 0,9 г хлорида натрия. Оказывает выраженное гемодинамическое действие как реополиглюкин и обусловливает хороший диуретический эффект. Доза введения при шоке — 0,4-0,8 л, после хирургических операций на магистральных сосудах — ежедневно по 0,4 л, при острой почечной недостаточности с сохраненной фильтрацией — 0,4-0,8 л однократно. Полиглюсолъ — 6 % раствор декстрана с добавлением сбалансированных по ионному составу солей из расчета на 1 л: хлорид натрия — 5,26 г, хлорид калия — 0,37 г, хлорид кальция — 0,55 г, хлорид магния — 0,3 г, ацетат натрия — 6,8 г. По гемодинамическому действию полиглюсоль сопоставим с по-лиглюкином, корригирует солевой обмен, уменьшает метаболический ацидоз. Лонгастерил-40 — 10 % раствор декстрана с молекулярной массой 40 к Да в 5 % растворе сорбита. Обладает реокорригирующим действием, позволяет 550____________________Глава 12. Альтернативы переливанию крови восполнять О ЦК и способствует улучшению микроциркуляции и почечного кровотока. В лечении геморрагического шока показана эффективность рондферри-на — кровезаменителя на основе радиационно-химически модифицированного декстрана, комплексно связанного с микроэлементами — железом, кобальтом и медью. В. А. Климкович и В. Н. Гапанович (2001) установили, что железо, входящее в состав рондферрина, активно включается в процессы кроветворения, что обеспечивает высокие противоанемические свойства нового препарата. При использовании рондферрина быстрее и стабильнее нормализуются волемические показатели, артериальное давление, скорость тканевого кровотока, кислотно-основное состояние и газовый состав крови, уровни содержания в плазме крови альбумина и общего белка, активность процессов пере-кисного окисления, липидов. 12.2. Альтернативы трансфузиям эритроцитов Учитывая эволюцию взглядов на определение показаний к гемотрансфу- зиям, наиболее простая альтернатива переливанию крови — отказ от этой процедуры. Это находится в рамках законных прав пациента. Однако, как показывает практика лечения членов секты Свидетелей Иеговы, вместе с «во дой» (риском гемотрансфузии) выплескивается и «ребенок» (эффективность гемотрансфузии). Последствия такого решения могут быть плачевны и даже фатальны. I Существенно уменьшает риск гемотрансфузии элиминация лейкоцитов методом фильтрации. Весьма эффективны технологии инактивации микроорганизмов, которые разрабатываются и в отношении клеточных компонентов. Серьезные практические достижения и большие перспективы связаны с разработкой и внедрением препаратов рекомбинантных белков крови, в том числе и гемоглобина (табл. 125). 12.2.1. Донорские эритроциты, унифицированные по АВО-специфичности: реальность и перспективы При переливаниях эритроцитсодержащих сред, особенно в экстремальных условиях, могут возникать проблемы с: — обеспечением нужным количеством крови; 551 Альтернативы трансфузиям эритроцитов Таблица 125 Рекомбинантные гомологи белков крови [Prowse С. V., 1998]
— обеспечением нужным количеством доноров; — возможностью проведения иммуногематологических исследований; — дефицитом времени на проведение трансфузиологических процедур. В войнах второй половины XX века применялся один из возможных вариантов решения этой проблемы — использование эритроцитов «универсальной» группы крови О (I). Серьезное препятствие созданию запасов таких сред — ограниченная распространенность группы крови О (I) в популяции (около 35 %). Как упоминалось в главе 6, специфичность антигенов Н, А и В определяется соответственно тремя терминальными иммунодоминантными сахарами — фукозой, N-ацетилгалактозамином и галактозой. Следовательно, существует возможность с помощью соответствующих ферментов трансформировать эритроциты других групп крови в «универсальные» эритроциты 0(1) группы и тем самым сделать возможным переливание таких эритроцитов без учета групповой принадлежности реципиента. Этот процесс схематично изображен на рис. 41. Для отщепления терминальных углеводов (на рисунке показано пунктиром) необходимы специфические ферменты: — сс-галактозаминидаза — для антигена А; — cc-галактозидаза — для антигена В. Оставшаяся часть групповых антигенов имеет на конце фукозу, характерную для Н-антигена — общего для всех эритроцитов. 552 Глава 12. Альтернативы переливанию крови 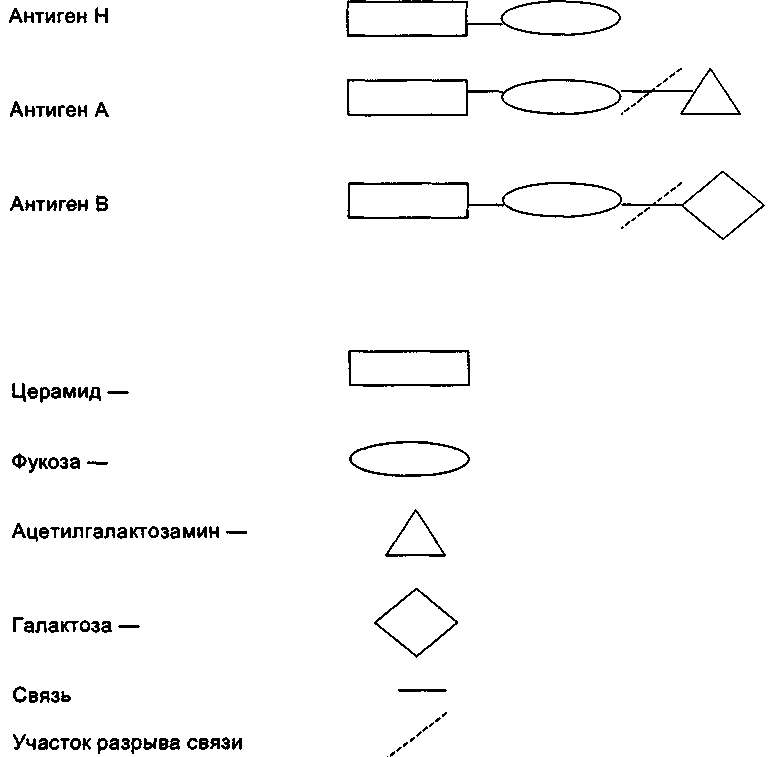 Рис. 41. Строение антигенов системы группы крови АВО и возможность их «универсализации». Альтернативы трансфузиям эритроцитов_____________________SS3 Фактически, invitroнужно провести процесс, обратный формированию группоспецифических антигенов, при котором в процессе созревания красной клетки тоже ферментативным путем N-ацетилгалактозамин и галактоза присоединяются к уже имеющемуся на клетке церамиду. После многолетних исследований в США [J. Goldstein и соавт.] с помощью высокоочищенной сс-галактозидазы из зерен кофе из эритроцитов группы В (III) получены клетки специфичности 0 (I), не уступающие по своим иммунологическим, биохимическим и функциональным свойствам нативным эритроцитам. Методика трансформации сходна с производством отмытых эритроцитов. Показана высокая клиническая эффективность трансформированных эритроцитов, острых и отдаленных побочных эффектов не отмечено. Ключевое условие трансформации эритроцитов — использование ферментов высокой специфичности, стабильности, чистоты и рН-оптимума. Фермент, пригодный для обработки эритроцитов группы А (II), не найден во многом вследствие полиморфизма структуры подтипов антигена А. Недостатки «универсальных» эритроцитов: — сохранение антигенов других систем групп крови; — высокая стоимость ферментных препаратов. Тем не менее разработка технологий производства'«универсальных» эритроцитов признана перспективной. Во-первых, перспективен путь удешевления ферментов (например, в США испытывается рекомбинантная сс-галак-тозидаза). Во-вторых, определенную экономию принесет устранение необходимости определения групповой принадлежности каждой порции донорской крови, снижение расходов на подбор и транспортировку «универсальных» эритроцитов. В-третьих, по сравнению с искусственными переносчиками кислорода «универсальные» эритроциты наиболее органичны. 12.2.2. Неоциты Эритроциты отличаются по плотности: удельный вес клеток увеличивается по мере их старения. Соответственно можно выделить менее плотную фракцию более молодых клеток — «неоцитов» с более длительной циркуляцией в сосудистом русле реципиента. Как показали Т. Spanos и соавт. (1996) на примере больных талассемией, использование неоцитов особенно эффективно у «трансфузиозависимых» пациентов. 12.2.3. Кровезаменители с газотранспортной функцией Одним из методов, альтернативных применению аллогенной крови, является использование кровезаменителей, обладающих функцией переноса газов 554____________________Глава 12. Альтернативы переливанию крови крови и прежде всего кислорода и углекислого газа. Зачастую, особенно в прессе, при характеристике этих препаратов используют термин «искусственная кровь», что, конечно, неверно, так как эти кровезаменители в определенной степени замещают только одну (правда, весьма существенную) функцию крови — газотранспортную. В качестве же истинно «искусственной крови» можно представить себе некий гипотетический комплексный полифункциональный коллоидно-металлоидный раствор, обеспечивающий, помимо переноса газов крови, волемический эффект, транспорт питательных и биологически активных веществ, регуляцию водно-солевого баланса и кислотно-основного равновесия, экскреторную функцию и т. д. Кроме того, этот заменитель крови должен быть нетоксичным, гарантировать абсолютную невозможность заражения реципиента любыми инфекционными заболеваниями и быть более стабильным при хранении, чем натуральная кровь. В проблеме поиска кровезаменителей с газотранспортной функцией активно развиваются два направления: 1) использование в качестве субстрата, переносящего газ, эмульсий перфторуглеродов (ПФУ); 2) использование модифицированного гемоглобина в роли переносчика газов. 12.2.3.1. Эмульсии перфторуглеродов В отличие от гемоглобина ПФУ не образуют химических соединений с кислородом, а растворяют его и другие газы согласно закону Генри. Эта связь линейная, и степень растворения кислорода в ПФУ прямо пропорциональна его парциальному давлению (в отличие от сигмовидной кривой диссоциации оксигемоглобина). Внутривенное введение гидрофобных ПФУ возможно только в виде эмульсий. В связи с тем, что ПФУ не подвергаются метаболическим превращениям в организме, они считались биологически инертными (до тех пор, пока не было обнаружен факт стимуляции детоксицирующей функции печени). Частицы внутривенно введенной эмульсии ПФУ быстро (в течение 12-20 ч) удаляются из сосудистого русла. Клетками ретикулоэндотелиальной системы (РЭС) захватывается до 30 % ПФУ, которые временно аккумулируются в печени, селезенке и костном мозге. Из кровотока и из клеток РЭС все ПФУ выводятся через дыхательные пути. Препараты ПФУ для внутривенного введения состоят из: — собственно перфторуглеродов; — солевой композиции; — эмульгатора, обеспечивающего стабильность эмульсии. Выбор ПФУ для кровезаменителя определяется соотношением кислородной емкости ПФУ, способностью образовывать стабильную эмульсию и длительностью задержки в тканях. Кислородная емкость ПФУ зависит от их химической структуры. Газотранспортные свойства эмульсии ПФУ зависят Альтернативы трансфузиям эритроцитов_____________________555 от концентрации ПФУ в эмульсии, размера ее частиц и реологических характеристик препарата. ПФУ как основа кровезаменителей должны удовлетворять следующим требованиям: — достаточной кислородной емкости; — отсутствию накопления в тканях; — высокой степени очистки; — отсутствию побочных эффектов. Наиболее изучены такие ПФУ первого поколения, как перфтордекалин (ПФД) и перфтортрипропиламин (ПФТПА), а из эмульгаторов — плюро-ник F-68 и его композиция с фосфолипидами яичного желтка. Все эти вещества и вошли в состав первого КЗПК на основе ПФУ — препарата Fluosol-DA 20 % (Green Cross, Япония). Содержание ПФУ в препарате составляло 20 весовых (11 объемных) процентов, отношение ПФД к ПФТПА равнялось 70:30, причем ПФД (период полувыведения — 7 дней) являлся основным кислородпереносящим компонентом, а ПФТПА (период полувыведения — 65 сут) обеспечивал стабильность. Размер частиц эмульсии не превышал 0,2 мкм, препарат необходимо было хранить в замороженном состоянии. При изучении биологических свойств Fluosol-DA оказалось, что препарат в ряде случаев снижал артериальное давление и содержание нейтрофильных лейкоцитов, что являлось проявлением его реактогенности. На первый препарат на основе ПФУ — Fluosol-DA — клиницисты возлагали большие надежды, считая его идеальным кандидатом в кровезаменители-переносчики кислорода вследствие большой кислородной емкости и биохимической инертности. Препарат был широко исследован при лечении острой кровопотери как в Японии, так и в США. В Японии к 1986 г. Fluosol-DA был перелит более чем 400 пациентам (в дозе 30 мл эмульсии на 1 кг массы тела больного, т. е. 6 г перфторуглеродов на 1 кг массы тела), которые принадлежали к секте Свидетелей Иеговы и по религиозным соображениям отказались от переливания крови. Инфузия препарата приводила к улучшению кислородного режима организма и стабилизации гемодинамики. В США клинические наблюдения у подобных больных с выраженной анемией (концентрация гемоглобина в среднем была на уровне 46 г/л) показали, что Fluosol-DA в дозе 30 мл/кг увеличивал содержание кислорода в плазме (при условии дыхания пациента смесью, обогащенной кислородом), причем этот эффект сохранялся в течение 12 ч после инфузии. Однако применение фторорганической эмульсии не оказывало существенного влияния на результаты лечения больных с геморрагическим шоком. В процессе клинического изучения Fluosol-DA были выявлены некоторые побочные эффекты — боли за грудиной, лейкопения, обусловленные, по-видимому, активацией системы комплемента. 556 ____ ______________Глава 12. Альтернативы переливанию крови Более плодотворными оказались попытки изучить эффективность Fluosol-DA при лечении ишемии миокарда. Предполагалось, что субмикронная эмульсия ПФУ способна доставить кислород через суженные коронарные артерии к ишемизированным участкам сердечной мышцы и тем самым уменьшить последствия острого нарушения коронарного кровотока. Эта гипотеза получила свое подтверждение в экспериментах на препаратах изолированного сердца крыс, кроликов и собак, в опытах на целостном организме с управляемой гемодилюцией и на модели инфаркта миокарда. Fluosol-DA и эмульсии других ПФУ (перфтортрибутиламин и перфторадамантат) проявили себя так же как эффективные кардиоплегические агенты. Тщательные клинические рандомизированные исследования, осуществленные в США в середине 1980-х гг., показали целесообразность использования Fluosol-DA при лечении острого инфаркта миокарда и в качестве кардиопротектора при проведении коронарной ангиопластики. Применение оксигенированной фторорга-нической эмульсии уменьшало болевой синдром, улучшало электрографические параметры деятельности сердца в послеоперационном периоде. Процент посттрансфузионных реакций колебался на уровне 2 %. Дальнейший поиск эффективных ПФУ привел к получению соединений, линейных по структуре. Оказалось, что линейные ПФУ лучше растворяют кислород и способны в меньшем объеме переносить то же количество кислорода, что и циклические соединения типа ПФД. К подобным веществам относятся бисфторбутилэтилен и перфтороктилбромид (ПФОБ). Последний составил основу препарата ПФУ второго поколения Oxygent (Alliance Pharm. Corp., США). Эта эмульсия привлекает своей стабильностью и быстротой выведения ПФУ из клеток РЭС. Большинство результатов последних лет получено в процессе клинических испытаний пока незарегистрированного препарата Oxygent. В стадии исследования находятся и другие препараты, например Therox (Dupont, США), Oxyfluor (HemoGen, США). Первый отечественный препарат с газотранспортной функцией — пер-фторан — создан в Институте теоретической и экспериментальной биофизики РАН (Пущине, Московская область) и в настоящее время разрешен к широкому клиническому применению. Состав перфторана: — перфтордекалин — 13 г; — перфторметилциклогексилпиперидин — 6,5 г; — проксанол — 4 г; — натрия хлорид — 0,6 г; — магния хлорид — 0,019 г; — калия хлорид — 0,039 г; — натрия гидрокарбонат — 0,065 г; — глюкоза — 0,2 г; — натрия гидрофосфат — 0,02 г; Альтернативы трансфузиям эритроцитов_____________________557 — вода для инъекций — до 100 мл. Растворимость кислорода — 6-7 об % при рО2 760 мм рт. ст., вязкость — 2,5 сП, осмолярность — 280-310 мосм/л, рН — 7,2-7,8, содержание ионов фтора — не более 10 мкмоль/л, средний размер частиц — 0,07 мкм. Установлено, что перфторан: — осуществляет кислородтранспортную функцию, на уровне микроциркуляции снабжает кислородом ткани через наиболее мелкие капилляры, увеличивая эффективную площадь сосудов и минутный объем кровотока; — создает условия для быстрого и полного освобождения кислорода из эритроцитов в результате большого значения константы диффузии для кислорода и углекислого газа в эмульсии и путем сдвига кривой диссоциации оксигемоглобина; — уменьшает вязкость системы эритроциты-плазма-эмульсия, увеличивая тем самым минутный кровоток; — осуществляет протекторную функцию, стабилизирует трансмембранный градиент ионов калия, кальция, водорода и воды, повышает устойчивость клеточных мембран к действию осмотических, механических и химических повреждающих агентов, уменьшает гемолиз, агрегационную способность и вязкость эритроцитов; — является эффективным жидким сорбентом с развитой активной поверхностью, площадь которой составляет 600 м2 в каждых 100 мл эмульсии; каждый миллилитр перфторана связывает 10 мг липидов. Перфторан — единственный препарат, который действует при жировой эмболии сразу, а не через 12-18 ч, как это бывает при введении липостабила; — обладает антиоксидантным действием; — активирует дезинтоксикационную функцию печени; — не оказывает токсического влияния на органы и ткани, не обладает канцерогенностью, мутагенностью, эмбриотоксичностью. Инфузия препарата повышает устойчивость организма животных к кро-вопотере, обеспечивает поддержание на высоком уровне парциального давления кислорода в смешанной венозной крови, а также минутного объема кровообращения и системного транспорта кислорода. Размер частиц эмульсии перфторана невелик (рис. 42), что выгодно отличает его от зарубежных препаратов ПФУ. Показания к применению перфторана: — острая и хроническая гиповолемия; — нарушения микроциркуляции, тканевого газообмена и метаболизма разной этиологии (гнойно-септические состояния, нарушения мозгового кровообращения, жировая эмболия, инфекции, респираторный дистресс-синдром взрослых, ДВС-синдром); — защита донорских органов (подготовка донора и реципиента); — использование в аппарате искусственного кровообращения; |
