Струков Патологическая анатомия. Литература для студентов медицинских институтов А. И. Струков В. В. Серов Патологическая анатомия Издание второе
 Скачать 16.97 Mb. Скачать 16.97 Mb.
|
|
Исход инфаркта зависит от особенностей причинного фактора и заболева- ния, которое осложняет инфаркт, от состояния организма и органа, в кото- ром он развивается, и от размеров инфаркта. Небольшие фокусы ишемического некроза могут подвергаться а у т о л и - з у с последующей полной регенерацией. Наиболее частый благоприятный ис- ход инфаркта, развивающегося по типу сухого некроза, — его о рганиза- ния и образование рубца (рис. 50). Организация инфаркта может завершиться его п е т р и ф и к ацией ил и г ем о сидероз ом, если речь 92 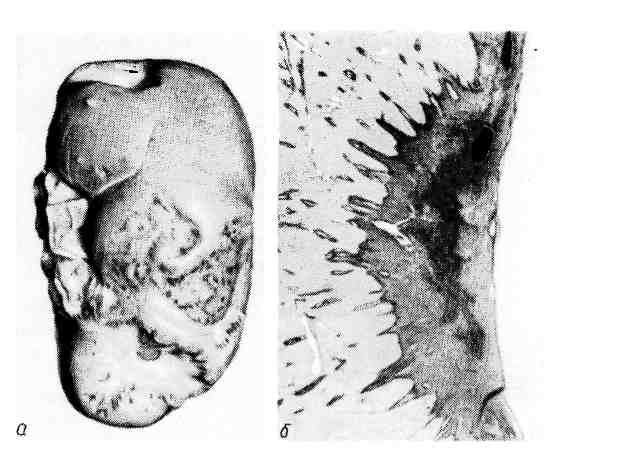 Рис. 50. Исход инфаркта. а — втянутые рубцы на поверх- ности почки после заживления инфаркта; б — рубец на месте ин- фаркта в селезенке (лупа). идет об организации геморрагического инфаркта. На месте инфаркта, разви- вающегося по типу колликвационного некроза, например в мозге, образуется киста. Неблагоприятный исход инфаркта — его гнойноерасплавление, ко- торое обычно связано с тромбобактериальной эмболией при сепсисе. Такие инфаркты называются септическими. Значение инфаркта для организма чрезвычайно велико и прежде всего по- тому, что инфаркт — это ишемический некроз. Все, что было сказано о значе- нии некроза, относится и к инфаркту. Однако важно отметить, что инфаркт является одним из самых частых и грозных осл.ожнений ряда сердечно-сосу- дистых заболеваний. Это прежде всего атеросклероз и гипертоническая бо- лезнь. Необходимо отметить также, что инфаркты при атеросклерозе и гипер- тонической болезни наиболее часто развиваются в жизненно важных органах — сердце и головном мозге, и это определяет высокий процент слу- чаев скоропостижной смерти и инвалидизации. Медико-социальное значение инфаркта миокарда и его последствий позволило выделить его как проявле- ние самостоятельного заболевания — и шеми ческой болезни сердца. Стаз Стаз (от лат. stasis — остановка) — остановка тока крови в сосудах ми- кроциркуляхорнохо русла, главным образом в капиллярах. Остановке тока крови обычно предшествует резкое его замедление, что обозначается как предстатическое состояние, или предстаз. В механизме стаза основное значение имеют изменения реологиче- ских свойств крови, представленные усиленной внутрикапил- лярной агрегацией эритроцитов, что ведет к увеличению сопроти- вления току крови по капиллярам, замедлению его и остановке. Гемолиз и свертывание крови при стазе не наступают. Состояние крови, в основе которого лежит агрегация эритроцитов, получило название слалжа (от англ. sludge — густая кровь, тина). Основными особенностями крови при сладже считают прилипание друг к другу эритроцитов, лейкоцитов или тромбоцитов и нарастание вяз- кости плазмы, что приводит к затруднению перфузии крови через сосуды микроциркуляторного русла. 93 очень рано в ткани на этой стадии исчезает гликоген, возникает нарушение ионного состава клеток (выход ионов магния и калия и поступление в клетку ионов кальция и натрия), снижается активность дыхательных ферментов, про- исходит набухание и деструкция митохондрий. Эти изменения способствуют закислению среды, денатурации белков и гидратации ткани. Возникает мест- ная смерть. Диагностика ишемической стадии инфарктов возможна на основании как микроскопических, так и макроскопических критериев. Для микроскопической диагностики используют гистохимические методы (исчез- новение гликогена, снижение активности большинства дегидрогеназ), электронную микроскопию (исчезновение гликогена, деструкция митохондрий) и люминесцентную микроскопию с исполь- зованием ряда флюорохромов (изменение цвета свечения зоны ишемии). Для макроскопи- ческойдиагностики применяют различные соли тетразолия, теллурит калия, которые вне участков ишемии (где активность дегидрогеназ высокая) восстанавливаются и окрашивают ткань в серый или черный цвет, а участки ишемии (где активность ферментов снижена или от- сутствует) остаются неокрашенными. Морфологическая характеристика ишемической стадии инфаркта имеет большое практическое значение, особенно при инфарктах миокарда и голов- ного мозга. Некротическая стадия инфаркта — это стадия аутолиза мертвой ткани. Поэтому для нее характерны все морфологические признаки некроза. Непосредственной причиной развития инфаркта являются: длительный спазм, тромбоз или эмболия артерии, а также функциональ- ное напряжение органа в условиях недостаточного его кро- воснабжения. Огромное значение для возникновения инфаркта имеет недостаточ- ность анастомозов и коллатералей, которая зависит от степени поражения стенок артерий и сужения их просветов (атеросклероз, облитери- рующий эндартериит), от степени нарушения кровообращения (например, ве- нозного застоя) и от уровня выключения артерии тромбом или эмболом. По- этому инфаркты и возникают обычно при тех заболеваниях, для которых характерны тяжелые изменения артерий и общие расстройства кровообраще- ния (ревматизм, пороки сердца, атеросклероз, гипертоническая болезнь, за- тяжной септический эндокардит). Острой недостаточностью коллатерального кровообращения обусловлено и развитие инфаркта при функциональном отя- гощении органа, обычно сердца, кровоснабжение которого нарушено. С недостаточностью анастомозов и коллатералей связано развитие венозных инфарктов при тромбозе вен в условиях застойного полно- кровия. Для возникновения инфаркта большое значение имеет также состояние тканевого обмена, т. е. метаболический фон, на котором развивается ишемический инфаркт. Обмен веществ в органах и тканях, в которых возни- кает инфаркт, как правило, нарушен; причиной нарушения является гипоксия, обусловленная общими расстройствами кровообращения. Лишь закупорка крупных магистральных артерий может привести к омертвению без предше- ствующих расстройств кровообращения и метаболических нарушений в ткани. Исход инфаркта зависит от особенностей причинного фактора и заболева- ния, которое осложняет инфаркт, от состояния организма и органа, в кото- ром он развивается, и от размеров инфаркта. Небольшие фокусы ишемического некроза могут подвергаться а у т о л и - з у с последующей полной регенерацией. Наиболее частый благоприятный ис- ход инфаркта, развивающегося по типу сухого некроза, — его организа- ция и образование рубца (рис. 50). Организация инфаркта может завершиться его петрификацией или гемосидерозом, если речь 92 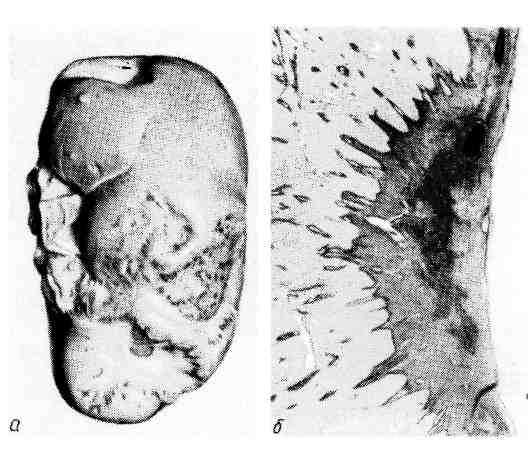 Рис. 50. Исход инфаркта. а — втянутые рубцы на поверх- ности почки после заживления инфаркта; б - рубец на месте ин- фаркта в селезенке (лупа). идет об организации геморрагического инфаркта. На месте инфаркта, разви- вающегося по типу колликвационного некроза, например в мозге, образуется киста. Неблагоприятный исход инфаркта — его гнойное расплавление, ко- торое обычно связано с тромбобактериальной эмболией при сепсисе. Такие инфаркты называются септическими. Значение инфаркта для организма чрезвычайно велико и прежде всего по- тому, что инфаркт — это ишемический некроз. Все, что было сказано о значе- нии некроза, относится и к инфаркту. Однако важно отметить, что инфаркт является одним из самых частых и грозных осложнений ряда сердечно-сосу- дистых заболеваний. Это прежде всего атеросклероз и гипертоническая бо- лезнь. Необходимо отметить также, что инфаркты при атеросклерозе и гипер- тонической болезни наиболее часто развиваются в жизненно важных органах — сердце и головном мозге, и это определяет высокий процент слу- чаев скоропостижной смерти и инвалидизации. Медико-социальное значение инфаркта миокарда и его последствий позволило выделить его как проявле- ние самостоятельного заболевания — ишемической болезни сердца. Стаз Стаз (от лат. stasis — остановка) — остановка тока крови в сосудах ми- кроциркулятарного русла, главным образом в капиллярах. Остановке тока крови обычно предшествует резкое его замедление, что обозначается как предстатическое состояние, или предстаз. В механизме стаза основное значение имеют изменения реологиче- ских свойств крови, представленные усиленной внутрикапил- лярной агрегацией эритроцитов, что ведет к увеличению сопроти- вления току крови по капиллярам, замедлению его и остановке. Гемолиз и свертывание крови при стазе не наступают. Состояние крови, в основе которого лежит агрегация эритроцитов, получило название с л а д ж а (от англ. sludge — густая кровь, тина). Основными особенностями крови при сладже считают прилипание друг к другу эритроцитов, лейкоцитов или тромбоцитов и нарастание вяз- кости плазмы, что приводит к затруднению перфузии крови через сосуды микроциркуляторного русла. 93 Развитию внутрикапиллярной агрегации эритроцитов способствуют: изменения капилляров, ведущие к повышению проницаемости их стенок; нарушения физико-химических свойств эритроцитов, выражающие- ся в снижении их поверхностного потенциала; изменения состава белков крови за счет увеличения грубодисперсных фракций; дисциркуляторные расстрой- ства — венозное полнокровие (застойный стаз) или ишемия (ишеми- ческий стаз), нарушения иннервации микроциркуляторного русла. Причиной развития стаза являются дисциркуляторные нарушения, они мо- гут быть связаны с действием физических (высокая температура, холод) и хи- мических (кислоты, щелочи) факторов, развиваются при инфекционных (на- пример, малярия, сыпной тиф) и неинфекционных (например, пороки сердца, ишемическая болезнь сердца) заболеваниях. Последствия и значение стаза определяются не только его длительностью, но и чувствительностью органа или ткани к кислородному голоданию (маля- рийная кома на почве стаза в капиллярах головного мозга). Стаз — явление обратимое. Состояние после разрешения стаза называется постстати- ческим. Необратимый стаз ведет к некробиозу и некрозу. Тромбоз Тромбоз (от греч. thrombosis — свертывание) — прижизненное свертыва- ние крови в просвете сосуда или в полостях сердца. Образующийся при этом сверток крови называют тромбом. При свертывании лимфы также говорят о тромбозе и внутрисосудистый сверток лимфы называют тромбом, однако закономерности лимфотромбоза и гемогромбоза различны. Тромбоз — патологический процесс, в основе которого лежит физиологиче- ское свойство крови подвергаться свертыванию. Свертывание крови — ферментативный аутокаталитический процесс, описанный отече- ственным физиологом А. А. Шмидтом в 1864 г. Согласно современному представлению, схема свертывания крови включает четыре стадии: I — протромбокиназа+ активаторы-> тромбокиназа (активный тромбопластин); II — протромбин + Са2++тромбокиназа->тромбин;
Установлено, что процесс свертывания крови совершается в виде каскадной реакции (теория «каскада») при последовательной активации белков-предшественников, или факторов свертывания, находящихся в крови или тканях. На этом основании различают внутреннюю (кровь) и внешнюю (ткань) свертывающие системы. Взаимоотношения внутренней и внешней систем представлены на схеме V [по Б. А. Кудряшову, 1975]. 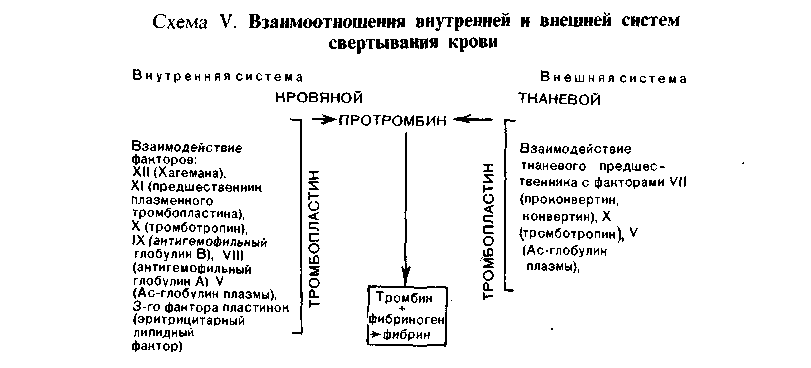 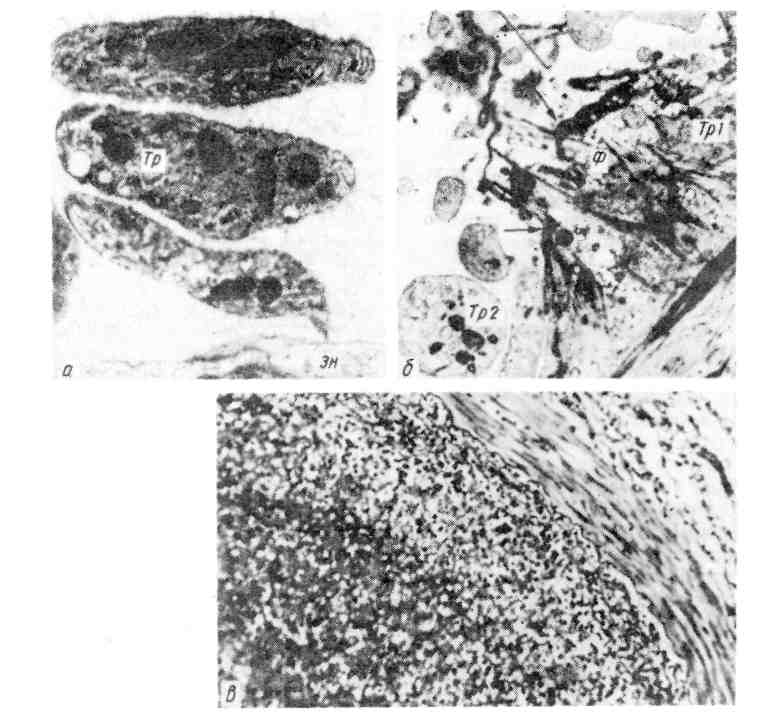 Рис. 51. Морфогенез громбообразования. а — первая стадия образования тромба. Небольшие скопления тромбоцитов (Тр) около поврежденной эндотелиальной клетки (Эн). Тромбоциты расположены на некотором расстоянии друг от дру- га, х 14000 (по Ашфорду и Фримену); б - вторая стадия образования тромба. В участке разрушенного эндотелия видны скопления тромбоцитов (Тр1) и фибрина (Ф); Тр2 - неизменённые тромбо- циты, х 7750 (по Ашфорду и Фримену); в — тромботические массы, состоящие из фибрина, лейкоцитов и агглютинирующихся эритроцитов. Большим достижением было доказательство наличия, помимо свертывающей, п р о т и в о- свертывающей системы крови; причем в последнее время находят возможным говорить о двух противосвертывающих системах (Б. А. Кудряшов). Первая из них представлена есте- ственными антикоагулянтами, такими, как антитромбин, гепарин, система фибрино- лизина (профибринолизин, или плазминоген; фибринолизин, или плазмин; их активаторы и ин- гибиторы). Вторая система — рефлекторн о-гуморальной регуляции гемостаза. Она включается в том случае, когда первая оказывается несостоятельной. Действие этой (вто- рой) противосвертывающей системы заключается в том, что при достижении в крови пороговой концентрации тромбина происходит рефлекторное возбуждение хеморецепторов кровеносного русла. Это ведет к выбросу в кровь гепарина и активаторов фибринолизина. В результате отно- сительного избытка гепарина блокируется активность тромбина, выброс активаторов плазмино- гена приводит к относительному избытку плазмина и лизису фибрина. Можно считать доказанным, что свертывающая и противосвертывающая системы являются взаимосвязанными частями единой системы гемостаза. Таким образом, тромбоз представляет собой проявление нарушенной регуляции единой системы гемостаза жид- кого состояния крови в сосудистом русле. 95 Механизм тромбообразования складывается из четырех последовательных стадий: агглютинации тромбоцитов, коагуляции фибриногена и образования фибрина, агглютинации эритроцитов, преципитации белков плазмы. Агглютинации тромбоцитов предшествует выпадение их из тока крови, направленное движение и прилипание (адгезия) к месту повреждения эндотелиальной выстилки (рис. 51). По-видимому, «травма» тромбоцитов способствует высвобождению липопротеидного комплекса периферической зоны пластинок (гиаломер), который обладает агглютинирующими свойства- ми. Агглютинация тромбоцитов завершается их дегрануляцией, высвобожде- нием серотонина и тромбопластического фактора пластинок, что ведет к образованию активного тромбопластина и включению последующих фаз свертывания крови. Коагуляция фибриногена и образование фибрина (см. рис. 51) связаны с ферментативной реакцией (тромбопластина тромбин-> -> фибриноген-> фибрин), причем матрицей для фибрина становится «оголен- ная» центральная зона пластинок (грануломер), которая содержит фермент с ретрактильными свойствами ретрактозим пластинок). Активность ретрактозима, как и серотонина, высвобождающегося при рас- паде пластинок и обладающего сосудосуживающими свойствами, позволяет «отжать» фибринный сверток, который захватывает лейкоциты, агглю- тинирующиеся эритроциты и преципитирующие белки плазмы крови (см. рис. 51). Морфология тромба. Тромб обычно прикреплен к стенке сосуда в месте ее повреждения, где начался процесс тромбообразования. Поверхность его го- фрированная (рис. 52), что отражает ритмичное выпадение склеивающихся тромбоцитов и следующее за их распадом отложение нитей фибрина при про- должающемся кровотоке. Тромб, как правило, плотной консистенции, сухой. Размеры тромба различны — от определяемых лишь при микроскопическом исследовании до выполняющих полости сердца или просвет крупного сосуда на значительном протяжении. Тромб обычно построен из ветвящихся балок склеившихся тромбоцитов и находящихся между ними пучков фибрина с эри- троцитами и лейкоцитами (см. рис. 51). В зависимости от строения и внешнего вида, что опре- деляется особенностями и темпами тромбообразования, различают белые, красные, смешанные (слоистые) и гиалиновые тромбы. Белый тромб состоит из тромбоцитов, фибрина и лейкоцитов (см. рис. 52), образуется медленно при быстром токе крови (чаще в артериях). Красный тромб, помимо тромбоцитов и фибрина, содержит большое число эритроцитов (см. рис. 52), образуется быстро при медленном токе кро- ви (обычно в венах). В наиболее часто встречающемся смешанном тром- бе (см. рис. 52), который имеет слоистое строение (слоистый тромб) и пестрый вид, содержатся элементы как белого, так и красного тромба. В смешанном тромбе различают головку (имеет строение белого тромба), тело (собственно смешанный тромб) и хвост (имеет строение красного тромба). Головка прикреплена к эндотелиальной выстилке сосуда, что отли- чает тромб от посмертного сгустка крови. Слоистые тромбы образуются ча- ще в венах, в полости аневризмы аорты и сердца. Гиалиновый тромб- особый вид тромбов. Он редко содержит фибрин, состоит из разрушенных эритроцитов, тромбоцитов и преципитирующих белков плазмы; при этом тромботические массы напоминают гиалин (рис. 53). Такие тромбы встре- чаются в сосудах микроциркуляторного русла. Тромб может быть п р и стен о ч н ы м, т. е. оставлять часть просвета сво- бодным (см. рис. 52), или закупоривающим, т. е. обтурировать просвет 96 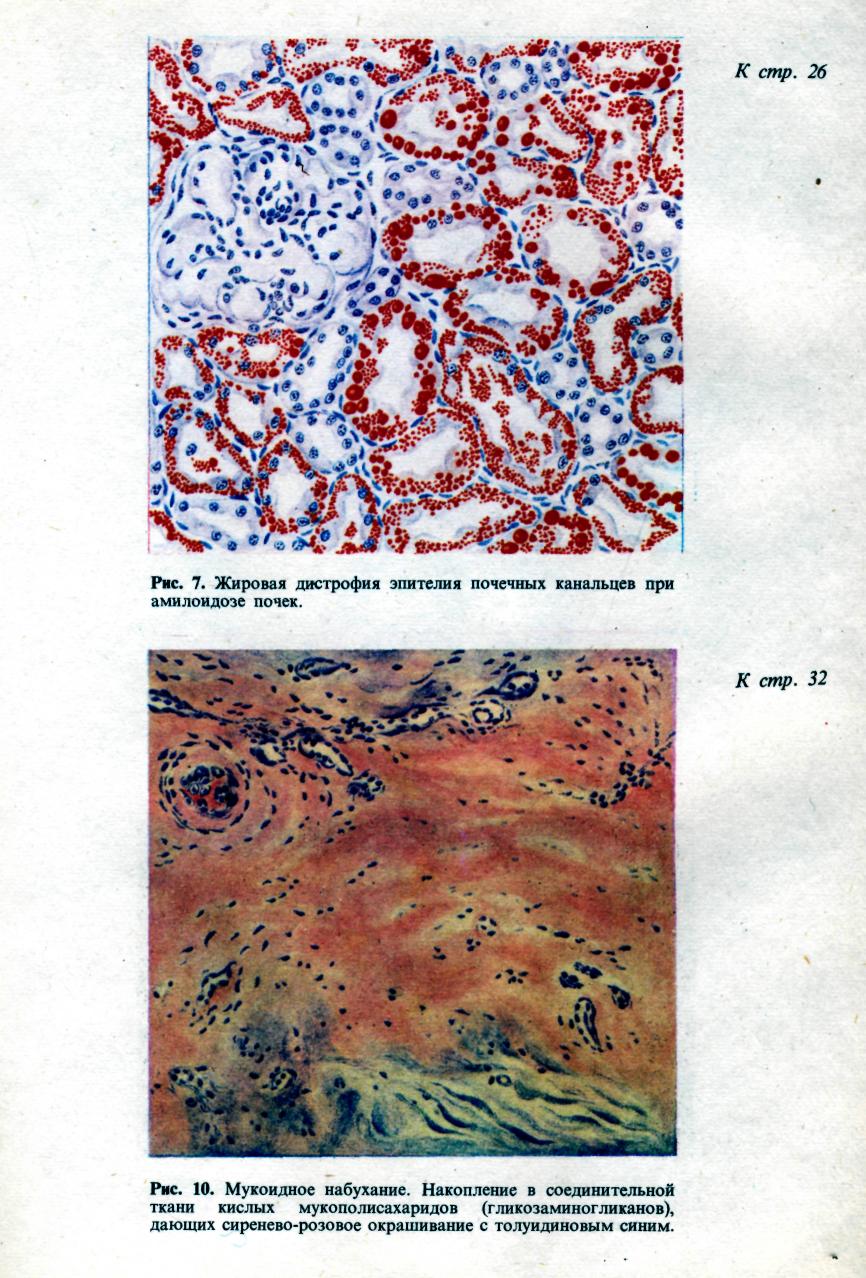 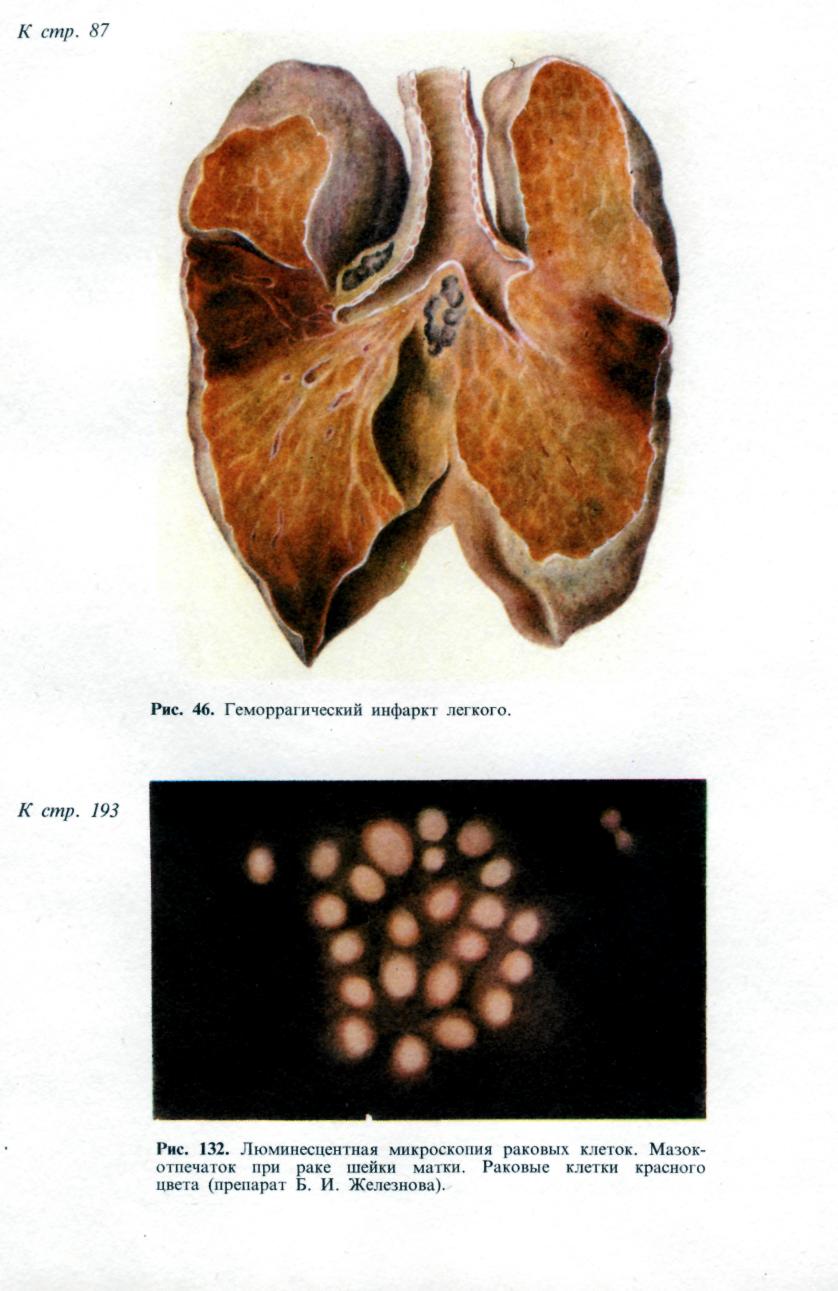 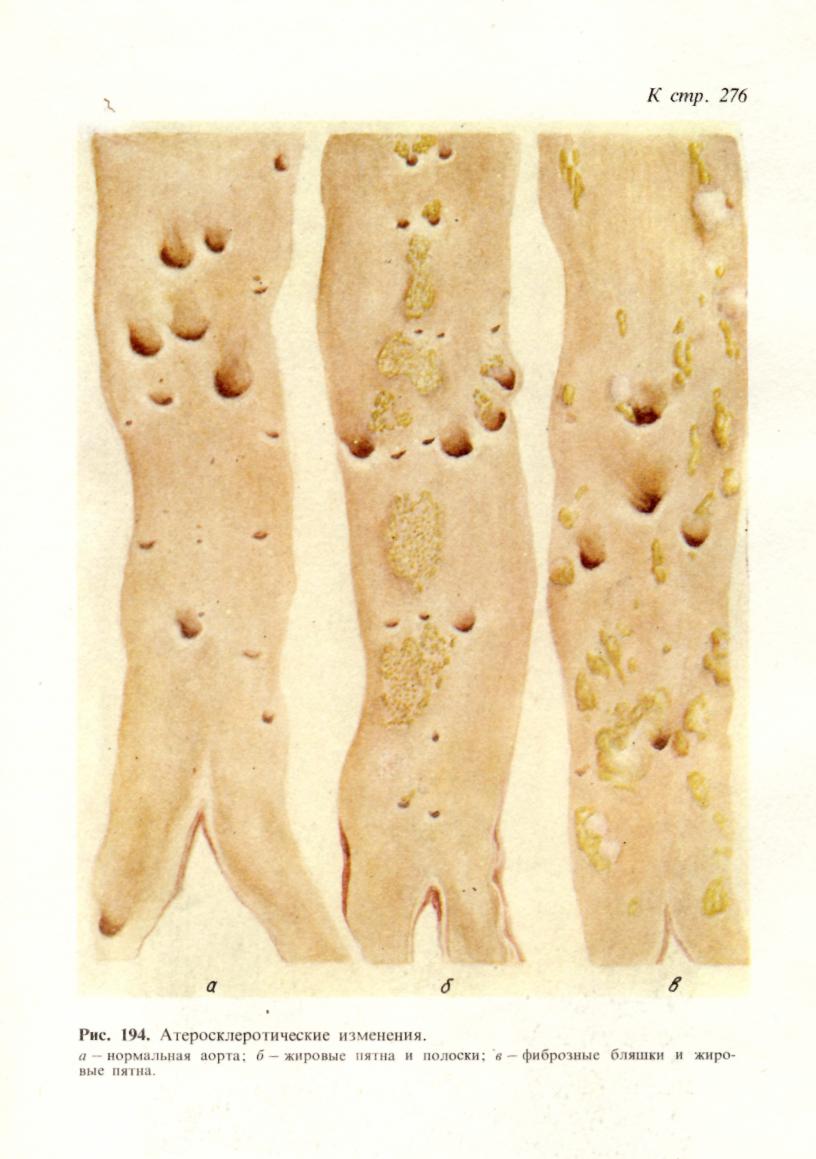 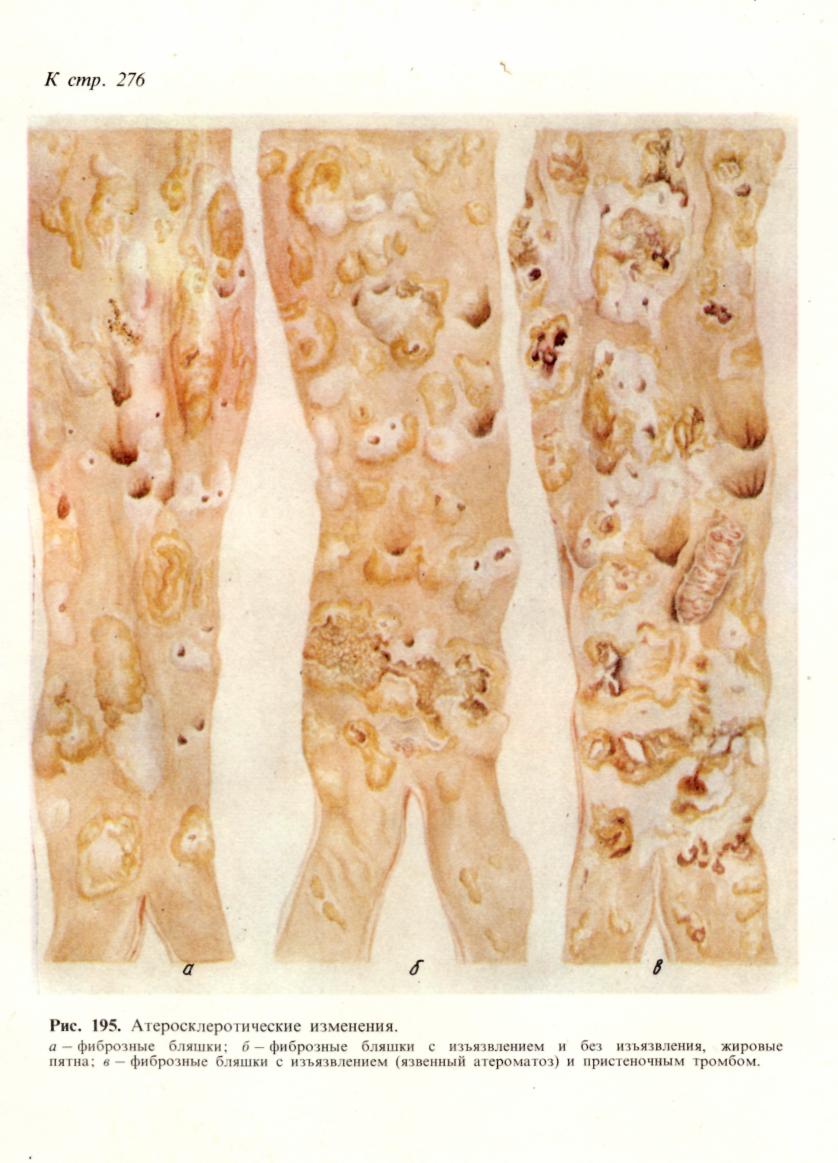 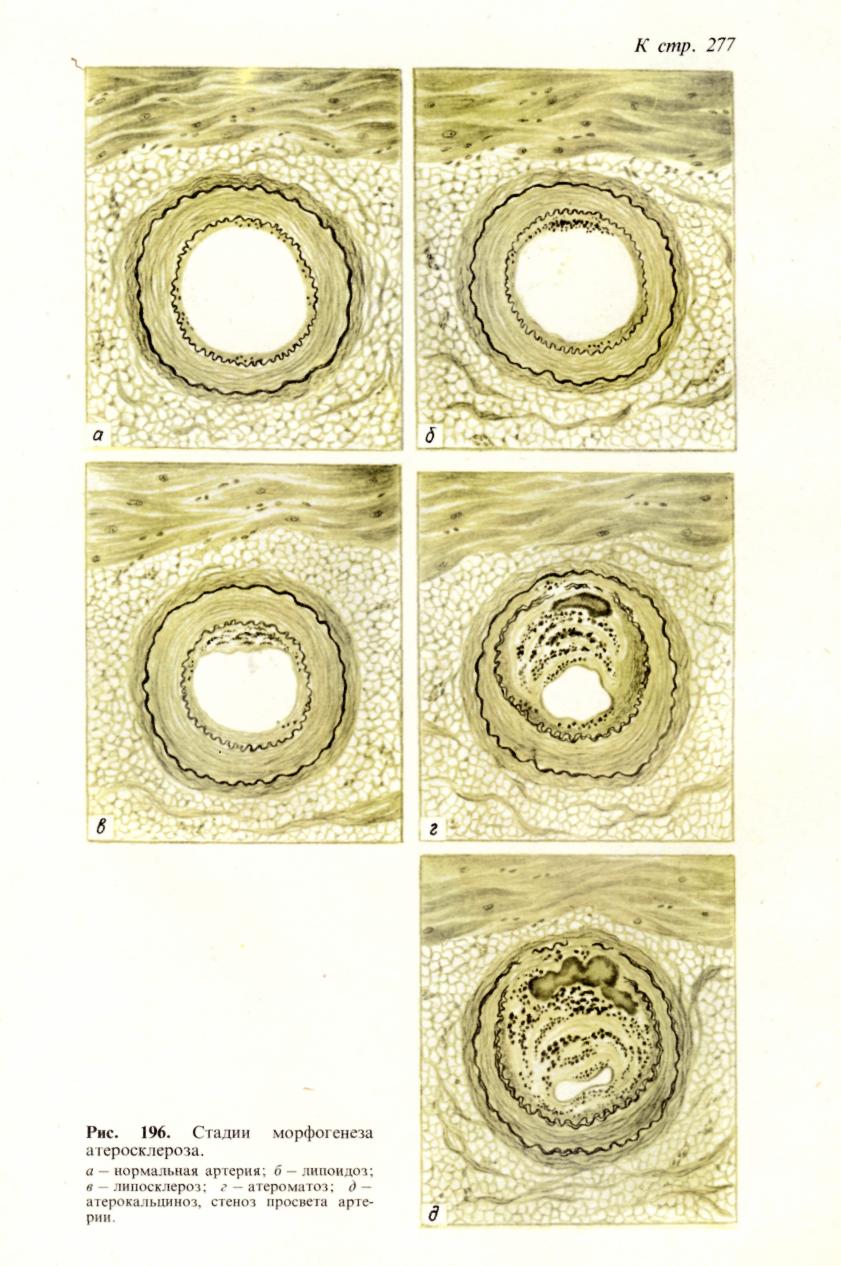    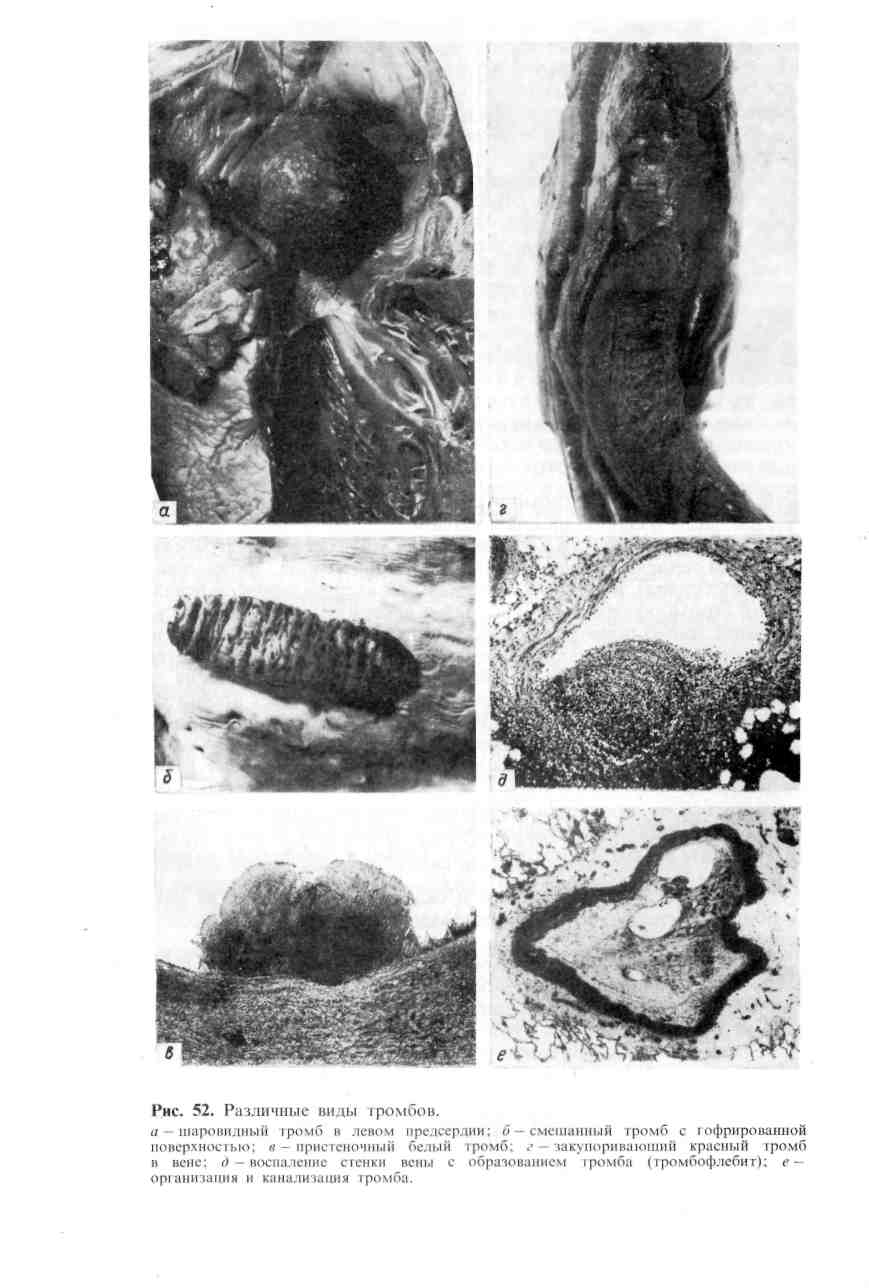 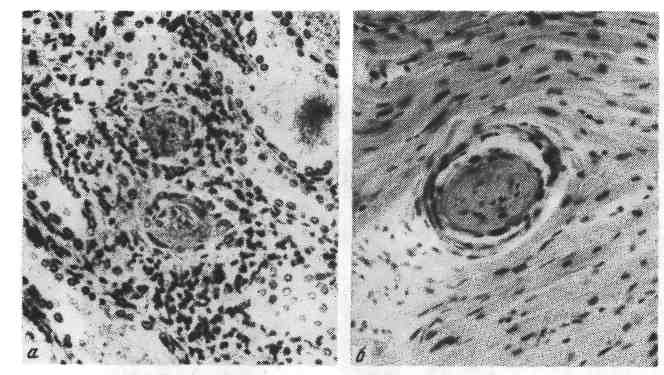 Рис. 53. Гиалиновый тромб. а —в артериолах почки; б —в мелкой ветви венечной артерии сердца. (обтурирующий тромб — см. рис. 52). Пристеночный тромб обнаружи- вается часто в сердце на клапанном или париетальном эндокарде при его во- спалении (тромбоэндокардит), в ушках и между траОекулами при хро- нической сердечной недостаточности (порок сердца, хроническая ишемическая болезнь сердца), в крупных артериях при атеросклерозе, в венах при их воспа- лении (тромбофлебит, см. рис. 52), в аневризмах сердца и сосудов. Закупори- вающий тромб образуется чаще в мелких артериях и венах при росте присте- ночного. Нередко он заполняет просвет аорты, крупной артерии или вены. Увеличение размеров тромба происходит путем наслоения тромботических масс на первичный тромб, причем рост тромба может происходить как по то- ку, так и против тока крови. Иногда тромб, который начал образовываться в венах, например голени, быстро растет по току крови, достигая собира- тельных венозных сосудов, например нижней полой вены. Такой тромбоз на- зывают прогрессирующим. Растущий тромб левого предсердия может отрываться от эндокарда. Находясь свободно в полости предсердия, он «от- шлифовывается» движениями крови и принимает шаровидную форму — ша- ровидны йтромб (см. рис. 52). Тромб в аневризмах называют д и л а т а - ционным. |
