Струков Патологическая анатомия. Литература для студентов медицинских институтов А. И. Струков В. В. Серов Патологическая анатомия Издание второе
 Скачать 16.97 Mb. Скачать 16.97 Mb.
|
|
Из осложнений наиболее часты и грозны тромбоэмболические, которые могут быть первыми проявлениями миокардита. Смерть наступает от сердечной недостаточности или тромбоэмболических осложнений. ПОРОКИ СЕРДЦА Пороки сердца (vicia cordis) — стойкие отклонения в строении сердца, нарушающие его функцию. Различают приобретенные и врожденные пороки сердца. ПРИОБРЕТЕННЫЕ ПОРОКИ СЕРДЦА Приобретенные пороки сердца характеризуются поражением клапанного аппарата сердца и магистральных сосудов и возникают в результате з а б о л е в а н и й сердца после рождения. 270 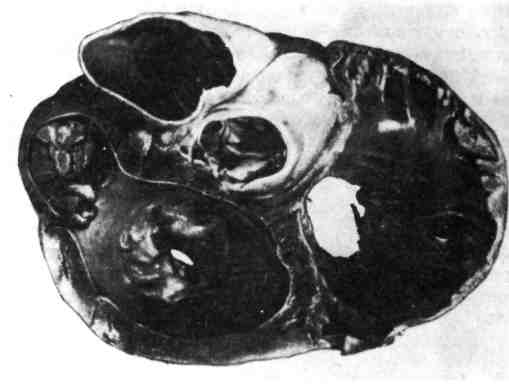 Рис. 192. Резко выраженный сте- ноз левого венозного (митраль- ного) отверстия (вид сверху).. Среди этих заболеваний большее значение имеет ревматизм, меньшее — атеросклероз, си- филис, бактериаль- ный эндокардит, бруцеллез, а также травма. Приобретенные поро- ки сердца — хронические заболевания, в редких слу- чаях, например, при разру- шении створок клапана вследствие язвенного эн- докардита возникают остро. Механизм формирования приобретенного порока сердца тесно связан с эво- люцией эндокардита, завершающейся организацией тромботических масс, рубцеванием, петрификацией и деформацией клапанов и фиброзных ко- лец. Прогрессированию склеротических изменений способствуют возникаю- щие при формировании порока нарушения гемодинамики. Патологическая анатомия. Склеротическая деформация клапанного аппара- та приводит к недостаточности клапанов, которые не в состоянии плотно смыкаться в период их закрытия, или сужению (стенозу) пред- сердно-желудочковых отверстий или устий магистральных сосудов. При комбинации недостаточности клапанов и стеноза отверстия говорят о ком- бинированном пороке сердца. Возможно поражение клапана (изолированный порок) или клапанов сердца (сочетанный по- рок). Наиболее часто развивается порок митрального клапана, или митральный порок, возникающий обычно при ревматизме и очень редко при атеросклерозе. Различают недостаточность митрального клапана, стеноз левого предсердно-желудочкового (митрального) отверстия и их ком- бинацию (митральную болезнь). Чистые формы недостаточности встречаются редко, чистые формы стеноза — несколько чаще. В большинстве случаев отме- чается их комбинация с преобладанием той или иной разновидности порока, которая в конечном итоге оканчивается стенозом отверстия. Прогрессирова- ние склероза, а следовательно, и порока обусловлено чаще всего повторными атаками ревматизма (эндокардита), а также гиперпластическими изменениями клапана, возникающими в связи с непрерывной травматизацией измененного клапана током крови. В результате этого в створках митрального клапана по- являются сосуды, затем соединительная ткань створок уплотняется, они пре- вращаются в рубцовые, иногда обызвествленные, сросшиеся образования. От- мечаются склероз и петрификация фиброзного кольца. Хорды также склерозируются, становятся толстыми и укороченными. При преоблада- нии недостаточности митрального клапана вследствие обратного то- ка крови (регургитации) при диастоле левое сердце переполняется кровью, развивается компенсаторная гипертрофия стенки левого желудочка. Сужение отверстия митрального клапана чаще развивается на уровне фиброзного кольца, и отверстие имеет вид узкой щели, напоминающей «пуго- вичную петлю», реже отверстие клапана имеет вид «рыбьей пасти» (рис. 192). 271  Рис. 193. Аортальный порок сердца. Утол- щение, склероз и сращение заслонок; гипер- трофия стенки левого желудочка. Сужение митрального отверстия может достигать такой степени, что оно едва пропускает браншу пин- цета. При преобладании стеноза воз- никает затруднение тока крови в малом круге кровообращения, левое предсердие расширяется, стенка его утолщается, эндокард склерозиру- ется, становится белесоватым. В ре- зультате гипертонии в малом кру- ге стенки правого желудочка под- вергаются резкой гипертрофии (утолщаются до 1 — 2 см), полость- желудочка расширяется. Порок аортальных кла- панов занимает по частоте вто- рое место после митрального и обычно возникает на почве ревма- тизма, реже — атеросклероза, септи- ческого эндокардита, бруцеллеза, си- филиса. При ревматизме склероз полулунных заслонок и порок клапанов развиваются в связи с теми же процессами, которые формируют мит- ральный порок. Заслонки срастаются между собой, утолщаются, в склерози- рованные заслонки откладывается известь (рис. 193), что приводит в одних случаях к преобладанию недостаточности клапанов, а в других — к сте- нозу аортального отверстия. При атеросклерозе обызвествление и склероз заслонок сочетаются с липоидозом и липосклерозом, причем измене- ния больше выражены на поверхности заслонок, обращенной к синусам. При септическом эндокардите и бруцеллезе наблюдаются резкая дест- рукция (узуры, перфоративные отверстия, аневризмы) заслонок и дефор- мация их в связи с выраженной петрификацией. Сифилитический аор- тальный порок сочетается обычно с мезаортитом; в связи с расшире- нием аорты в этих случаях преобладает недостаточность клапанов. Сердце при аортальных пороках подвергается значительной рабочей ги- пертрофии, главным образом за счет левого желудочка (см. рис. 193). При недостаточности аортальных клапанов масса сердца может достигать 700 — 900 г — возникает так называемое бычье сердце (cor bovinum). Эндокард левого желудочка утолщен, склерозирован. В результате нарушений гемо- динамики ниже клапанного отверстия иногда возникают образования, напо- минающие полулунныё заслонки («дополнительные клапаны»). 1 Приобретенные пороки трехстворчатого клапана и клапа- нов легочной артерии возникают редко на почве ревматизма, сифи- лиса, сепсиса, атеросклероза. Возможны как недостаточность клапанов, так и стеноз отверстия. Помимо изолированных, часто наблюдаются сочетанные пороки: митрально-аортальный, митрально-трикуспидальный, митрально-аортально- трикуспидальный. Многие сочетанные пороки являются и комбинирован- ными. Приобретенный порок сердца может быть компенсированным и декомпенсированным. 272 Компенсированный порок сердца протекает без расстройств кро- вообращения, нередко длительно и латентно. Компенсация осуществляется за счет гипертрофии тех отделов сердца, на которые падает усиленная нагрузка в связи с пороком. Возникает концентрическая гипертрофия миокарда. Одна- ко гипертрофия имеет свои пределы, и на определенном этапе ее развития в миокарде появляются дистрофические изменения, которые ведут к ослабле- нию работы сердца. Концентрическая гипертрофия сменяется эксцентрической вследствие наступившей миогенной дилатации полостей сердца. Декомпенсированный порок сердца характеризуется расстрой- ством сердечной деятельности, ведущей к сердечно-сосудистой недостаточно- сти. Причиной декомпенсации могут быть обострение ревматического процес- са, случайная инфекция, чрезмерная физическая нагрузка, психическая травма. Сердце становится дряблым, полости расширяются, в ушках его образуются тромбы. Обнаруживается белковая и жировая дистрофии мышечных волокон, в строме появляются очажки воспалительной инфильтрации. В органах возни- кает венозный застой, появляются цианоз, отеки, водянка полостей. Сердеч- но-сосудистая недостаточность становится частой причиной смерти больных, страдающих пороком сердца. Реже смерть наступает внезапно от тромбоэмболии, закупорки суженного митрального отверстия шаровидным тромбом, паралича гипертрофированного сердца, пневмонии. ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА Врожденные пороки сердца возникают в результате нарушения формирования сердца и отходящих от него сосудов (см. «Болезни детского возраста»). КАРДИОСКЛЕРОЗ Кардиосклероз — разрастание соединительной ткани в сердечной мы- шце. Как правило, это — вторичный процесс. Патологическая анатомия. Различают очаговый и диффузный кардиоскле- роз. При очаговом кардиосклерозе в мышце сердца образуются различной величины белесоватые тяжистые участки (рубцы). Такие рубцы обычно образуются при организации инфарктов миокарда. Они пронизывают иногда толщу мышцы сердца и представляют собой обширные поля (крупцооча- говый кардиосклероз), на месте которых нередко формируется хро- ническая аневризма (от греч. aneuryno — расширять) сердца. По периферии таких рубцов миокард утолщен (регенерационная гипертрофия). Доволь- но часто развивается мелкоочаговый кардиосклероз, предста- вленный белесоватыми периваскулярными очажками и полосками, которые равномерно разбросаны в мышце сердца. Он возникает в результате разраста- ния соединительной ткани в участках дистрофии, атрофии и гибели отдельных мышечных клеток в связи с гипоксией. Диффузный кардиосклероз, или миофиброз, характеризует- ся диффузным утолщением и огрубением стромы миокарда за счет новообра- зования в ней соединительной ткани. Соединительная ткань в таких случаях оплетает, как бы замуровывает атрофирующиеся мышечные волокна. Морфогенез. Различают три вида кардиосклероза: постинфарктный, за- местительный и миокардитический. Постинфарктный кардиоскле- роз обычно бывает крупноочаговым, замести т е льны й — мелкооча- говым, миокардитический — диффузным (миофиброз). 273 Клиническое значение. С кардиосклерозом связано нарушение сократитель- ной функции миокарда, проявляющееся в сердечной недостаточности и нару- шениях ритма сердца. Крупноочаговый постинфарктный кардиосклероз слу- жит основой развития хронической аневризмы сердца. АТЕРОСКЛЕРОЗ Атеросклероз (от греч. athere — кашица и sklerosis — уплотнение) — хроническое заболевание, возникающее в результате нарушения жирового и белкового обмена, характеризующееся поражением артерий эластиче- ского и мышечно-эластического типа в виде очагового отложения в ин- тиме липидов и белков и реактивного разрастания соединительной ткани. Атеросклероз широко распространен среди населения экономически развитых стран Европы и Северной Америки, в странах Африки и Азии он встречается реже. Болеют обычно люди во второй половине жизни. Проявле- ния и осложнения атеросклероза являются наиболее частыми причинами смертности и инвалидности в большинстве стран мира. Следует отличать атеросклероз от артериосклероза, которым обозначают склероз ар- терий вне зависимости от причины и механизма его развития. Атеросклероз является лишь разновидностью артериосклероза, отражающей нарушения метаболизма липидов и белков («метаболический артериосклероз»). В таком толковании термин «атеросклероз» был введен в 1904 г. Маршаном и обоснован экспериментальными исследованиями Н. Н. Анич- кова. Поэтому атеросклероз называют болезнью Маршана — Аничкова. В зависимости от этиологических, патогенетических и морфологических признаков разли- чают следующие виды артериосклероза: 1) атеросклероз («метаболический артериос- клероз»); 2) артериолосклероз, или гиалиноз (например, при гипертонической болезни); 3) во- спалительный артериосклероз (например, сифилитический, туберкулезный); 4) аллергический артериосклероз (например при узелковом периартериите); 5) токсический артериосклероз (на- пример, адреналиновый); 6) первичный кальциноз средней оболочки артерий (медиакальциноз Менкеберга); 7) возрастной (старческий) артериосклероз. Этиология и патогенез. В развитии атеросклероза наибольшее значение имеют следующие факторы: 1) обменные факторы; 2) гормональные фак- торы; 3) артериальная гипертония; 4) стрессовые и конфликтные ситуации, ве- дущие к психоэмоциональному перенапряжению; 5) состояние сосудистой стенки; 6) наследственные и этнические факторы. Среди обменных факторов основное значение имеют нарушения жирового и белкового обмена. Гиперлипемии (гиперхолестеринемии) придается чуть ли не ведущая роль в этиологии атеросклероза. Это доказано экспериментальными исследованиями. Скармливание животным холестерина приводит к гиперхоле- стеринемии, отложению холестерина и его эфиров в стенке аорты и артерий, развитию атеросклеротических изменений. У больных атеросклерозом людей также нередко отмечаются гиперхолестеринемия, ожирение. Эти данные по- зволяли ранее считать, что в развитии атеросклероза исключительное значе- ние имеет алиментарный фактор (алиментарная инфиль- трационная теория атеросклероза Н. Н. Аничкова). Однако в дальнейшем было доказано, что избыток экзогенного холестерина у челове- ка во многих случаях не приводит к развитию атеросклероза, корреляция между гиперхолестеринемией и выраженностью морфологических изменений, свойственных атеросклерозу, отсутствует. В настоящее время в развитии атеросклероза придается значение не столь- ко самой гиперхолестеринемии, сколько нарушению соотношений холесте- рина с фосфолипидами (нарушение холестеринолецитинового коэффициента) и белками (избыточное образование В-липопротеидов). Подчеркивается важ- ное значение жиробелкоаых комплексов — В-липопротеидов, которые могут выступать в роли атерогенных веществ и аутоантигенов. 274 Доказательство антигенных свойств В-липопротеидов явилось основанием для создания иммунологической теории атеросклероза. Со- гласно этой теории, при атеросклерозе образуются иммунные комплексы В- липопротеид — аутоантитело, которые, циркулируя в крови, откладываются в интиме артерий, что ведет к развитию характерных изменений. О значении в развитии атеросклероза нарушений не только липидного, но и белкового обмена свидетельствует частое возникновение атеросклероза при подагре, желчнокаменной болезни. Значение гормональных факторов в развитии атеросклероза не- сомненно. Так, сахарный диабет и гипотиреоз способствуют, а гипертиреоз и эстрогены препятствуют развитию атеросклероза. Несомненна и роль а р - териальной гипертонии в атерогенезе. Вне зависимости от характера гипертонии при ней отмечается усиление атеросклеротического процесса. При гипертонии атеросклероз развивается даже в венах (в легочных венах — при гипертензии малого круга, в воротной вене — при портальной гипертензии). Эти данные свидетельствуют о значении гемодинамического фак- тора в патогенезе атеросклероза. Исключительная роль в этиологии атеро- склероза отводится стрессовым и конфликтным ситуациям, т. е. нервному фактору. С этими ситуациями связано психоэмо- циональное перенапряжение, ведущее к нарушению нейроэндо- кринной регуляции жиробелкового обмена и вазомоторным расстройствам, что определяет развитие атеросклеротических изменений (нервно-мета- болическая теория атеросклероза А. Л. Мясникова). Поэтому атеросклероз рассматривается как болезнь урбанизации, болезнь сапиентации. Атеросклероз — заболевание жителей города, а не деревни, работников в основном умственного (интеллектуального), а не физического труда. Состояние сосудистой стенки в значительной мере определяет развитие атеросклероза. Имеют значение заболевания (инфекции, интоксика- ции, артериальная гипертония), ведущие к поражению стенки артерий (арте- риит, плазматическое пропитывание, тромбоз, склероз), что «облегчает» воз- никновение атеросклеротических изменений. Избирательное значение при этом имеют пристеночные и интрамуральные тромбы, на которых «строится» атеросклеротическая бляшка (тромбогенная теория Рокитанского — Дьюгеда). Некоторые исследователи придают основное значение в развитии атеро- склероза возрастным изменениям артериальной стенки и рассматривают атеросклероз как «проблему возраста», как «геронтологиче- скую проблему» (И. В. Давыдовский); нозологическая сущность атеросклеро- за отвергается. Эта концепция не разделяется большинством патологов. Роль наследственных факторов в атеросклерозе доказана (на- пример, атеросклероз у молодых людей при семейной гиперхолестеринемии), но изучена недостаточно. Имеются данные о роли этнических факто- ров в его развитии. Таким образом, атеросклероз следует считать полиэтиологическим заболеванием, возникновение и развитие которого связаны с влиянием экзогенных и эндогенных факторов. Патологическая анатомия и морфогенез. Сущность процесса хорошо отра- жает терминов интиме артерий появляются кашицеобразный жиро-белковый детрит (athere) и очаговое разрастание соединительной ткани (sclerosis), что приводит к формированию атеросклеротиче- ской бляшки, суживающей просвет сосуда. Обычно поражаются, как уже упоминалось, артерии эластического и мышечно-эластического типа, т. е. ар- терии крупного и среднего калибра; значительно реже в процесс вовлекаются мелкие артерии мышечного типа. 275 Атеросклеротический процесс проходит определенные стадии (фаз ы), которые имеют макроскопическую и микроскопическую характеристику (морфогенез атеросклероза). При макроскопическом исследовании различают следующие виды атеро- склеротических изменений, отражающие динамику процесса (рис. 194, 195, см. на цветн. вкл.): 1) жировые пятна или полоски; 2) фиброзные бляшки; 3) ос- ложненные поражения, представленные фиброзными бляшками с изъязвле- нием, кровоизлияниями и наложениями тромботических масс; 4) кальциноз, или атерокальциноз. Жировые пятна или полоски — это участки желтого или желто-се- рого цвета (пятна), которые иногда сливаются и образуют полоски, но не воз- вышаются над поверхностью интимы. Они содержат липиды, выявляемые при тотальной окраске сосуда красителями на жиры, например Суданом. Раньше всего жировые пятна и полоски появляются в аорте на задней стенке и у места отхождения ее ветвей, позже — в крупных артериях. У 50 % детей в возрасте моложе 1 года можно обнаружить в аорте ли- пидные пятна. В юношеском возрасте липидоз усиливается, жировые пятна появляются не только в аорте, но и в венечных артериях сердца. С возрастом изменения, характерные для физиологического раннего липидоза, в подав- ляющем большинстве случаев исчезают и не являются источником развития дальнейших атеросклеротических изменений. Фиброзные бляшки — плотные, овальные или круглые, белые или бело-желтые образования, содержащие липиды и возвышающиеся над поверхностью интимы. Часто они сливаются между собой, придают вну- тренней поверхности сосуда бугристый вид и резко суживают его просвет (стенозирующий атеросклероз). Наиболее часто фиброзные бляш- ки наблюдаются в брюшной аорте, в отходящих от аорты ветвях, в артериях сердца, мозга, почек, нижних конечностей, сонных артериях и др. Чаще пора- жаются те участки сосудов, которые испытывают гемодинамическое (меха- ническое) воздействие (в областях ветвления и изгибов артерий, на стороне их стенки, которая имеет жесткую подстилку). Осложненные поражения возникают в тех случаях, когда в толще бляшки преобладает распад жиро-белковых комплексов и образуется детрит, напоминающий содержимое ретенционной кисты сальной железы, т. е. ате- ромы. Поэтому такие изменения называют атероматозными. Про- грессирование атероматозных изменений ведет к деструкции покрышки бляшки, ее изъязвлению (атероматозная язва), кровоизлияниям в толщу бляшки (интрамуральная гематома) и образованию тромботических наложений на месте изъязвления бляшки. С ос- ложненными поражениями связаны: острая закупорка артерии тромбом и развитие инфаркта, эмболия как тромботическими, так и атероматозными массами, образование аневризмы сосуда в месте его изъязвления, а также артериальное кровотечение при разъедании стенки сосуда атероматозной язвой. Кальциноз, или атерокальциноз, — завершающая фаза атеро- склероза, которая характеризуется отложением в фиброзные бляшки солей кальция, т. е. их обызвествлением. Бляшки приобретают каменистую плотность (петрификация бляшек), стенка сосуда в месте петрифика- ции резко деформируется. Различные виды атеросклеротических изменений нередко сочетаются; в одном и том же сосуде, например в аорте, можно видеть одновременно жи- ровые пятна и полосы, фиброзные бляшки, атероматозные язвы с тромбами и участки атерокальциноза, что свидетельствует о волнообразности течения атеросклероза. 276 Микроскопическое исследование позволяет уточнить и дополнить характер и последовательность развития изменений, свойственных атеросклерозу. На основании его результатов выделены следующие стадии морфогенеза атеросклероза (рис. 196, см. на цветн. вкл.): 1) долипидная; 2) липидоз; 3) липосклероз; 4) атероматоз; 5) изъязвление; 6) атерокальциноз. В изучении морфогенеза, патогенеза и этиологии атеросклероза огромное значение имело создание его экспериментальной холестерино- вой модели. Впервые модель атеросклероза была создана отечественными учеными — патологоанатомом Н. Н. Аничковым и патофизиологом С. С. Халатовым на кроликах при скармливании им холе- стерина. В дальнейшем подобная модель воспроизведена на курах, свиньях, собаках, обезьянах и других животных. При кормлении животных холестерином удалось выявить в стенке артерий изменения, весьма близкие (но не тождественные) атеросклерозу человека, проследить их дина- мику, изучить факторы, ускоряющие и замедляющие развитие атеросклероза, а также способ- ствующие регрессии атеросклеротических изменений. Эти исследования явились основой для разработки рациональной терапии атеросклероза. Долипидная стадия характеризуется изменениями, отражающими общие нарушения метаболизма при атеросклерозе (гиперхолестеринемия, на- копление грубодисперсных белков и мукоидных веществ в плазме крови, по- вышение активности гиалуронидазы и т. д.) и «травму» интимы продуктами нарушенного метаболизма. К этим изменениям относятся: 1) повышение проницаемости эндотелия и мембран интимы, что ведет к накоплению во внутренней оболочке белков плазмы, фибриногена (фибрина) и образованию плоских пристеночных тромбов; 2) накопление кислых гликозаминогликанов (в основном сульфатированных мукополисаха- ридов) в интиме, с чем связано появление мукоидного отека внутрен- ней оболочки, а поэтому благоприятных условий для фиксации в ней В-липо- протеидов, холестерина, белков; 3) деструкцией эндотелия, о а - зальных мембран интимы, эластических и коллаге- нов ых волокон, способствующей еще большему повышению проницае- мости интимы для продуктов нарушенного обмена и пролиферации гладкомышечных клеток. Не исключено, что такие вещества, как хондроитин- сульфаты и холестерин, откладываются в интиме вследствие травмы эласти- ческих структур. Ряд веществ нарушенного обмена, в частности липиды, холестерин и фибрин, хорошо вы- являются в эндотелии и за базальной его мембраной при электронно-микроскопическом иссле- довании (рис. 197). Из этого следует, что понятие «долипидная стадия» уточняется результатами электронно-микроскопического анализа начальных изменений интимы при атеросклерозе. Сущ- ность этих изменений заключается в адаптивной реакции интимы на первичные гуморально-ме- таболические и нервно-сосудистые нарушения (В. X. Анестиади). Продолжительность долипидной стадии определяется возможностью ли- политических и протеолитических (фибринолитических) ферментов интимы «очищать» ее от «засорения» продуктами нарушенного метаболизма. Как правило, активность этих ферментов интимы в долипидной стадии повышена, истощение их знаменует начало стадии липидоза. В стадии липидоза отмечается очаговая инфильтрация интимны, особен- но поверхностных ее отделов, липидами (холестерином), В-липопротеидами, белками (рис. 198), что ведет к образованию жировых пятен и полос. Липиды диффузно пропитывают интиму и накапливаются в макро- фагах, которые получили название ксантомных клеток (от греч. xant- hos — желтый). Роль этих клеток выполняют гладкомышечные клетки. В эн- дотелии также появляются липидные включения, что свидетельствует об инфильтрации интимы липидами плазмы крови. Отчетливо выражены набуха- ние и деструкция эластических мембран. 277   Рис. 197. Атеросклероз, долипидные изменения интимы аорты. В эндотелиальной клетке увеличивается зона комплекса Гольджи (АГ), более выражена эндо- плазматическая сеть (ЭС), в которой появляется плотный материал — липиды (Л); базальная мембрана (БМ) несколько разрыхлена; за базальной мембраной среди коллагеновых (K.лB) и эластических (ЭВ) волокон фибриллярные отложения (Фл) белков и липидов (77). Я-ядро, х 23 000 (по Гиру). Рис. 198. Липоидоз. Во внутренних отделах интимы скопления липидов (черного цвета). Липосклероз характеризуется разрастанием молодых соединительно- тканных элементов интимы в участках отложения и распада липидов и бел- ков, появлением большого числа макрофагов — ксантомных клеток, разруше- нием эластических и аргирофильных мембран. Очаговое разрастание в интиме молодой соединительной ткани и ее последующее созревание ведут к форми- рованию фиброзной бляшки (рис. 199), в которой появляются тонко- стенные сосуды, связанные с vasa vasorum. Существует точка зрения, что формирование фиброзной бляшки связано с пролиферацией гладкомышечных клеток, возникающей в ответ на поврежде- ние эндотелия и эластических волокон артерий. При атероматозе липидные массы, составляющие центральную часть бляшки, а также прилежащие коллагеновые и эластические волокна распа- даются (рис. 200). При этом образуется мелкозернистая аморфная масса, в которой обнаруживаются кристаллы холестерина и жирных кислот, обрыв- ки эластических и коллагеновых волокон, капельки нейтральных жиров (ате- роматозный детрит). В краях у основания бляшки появляется много новообразованных сосудов, врастающих из vasa vasorum, а также ксантомные клетки, лимфоциты, плазматические клетки. Атероматозньте массы отграни- чены от просвета сосуда слоем зрелой, иногда гиалиниаированной соедини- тельной ткани (покрышка бляшки). В связи с тем что атероматозному распаду подвергаются гладкие мышечные волокна средней оболочки, бляшка «погружается» довольно глубоко, достигая в некоторых случаях адвентиции. Атероматоз —начало осложненных п о р а ж е н и й. При прогрес- 278   Рис. 199. Липосклероз. Просвет венечной артерии сердца сужен фиброзной бляшкой. |
