Струков Патологическая анатомия. Литература для студентов медицинских институтов А. И. Струков В. В. Серов Патологическая анатомия Издание второе
 Скачать 16.97 Mb. Скачать 16.97 Mb.
|
|
Патологическая анатомия. Попадая в стенку толстой кишки, амеба и про- дукты ее жизнедеятельности вызывают отек и гистолиз, некроз слизистой оболочки, образование язв. Участки некроза слизистой оболочки не- сколько выбухают над ее поверхностью, они окрашены в грязно-серый или зе- леноватый цвет. На разрезе видно, что зона некроза проникает глубоко в под- слизистый и мышечный слои. При образовании язвы края ее становятся подрытыми и нависают над дном. По мере прогрессирования некроза раз- меры язвы увеличиваются. Амебы находят на границе между омертвевшими и сохранившимися тканями. Характерно, что клеточная реакция в стенке киш- ки выражена слабо. Однако по мере присоединения вторичной инфекции воз- 508 никает лейкоцитарная реакция, появляется гной. Иногда развивается флегмо- нозная и гангренозная форма колита. Глубокие язвы заживают рубцом. Некротически-язвенные изменения наиболее часто и резко выражены в слепой кишке (хроническийязвенный колит). Однако нередки случаи, когда язвы образуются на всем протяжении толстой кишки и даже в подвздошной кишке. Регионарные лимфатические узлы несколько увеличены, но амебы в них не обнаруживаются, в кровеносных сосудах стенки кишки амебы обычно нахо- дят. Осложнения амебиаза делят на кишечные и внекишечные. Из кишечных наиболее опасны прободениеязвы, кровотечение, образование стенозирующих рубцов после заживления язв, развитие воспали- тельных инфильтратов вокруг пораженной кишки, которые нередко симулируют опухоль. Из внекишечных осложнений наиболее опасным являет- ся развитие абсцесса печени. БАЛАНТИДИАЗ Балантидиаз характеризуется развитием хронического язвенного ко- лита. Редко отмечается изолированное поражение червеобразного отростка. Этиология. Возбудителем балантидиаза является инфузория Balantidium coli. Патологическая анатомия. Изменения при балантидиазе сходны с таковы- ми при амебиазе, однако при балантидиазе, который встречается значительно реже амебиаза, поражение кишки не столь резко выражено. Вначале наблю- дается поражение поверхностных слоев слизистой оболочки с образованием эрозий. В дальнейшем, по мере проникновения балантидий в подслизистый слой, развиваются язвы, которые имеют разную величину и форму, края их подрыты, на дне видны серо-грязные остатки некротических масс. Баланти- дий обнаруживаются обычно по соседству с очагами некроза, а также в крип- тах и толще слизистой оболочки вдали от язв. Они могут проникать и в мы- шечный слой, в просвет лимфатических и кровеносных сосудов. Местные кле- точные реакции при балантидиазе выражены слабо, среди клеток инфильтрата преобладают эозинофилы. Важнейшее из осложнений балантидиаза — прободение язвы с разви- тием перитонита. Присоединение к язвенному процессу вторичной инфекции может привести к септикопиемии. эхинококке» Эхинококкоз — заболевание человека и животных, вызываемое личи- ночной стадией (финной) эхинококка из класса ленточных червей и семейства цепней. Этиология. Наибольшее значение в патологии человека и животных имеют Echinococcus granulans, вызывающий гидатидозную форму эхинококко- за, и Echinococcus multilocularis, вызывающий альвеолярную форму эхинококкоза, или альвеококкоз. Гидатидозный эхинококкоз встречается чаще, чем альвеококкоз. Эпидемиология и патогенез. В развитии гидатидозного эхинококкоза у че- ловека большая роль принадлежит облигатному хозяину половозрелого лен- точного червя — собаке, у которой паразит обитает в кишечнике. Личинка альвеококка, отличающаяся от личинки гидатидозного эхинококка, обнаружи- вается у грызунов и человека. Человек, вероятно, заражается при обработке шкур грызунов. Альвеококкоз характеризуется определенной географической 509  Рис. 368. Альвеококкоз. Среди некротических масс — пузыри эхинокок- ка, окруженные зоной продуктивного воспале- ния. патологией. В нашей стране он чаще наблюдается в Якутии, Казахстане, очень редко — в Европейской части СССР. Очаги альвеококкоза встречаются также в некоторых странах Европы. Патологическая анатомия. При гидатидозномэхинококкозе в ор- ганах появляются пузырьки (или один пузырь) той или иной величины (от ореха до головы взрослого человека). Они имеют беловатую слоистую хити- новую оболочку и заполнены прозрачной бесцветной жидкостью. В жидкости белок отсутствует, но содержится янтарная кислота. Из внутреннего гермина- тивного слоя оболочки пузыря возникают дочерние пузыри со сколексами. Эти дочерние пузыри заполняют камеру материнского пузыря (однока- мерный эхинококк). Ткань органа, в котором развивается однока- мерный эхинококк, подвергается атрофии. На границе с эхинококком разра- стается соединительная ткань, образуя вокруг пузыря капсулу. В капсуле обнаруживаются сосуды с утолщенными стенками и очаги клеточной инфиль- трации с примесью эозинофилов. В участках капсулы, прилегающей непосред- ственно к хитиновой оболочке, появляются гигантские клетки инородных тел, фагоцитирующие элементы этой оболочки. Чаще эхинококковый пузырь об- наруживается в печени, легких, почках, реже — в других органах. При альвеококкозе онкосферы дают начало развитию сразу несколь- ких пузырьков, причем вокруг них появляются очаги некроза. В пузырьках альвеококкоза образуются выросты цитоплазмы, и рост пузырей происходит путем почкования наружу, а не внутрь материнского пузыря, как это имеет место при однокамерном эхинококке. В результате этого при альвеококкозе образуются все новые и новые пузырьки, проникающие в ткань, что ведет к ее разрушению. Поэтому альвеококк называют также многокамерным эхинококком. Следовательно, рост альвеококка имеет инфильтрирующий характер и подобен росту злокачественного новообразования. Выделяющиеся из пузырьков токсические вещества вызывают в окружающих тканях некроз и продуктивную реакцию. В грануляционной ткани много эозинофилов и ги- гантских клеток инородных тел, фагоцитирующих оболочки погибших пузы- рьков (рис. 368). Первично альвеококк чаще встречается в печени, реже — в других орга- нах. В печени он занимает целую долю, очень плотен (плотность доски), на разрезе имеет пористый вид с прослойками плотной соединительной ткани. В центре узла иногда образуется полость распада. Альвеококк склонен к г е - 510 матогенному и лимфогенному метастазированию. Гемато- генные метастазы альвеококка при первичной локализации его в печени по- являются в л е г к и х, затем ворганахбольшого круга кровообра- щения (почках, головном мозге, сердце и др). В связи с этим клинически альвеококк ведет себя как злокачественная опухоль (рак). Осложнения при эхинококкозе чаще связаны сростомпузыря в печени или метастазами альвеококка. Возможно развитие амилоидоза. ЦИСТИЦЕРКОЗ Цистицеркоз— хронический гельминтоз, который вызывается личиноч- ной стадией (финной) вооруженного (свиного) цепня (солитера). Этиология, эпидемиология, патогенез. Заболевание развивается у людей, а также у некоторых животных (свиней, собак, кошек), являющихся промежу- точными хозяевами паразита и его финнозной стадии. Животные заражаются, поедая каловые массы человека, содержащие яйца гельминта. Человек зара- жается при употреблении в пищу мяса свиней, в котором паразитирует финна (цистицерк). Развитие финны во взрослого паразита происходит в кишечнике человека. При паразитировании свиного солитера в кишечнике у человека может развиться цистицеркоз. Это происходит при попадании яиц солитера в желудок, где их оболочка растворяется, зародыши проникают через стенку желудка в просвет сосудов, переносятся в различные ткани и органы, где и превращаются в цистицерки. Патологическая анатомия. Цистицерк имеет вид пузырька величиной с го- рошину. От его стенки внутрь отходит головка с шейкой. Вокруг цистицерка развивается воспалительная реакция. Инфильтрат состоит из лимфоцитов, плазматических клеток, фибробластов, эозинофилов. Вокруг инфильтрата по- степенно появляется молодая соединительная ткань, которая созревает и образует вокруг цистицерка капсулу. В ткани головного мозга в формирова- нии капсулы вокруг цистицерка принимают участие клетки микроглии. С те- чением времени цистицерк погибает и обызвествляется. Цистицерки обнаруживаются в самых разнообразных органах, но чаще всего в головном мозге, глазе, мышцах, подкожной клетчат- ке. В мягких мозговых оболочках основания головного мозга на- блюдается ветвистый (рацемозный) цистицерк. Наиболее опасен цистицерк головного мозга и глаза. ОПИСТОРХОЗ Описторхоз — заболевание человека и млекопитающих, вызываемое паразитами вида трематод. Первое описание морфологии описторхоза при- надлежит русскому патологоанатому К. Н. Виноградову (1891). Этиология. Для человека наибольшее значение имеет инвазия Opistorchia felineus (двуустка кошачья). Эпидемиология и патогенез. Человек и плотоядные животные, зараженные описторхозом, являются источником инвазии для моллюсков битиний, ко- торые заглатывают яйца паразита, попавшие в воду с фекалиями больных людей и животных. В организме моллюсков размножаются личиночные ста- дии гельминта, что заканчивается выходом в воду церкариев. Они проникают через кожу рыб в их подкожную клетчатку и мышцы, превращаясь здесь в ме- тацеркариев. Заражение описторхозом человека и млекопитающих происходит при употреблении в пищу сырой рыбы с личинками гельминта (метацерка- риями). Оптимальной средой обитания для двуусток становятся желчные пути. 511 Патологическая анатомия. Основные изменения развиваются в желчных путях и паренхиме-печени. Во внутрипеченочных желчных протоках, где находится большое число паразитов, развивается воспаление. Стенки про- токов инфильтрированы лимфоидными элементами, плазматическими клетка- ми, эозинофилами. Эпителий образует реактивные разрастания с формирова- нием железистых структур в подэпителиальном слое^" В исходе развивается склероз стенок протоков и перидуктальный склероз. В^паренхиме печени по- являются участки некроза, которые замещаются разрастающейся соедини- тельной тканью. Склеротические изменения в печени имеют очаговый харак- тер и связаны с преимущественной локализацией паразитов в желчных путях. В стенке желчного пузыря также возникает воспаление. В поджелудочной железе отмечаются расширение протоков, в ко- торых находят скопления гельминтов, гиперплазия слизистой оболочки, во- спалительные инфильтраты в стенке протоков и строме железы. Осложнения связаны с присоединением вторичной инфекции желчных пу- тей, что приводит к развитию гнойного холангита и холангиоли- та, При длительном течении описторхоза возможен цирроз печени. В ре- зультате длительной и извращенной пролиферации эпителия желчных путей иногда развивается холангиоцеллюлярный рак печени. шистосомоз Шистосомоз — хронический гельминтоз с преимущественным пораже- нием мочеполовой системы и кишечника. Этиология. Возбудителем этого гельминтоза у человека являются шисто- сомы из группы трематод: Schistosoma haematobium, Schistosoma mansoni и Schistosoma japonicum. Schistosoma haematobium вызывает шистосомоз мочеполовой системы, который впервые был обнаружен Бильгарцом и поэтому носит название бильгарциоза. Эпидемиология и патогенез. Яйца паразита проделывают свой цикл разви- тия в организме пресноводных моллюсков до стадии церкариев, которые и внедряются через кожу в организм человека. Церкарии очень быстро созре- вают и превращаются в шистосомулы, проникающие в периферические вены, где и образуются половозрелые особи. Отсюда оплодотворенные самки на- правляются к месту излюбленного обитания: вены таза, мезентериальные и геморроидальные вены, а также в стенку толстой кишки. Здесь самки от- кладывают яйца, что вызывает повреждение ткани. Часть яиц выделяется с мочой и калом во внешнюю среду, являясь источником распространения гельминтоза. Очаги главным образом уринарного шистосомоза находятся в Африке. Schistosoma mansoni встречается в Южной и Центральной Америке, Африке, Schistosoma japonicum — в Японии и странах Юго-Восточной Азии. Патологическая анатомия. При шистосомозе наблюдаются изменения пре- жде всего в местах отложения яиц, т. е. в мочевом пузыре, стенке толстой кишки. Наиболее часто встречается уринарный шистосомоз, при кото- ром поражается мочевой пузырь. В ранний период болезни в поверх- ностных слоях слизистой оболочки мочевого пузыря развиваются воспаление, кровоизлияния, слущивание эпителиального покрова. Затем изменения рас- пространяются на более глубокие слои стенки. В подслизистом слое вокруг яиц шистосом появляются лейкоцитарные инфильтраты, они охватывают всю толщину слизистой оболочки, в которой образуются язвы. Со временем экс- судативная тканевая реакция сменяется продуктивной, вокруг яиц формирует- ся грануляционная ткань с большим числом эпителиоидных клеток, образует- ся шистосомная гранулема (рис. 369). Процесс приобретает хроническое течение, исходом которого являются склероз и деформация стенки пузыря. 512 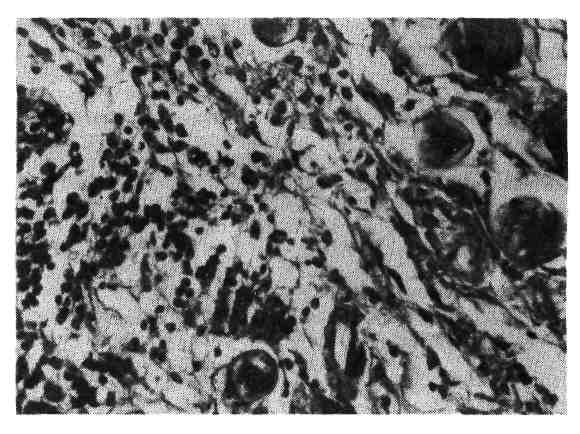 Рис. 369. Уринарный ши- стосомоз. Яйца паразитов в шистосомной грану- леме. Погибшие яйца обызвествляются. Распространение паразита в вены малого таза ведет к возникновению очагов поражения в предстательной железе, при- датке яичка. При медленном заживлении язв мочевого пузыря и длительном течении болезни возможно развитие рака. При шистосомозе толстой кишки в ней развиваются аналогичные из- менения, завершающиеся склерозом стенки. Встречаются случаи шистосомно- го аппендицита. Возможно гематогенное распространение процесса. Па- разиты заносятся в печень, легкие, головной мозг и на месте их внедрения возникают воспалительные инфильтраты из лимфоцитов, нейтрофилов, эпите- лиоидных клеток. Быстро образуется грануляционная ткань, развивается склероз. БОЛЕЗНИ ДЕТСКОГО ВОЗРАСТА ПРЕНАТАЛЬНАЯ ПАТОЛОГИЯ ПОНЯТИЕ О ПЕРИОДИЗАЦИИ И ЗАКОНОМЕРНОСТЯХ ПРОГЕНЕЗА И КИМАТОГЕНЕЗА В понятие «пренатальная (синоним: антенатальная) патология» включают- ся все патологические процессы и состояния человеческого зародыша, начиная с оплодотворения и кончая рождением ребенка. Пренатальный период челове- ка исчисляется длительностью беременности — 280 днями, или 40 нед, по ис- течении которых наступают роды. Учение о внутриутробной патологии (уродствах и пороках развития) возникло очень давно. В арабской медицине XI, XII и XIII веков имелись уже подробные описания различных вро- жденных пороков. Амбруаз Паре (1510—1590) написал о них специальную книгу. Однако науч- ное изучение этого вопроса началось в начале XX века (Швальбе). При этом большинство иссле- дователей считали, что основное значение в развитии врожденных пороков у человека имеет наследственность. Большое значение для понимания влияния факторов внешней среды на фор- мирование пороков развития имело открытие австралийского офтальмолога Грегга, который в 1951 г. опубликовал свои данные о значении вируса краснухи (рубеолы) в возникновении мно- жественных врожденных пороков развития у человека. Он показал, что при заболевании матери 513 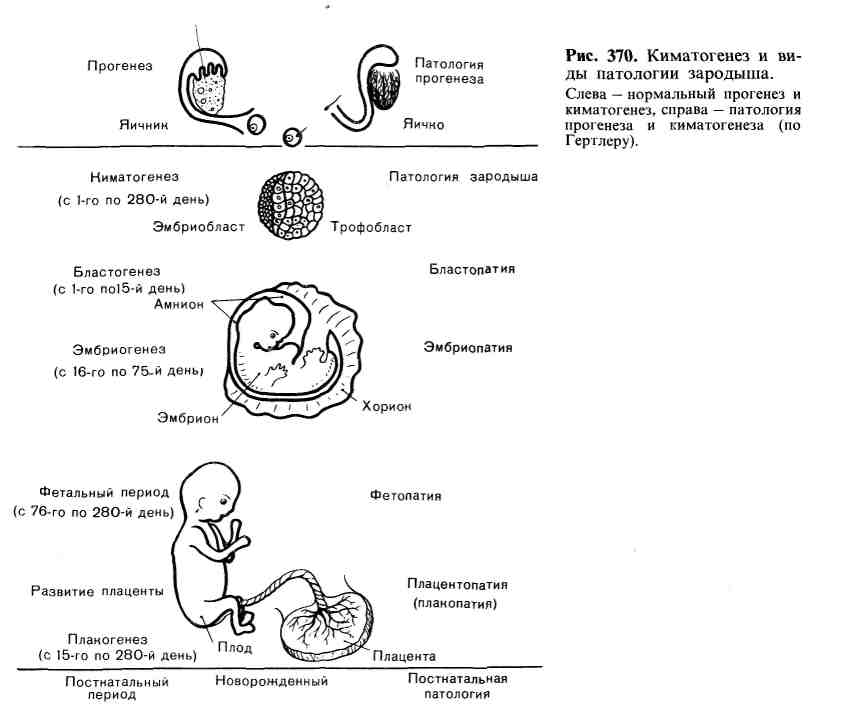 краснухой в первую треть беременности у 12 % детей развиваются врожденные пороки и в 7,2 % отмечается мертворожденность, во вторую треть беременности — 3,8 и 4,6 % соответственно, в последнюю треть беременности пороков развития у плода не возникает, а мертворожденность имеет место в 1,7 % случаев. С этого момента сформировалось учение о возможности проявле- ния пороков развития у человека, обусловленных воздействием экзогенных факторов, и под- твердились данные об основном значении времени воздействия этих факторов на развивающий- ся зародыш. В настоящее время пренатальная патология человека выросла в проблему, имеющую не меньшее значение в медицине, чем проблема сердечно-сосу- дистых заболеваний, опухолей и психических болезней. Все развитие, начиная от созревания половой клетки (гаметы) до рождения зрелого плода, делят на два периода — период прогенеза и период киматоге- неза (от греч. kyema — зародыш) (рис. 370). Периоду прогенеза соответ- ствует созревание гамет (яйцеклетки и сперматозоида) до оплодотворения. В этот период возможно возникновение патологии гамет— гамето- п а т и и. В зависимости от того, в каких структурах наследственного аппарата гаметы произошла мутация, различают генные, хромосомные и геномные му- тации. Наследственные болезни, в том числе и пороки развития, могут быть следствием мутаций гамет родителей ребенка (спонтанные мутации) или его отдаленных предков (унаследованные мутации). Период киматогенеза исчисляется с момента оплодотворения и образования зиготы до родов и делится на три периода. Первый период — бластогенез — продолжается с момента оплодотворения до 15-го дня бере- менности, когда идет дробление яйца, заканчивающееся выделением эмбрио- 514 и трофобласта. Второй период — эмбриогенез — охватывает отрезок вре- мени с 16-го по 75-й день беременности, когда осуществляется основной органо- генез и образуются амнион и хорион. Третий период — фетогенез — продол- жается с 76-го по 280-й лень, когда идут дифференцировка и созревание тка- ней плода, а также образование плаценты, заканчивающиеся рождением плода. Период фетогенеза делят на ранний фетальный (с 76-го по 180-й день), к концу которого незрелый плод приобретает жизнеспособность, и п о - зднийфетальный(с 181-го по 280-й день), когда завершается созревание плода с одновременным старением плаценты. С периодом киматогенеза со- впадает киматопатия. Соответственно периодам киматогенеза разли- чают :бластопатию, эмбриопатию, раннююипозднюю фето- п ати и. Этиология. После открытия рубеолярной эмбриопатии расширились пред- ставления о влиянии экзогенных факторов, приводящем к киматопатиям. Это нашло свое подтверждение в многочисленных экспериментальных исследова- ниях. По современным' данным, 20 % пороков развития (основная патология пе- риода киматогенеза) связано с генными мутациями, 10%—с хромо- сомными аберрациями, 1О % — с влиянием экзогенных факто- ров, 60 %— с невыясненной этиологией. Полагают, что в патологии человека часто имеет место комбинация наследственных и экзогенных факторов, когда влияние экзогенных факторов оказывается лишь провоцирующим. К экзогенным факторам, способным вызывать киматопатии у че- ловека, относятся вирусы и некоторые другие микроорганизмы, а именно ви- русы краснухи, кори, ветряной оспы herpes simplex, инфекционного монону- клеоза, эпидемического паротита и гепатита, полиомиелита и гриппа, а также микоплазма, листерелла, трепонема, токсоплазма, реже микооактерия тубер- кулеза и др. Кроме инфекционных агентов, киматопатии могут быть обусло- влены влиянием лучевой энергии (у-лучи), ионизирующей радиа- ции, некоторыми лекарственными препаратами — талидомидом, гидантоином, цитостатическими средствами, гормонами, витаминами (в част- ности, витамином D), хинином и др., алкоголем, гипоксией различно- го генеза, эндокринными заболеваниями матери — сахарным диа- бетом, тиреотоксическим зобом. Употребление во время беременности алкоголя приводит к развитию алкогольной эмбриофетопатии, ха- рактеризующейся общей гипоплазией, умеренной недоношенностью, микроце- фалией, сочетающейся с птозом век, эпикантом, микрогенией. Реже встре- чаются врожденные пороки сердца. В настоящее время в связи с новыми методами лечения получили особое значение диабетические и тиреотоксические фето- и эмбриопатии. До лечения инсулином у женщин, страдающих сахарным диабетом, беременность наблю- далась редко. В настоящее время способность к деторождению у этих женщин такая же, как и у здоровых. Однако у детей, матери которых больны са- харным диабетом, пороки развития отмечаются чаще. К так называемой диабетической эмбриопатии относятся пороки развития скелета, сердечно-сосудистой, центральной нервной и мочеполовой систем. Диабе- тическая фетопатия проявляется в виде недоношенности или рождения гигантского плода кушингоидного вида. При повышенной и пониженной функциях щитовидной железы наблюдается склонность к абортам и выкиды- шам. Среди пороков развития при тиреотоксикозах преобладают анэнцефа- лия, пороки сердца, гипотиреозы с умственной отсталостью — так называемые тиреотоксические эмбриофетопатии. Патогенез. Механизм развития киматопатии изучен пока недостаточно, так как методов изучения киматопатии в динамике мало. Кроме того, приходится 515 иметь дело с двумя биологическими объектами — матерью и зародышем, на- ходящимися в сложных взаимоотношениях. Первая закономерность, характерная для патологии внутриутроб- ного периода при любом патогенном воздействии, — обязательное искажение нормального хода развития зародыша. Поэтому для понимания патогенеза пренатальной патологии большое значение имеет изучение реактивности за- родыша в разные периоды киматогенеза, так как основной жизненной функ- цией зародыша является беспрерывно идущий процесс морфогенеза. На про- цессах формообразования в первую очередь и сказывается влияние пато- генных факторов. Нарушение хода морфогенеза называется дизонтогенезом. Однако в разные периоды киматогенеза расстройства дизонтогенеза возникают на разных уровнях — от грубых нарушений развития зародыша, несовместимых с жизнью на ранних его этапах, до нарушения тонких ультраструктур клеток и тканей на поздних этапах. По мере созревания зародыша у него постепенно развивается способность реагировать на различные патогенные влияния не только нарушением морфогенеза, но и развитием других патологических про- цессов — альтерации тканей, воспаления, иммуноморфологических и компен- саторно-приспособительных сдвигов, полной и неполной регенерации тканей. Второй закономерностью, характерной для патологии особенно поздних периодов киматогенеза, является сочетание нарушений морфогенеза с другими патологическими процессами, например пороков формирования сердца с гиперплазией мезенхимальных тканей, пороков формирования голов- ного мозга с наличием некрозов, кровоизлияний и др. Третьей закономерностью, определяющей патогенез любого из периодов киматогенеза и имеющей большое значение в развитии того или иного патологического состояния зародыша, является время воздей- ствия на него патогенного агента. Так, в период бластогенеза зародыш на любое воздействие отвечает нару- шением имплантации оплодотворенного яйца или развития эмбрио- и трофо- бласта в бластоцисте. В период эмбриогенеза, когда осуществляется основной морфогенез внутренних органов и частей тела зародыша, почти любое повре- ждение приводит к развитию того или иного врожденного порока или к гибе- ли эмбриона. По данным советских эмбриологов П. Г. Светлова и А. П. Дыбана, пренатальная гибель за- родыша чаще наблюдается в определенные сроки его внутриутробной жизни. Для эмбриона млекопитающих и человека такими периодами особо высокой чувствительности к патогенным агентам являются имплантация оплодотворенного яйца в слизистую оболочку матки, что со- ответствует 14 дням внутриутробного развития, и плацентация — начало формирования пла- центы, что соответствует 3-6 нед внутриутробного развития. Эти два периода наибольшей чув- ствительности зародыша к воздействию повреждающих агентов получили название первого ивторогокритическихпериодов. Однако гибель эмбриона в большинстве случаев на- ступает не сразу после повреждения, а через некоторое время, так как сроки пренатальной смертности запаздывают по отношению к названным срокам критических периодов. Так, оказа- лось, что для первого критического периода наибольшая пренатальная смертность приходится на 4-ю неделю беременности, а для второго — на 8 —11-ю неделю. Такое запаздывание соответ- ствует клиническим наблюдениям, по которым преобладающая часть самопроизвольных абор- тов у женщин зарегистрирована именно в сроки от 4 до 10—11 нед беременности. Оказалось, что различные тератогенные агенты могут привести кодномуитомужепорокуразвитияв зависимости от времени воз- действия на эмбрион; например, влияние лучевой энергии и хинина на 3-й не- деле внутриутробного развития приводит к нарушениям формирования нерв- ной трубки зародыша. Вместе с тем один и тот же тератогенный агент может вызвать разные по- роки развития, воздействуя в различные сроки эмбриогенеза. 516 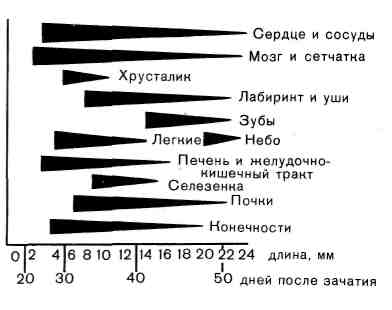 |
