ЛЕКЦИИ 50 лекций по хирургии под редакцией академика B.C. Савельева. ЛЕКЦИИ 50 лекций по хирургии под редакцией академика B.C. Савель. Media medica 2003 п од редакцией академика B. C. Савельева
 Скачать 9.44 Mb. Скачать 9.44 Mb.
|
|
Рис. 1. Шкалы оценки интенсивности боли. шво 0 12 3
ВАШ 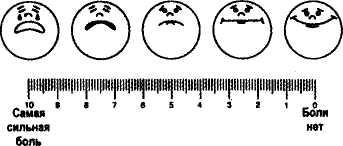 О  ценка интенсивности боли необходима для контроля эффективности обезболивания. В качестве меры эффективности обезболивания применяются шкалы оценки выраженности боли у пациентов в покое (рис.1), а также данные состояния гемодинамики и спирометрических тестов. ценка интенсивности боли необходима для контроля эффективности обезболивания. В качестве меры эффективности обезболивания применяются шкалы оценки выраженности боли у пациентов в покое (рис.1), а также данные состояния гемодинамики и спирометрических тестов.Наиболее часто применяют визуально-аналоговую шкалу интенсивности боли (ВАШ) от 0 до 10 баллов в виде линии длиной 10 см, над которой графически отражена степень болевых ощущений. Эту шкалу предъявляют пациенту, и он сам отмечает на ней степень своих болевых ощущений. Подобные шкалы необходимы для количественной характеристики динамики интенсивности болевого синдрома в процессе лечения. Данные ВАШ в покое не позволяют судить о том, насколько хорошо пациент благодаря проводимой аналгезии может двигаться и откашливать мокроту. Поэтому ряд исследователей признают более важным тестировать пациентов с помощью ВАШ при движении и откашливании. Эффективным обезболивание можно считать при наличии оценки по ВАШ при откашливании 3 балла и ниже. При таких значениях ВАШ пациенты в состоянии двигаться, довольно глубоко дышать и эффективно откашливаться, что снижает риск развития легочных и тромботических осложнений. У пациентов отделений реанимации и интенсивной терапии, которым проводится искусственная вентиляция легких и седация, оценка интенсивности болевого синдрома с помощью визуально-аналоговых шкал затруднена. По данным SUPPORT (the Study to Understand Prognoses and Preferences for Outcomes and Risks of Treatment), боль испытывают около 50% пациентов в критическом состоянии, и 15% описывают ее как очень интенсивную. В то же время изменения физиологических показателей (частота сердечных сокращений, артериальное давление, частота дыхания, потоотделение, размер зрачка) в ответ на боль в условиях блока интенсивной терапии не являются специфичными. Оценивать интенсивность боли у этих больных необходимо для назначения адекватных доз анальгетиков, так как известно, что оптимальное обезболивание может положительно влиять на исход заболевания. Рядом исследователей предложена поведенческая шкала боли (Behavioral Pain Scale, BPS), оценка по которой может быть произведена в ходе наблюдения за больными. Интенсивность болевого синдрома у пациентов на искусственной вентиляции легких, кото- 390 анестезиология и реаниматология рым проводится седация, оценивается по состоянию мимической мускулатуры, движениям верхних конечностей, синхронности с аппаратом ИВЛ. Исследования показали, что, используя BPS, можно достоверно оценить выраженность боли даже у этого контингента больных. Невозможно в краткой лекции описать все способы послеоперационной аналгезии, однако их можно сгруппировать следующим образом для удобства восприятия и последующего изложения: 1. Использование опиоидов для послеопераци онной аналгезии:
• непарентеральное введение опиоидов (щеч ное/подъязычное, пероральное, трансдермальное, назальное, ингаляционное, внутрисуставное). 2. Методы регионарной аналгезии (с использова нием местных анестетиков и их комбинаций с опиоидами и клофелином): • эпидуральная; • другие (внутриплевральная, паравертебраль- ная, субарахноидальная, продолжительная блокада межреберных нервов, аналгезия плечевого сплете ния). 3. Применение нестероидных противовоспали тельных препаратов:
4. Применение о^-адренергических агонистов:
7. Нефармакологические методы:
Исторически сложилось так, что очень широко, вплоть до настоящего времени, для послеоперационной аналгезии использовали опиоиды. Ниже приведены наркотические аналгетики, применяемые в настоящее время для послеоперационного обезболивания (табл. 1). Морфин применяется обычно в дозе 10 мг внутримышечно, действие его продолжается 3-5 ч. Высшая доза для взрослых: разовая 0,02 г, суточная 0,05 г. Наиболее важными побочными эффектами являются угнетение дыхания, тошнота и рвота. Хотя морфин имеет ряд нежелательных побочных эффектов, он является отличным аналгетиком и принят в качестве "золотого стандарта", в сравнении с которым оценивается действие всех остальных опиоидов. Промедол (тримеперидин) применяется обычно в дозе 20 мг, что вызывает 3-4-часовую аналгезию. По аналгетической активности он несколько слабее морфина, но значительно менее токсичен, в меньшей степени угнетает дыхательный центр, реже вызывает рвоту. Омнопон (пантопон) представляет собой смесь гидрохлоридов алкалоидов опия, где на долю морфина приходится около 50%, применяется в дозе 20 мг. Высшая доза для взрослых: разовая - 0,03 г, суточная - 0,1 г. Обладает меньшей аналгетической активностью, чем морфин и промедол, что обусловливает его меньшую популярность. Бупренорфина гидрохлорид - один из популярных препаратов для послеоперационного обезболивания за рубежом. Относится к частичным агонистам ц-опиоидных рецепторов, одновременно являясь антагонистом к-опиоидных рецепторов. Бупренорфин по аналгетической активности превосходит морфин в 30-40 раз, его разовая доза составляет при внутримышечном и внутривенном введении 0,3-0,6 мг, при сублингвальном - 0,2-0,4 мг. Важное преимущество препарата - возможность его применения в различных формах - внутримышечное, внутривенное, суб-лингвальное, а также в форме назального спрея. Длительность действия препарата 6-8 ч. Отличительная особенность бупренорфина - его высокое сродство к ц-опиоидным рецепторам, вследствие чего депрессия дыхания, вызванная бупренорфином, лишь частично устраняется высокими дозами конкурентного антагониста налоксона. Трамадола гидрохлорид (тралюл) - аналгетик, опосредующий обезболивающий эффект как через ц-опиоидные рецепторы, так и путем ингибирования норадренергического и серотонинергического механизма передачи болевой импульсации. Большое преимущество препарата - наличие значительного количества лекарственных форм (ампулированная, таблетированная, капсулы, капли, свечи). Внутривенно и внутримышечно трамадол применяется обычно в дозе 100 мг. Буторфанола тартрат (стадол) - агонист-антагонист - синтетический аналгетик класса налор-фин-циклазоцина. Для внутривенного и внутримышечного введения применяется в дозе 2 мг; продолжительность действия 3-4 ч. Аналгетическая активность препарата в 5-7 раз выше морфина. Аналгети-ческий эффект буторфанола опосредуется путем взаимодействия с к-опиоидными рецепторами, поэтому препарат оказывает незначительное депрессивное влияние на функцию дыхания. К положительным сторонам препарата относятся: низкий наркогенный потенциал, отсутствие влияния на моторику желудочно-кишечного тракта и тонус сфинктеров, к отрицательным - неблагоприятное воздействие на гемодинамику (увеличение СИ, ДЛА, ЛСС) и вероятность развития дисфории. Т  аблица 1. Эквианалгетические дозы опиоидов для парентерального введения аблица 1. Эквианалгетические дозы опиоидов для парентерального введенияДоза, мг П  репарат репарат10 1,5 10 2 0,1 1 75 0,3 2 М  орфин орфинГидроморфон Метадон Леворфанол Фентанил Оксиморфон Меперидин Бупренорфин Буторфанол  391 391анестезиология и реаниматология Налбуфина гидрохлорид (нубаин) - агонист-ан-тагонист опиоидных рецепторов. Агонистическая активность препарата опосредуется через к-опиоид-ные рецепторы. Аналгетическая активность налбуфина, по сравнению с морфином составляет 0,5-1, т.е. 10 мг налбуфина эквивалентны такой же дозе морфина. Налбуфин обладает крайне низкой степенью развития привыкания и минимальным влиянием на гемодинамику. Препарат вызывает незначительное угнетение дыхания, не имеющее клинического значения. Для налбуфина характерно наличие эффекта «потолка» в отношении аналгетической активности и влияния на дыхание - повышение дозы налбуфина не усиливает аналгезию и депрессию дыхания («потолок» составляет около 30 мг/70 кг). Считаем необходимым остановиться более подробно на путях использования этого метода обезболивания. Традиционным является внутримышечное введение опиоидов в послеоперационном периоде. Как правило, для этого используют морфин, промедол (тримеперидин) и омнопон (пантопон). К достоинствам традиционной аналгезии относятся: легкость применения, дешевизна метода, а также постепенное развитие побочных эффектов, что дает больше возможностей борьбы с ними. Вместе с тем эта методика часто приводит к неадекватному обезболиванию (более 60% пациентов отмечают неудовлетворительное качество послеоперационной аналгезии). Причины данного факта кроются в том, что вводятся фиксированные дозы, без учета фармакологической вариабельности; часто инъекции опиоидов производятся с большими перерывами, т.е. тогда, когда уже произошел «прорыв» боли. Немаловажным моментом является также и то, что при внутримышечном пути введения начало обезболивания замедлено. Внутривенное введение опиоидов (болюс, продолжительная инфузия, контролируемое пациентом обезболивание - КПО). Болюсное введение - наиболее быстрый способ достижения аналгезии. Быстрее действуют те препараты, которые более липофильны. Этот метод применяется для аналгезии пациентов, находящихся на ИВЛ в условиях ОИТ. Угнетение дыхания в такой ситуации является не недостатком, а преимуществом. КПО - метод, использующий быстрый аналгети-ческий эффект болюсного введения. Пациент сам определяет скорость внутривенного введения препарата, обеспечивая тем самым контроль с обратной связью. Прибор для КПО включает точный источник инфузии и контролируемое устройство пациент - прибор. Для ограничения устанавливаемой дозы, числа доз, которые могут быть введены, а также интервала между дозами предусмотрено специальное устройство безопасности. Ниже приведены параметры КПО (табл. 2). При КПО устранение боли обеспечивается лучше, чем при обычном методе периодического внутримышечного введении аналгетика. Трансдермальное применение - фентанил, будучи высоколипофильным веществом, легко проникает через кожу. Наклейки с фентанилом позволяют поддерживать постоянную концентрацию препарата в крови с помощью системы, которую заменяют каждые 3 сут. Трансдермальная система высвобождает препарат со скоростью 25 мкг/ч. Максимальный болеутоляющий эффект после наложения наклейки развивается в течение 24-72 ч. Ввиду широкой фармакологической вариабельности такого пути у разных пациентов этот метод малопригоден для контроля острой боли. Метод более применим для устранения хронической боли при злокачественных заболеваниях в терминальной стадии. Ректальное введение опиоидов - этот путь введения широко не применяется. Из прямой кишки опиоиды быстро всасываются и попадают в систему нижней полой вены, а затем, минуя печень, в системный кровоток. Однако при этом отмечается значительная вариабельность достигаемой плазменной концентрации препарата. Считается, что лучшим показанием к ректальному введению опиоидов служит трудно контролируемая хроническая боль, сопровождающаяся дисфагией. Сублингвальное применение бупренорфина позволяет достичь хорошего уровня аналгезии. Сочетание этого метода с введением агонистов опиоидных рецепторов может привести к развитию дисфории и возобновлению болевого синдрома; так что при выборе этого способа аналгезии важно использование бупренорфина в качестве единственного опиоида в период подготовки и проведения операции, а также в послеоперационном периоде. В последнее время уделяется большое внимание использованию регионарного обезболивания, не  Параметры режима* Параметры режима*Препарат  морфин морфингидроморфон меперидин  Концентрация, мг/мл Концентрация, мг/млДоза по требованию, мл Интервал блокировки, мин Скорость постоянной инфузии, мл/ч днем ночью Предельная доза за 1 ч, мл Нагрузочная доза (каждые 5 мин до состояния комфорта), мг Максимальная нагрузочная доза, мг 1 1 6 0 0,5 < 12 2 10-15 0,5 0,5 10 0 0,5 <6 0,5 2-4 10 1 6 0 0,5 < 10 2 75-150  *Указанные дозы рассчитаны на пациентов с массой тела 55-70 кг, не принимающих опиоиды; следует корригировать дозы в соответствии с состоянием пациента, опытом приема. *Указанные дозы рассчитаны на пациентов с массой тела 55-70 кг, не принимающих опиоиды; следует корригировать дозы в соответствии с состоянием пациента, опытом приема.3  92 92анестезиология и реаниматология только как метода интраоперационной защиты пациента, но и как способа адекватной аналгезии в послеоперационном периоде. Самый распространенный метод послеоперационной регионарной аналгезии — эпидуральная блокада. Длительная эпидуральная аналгезия является эффективным методом купирования послеоперационной острой боли с низким риском развития побочных эффектов и высокой степенью удовлетворенности пациентов качеством обезболивания. Эта методика абсолютно показана у пациентов с высоким риском развития сердечно-легочных осложнений после торакальных, ортопедических, абдоминальных операций. В проведении ДЭА нуждаются от 5 до 15% хирургических больных. С появлением местных анестетиков длительного действия стало возможным проведение продленной эпидуральной инфузии, которая обладает определенными преимуществами перед перемежающимися болюсными введениями. К сожалению, продленной эпидуральной инфузии свойственны и недостатки. Если очаги болевой импульсации значительно удалены друг от друга, невозможно провести полноценное обезболивание. Возможно обеспечение аналгезии на протяжении 5—7 дерматомов, в проекции которых находится кончик эпидурального катетера. В зависимости от характера операции предлагаются следующие уровни установки катетеров для эпидуральной аналгезии:
Thy и выше может оказывать существенное влияние на функционирование жизненно важных систем органов (дыхательная и сердечно-сосудистая). В настоящее время в клинических условиях для эпидурального обезболивания используются следующие группы препаратов:
|

