ЛЕКЦИИ 50 лекций по хирургии под редакцией академика B.C. Савельева. ЛЕКЦИИ 50 лекций по хирургии под редакцией академика B.C. Савель. Media medica 2003 п од редакцией академика B. C. Савельева
 Скачать 9.44 Mb. Скачать 9.44 Mb.
|
|
Заключение Анализ этиологии легочных деструкции позволяет утверждать, что это проблема не столько медицинская, а скорее социально-медицинская, отражающая неблагополучие современного российского общества. Поэтому важным этапом профилактики возникновения ОБДЛ является улучшение социальных условий жизни и санитарное просвещение населения. Опыт госпитальной хирургической клиники позволил нам осветить некоторые аспекты лечения ОБДЛ, но мы не претендуем на их бесспорность. Мы попытались акцентировать внимание на тех аспектах проблемы, которые, на наш взгляд, недостаточно освещены в литературе. Несмотря на успехи легочной хирургии, летальность среди больных с острыми абсцессами и особенно, гангреной легкого остается высокой. Внед- рение в клиническую практику антибиотикотера-пии, прогресс в реаниматологии, совершенствование техники оперативных вмешательств позволили снизить летальность при абсцессах до 2-8%. При распространенной гангрене легкого она остается на уровне 15-25%. Наиболее частыми причинами смерти являются пневмогенный сепсис и полиорганная недостаточность (около 30-45%), легочное кровотечение (до 10%). Анализ причин летальных исходов позволяет прийти к выводу, что прогресс в этом сложном разделе хирургии должен быть связан прежде всего со своевременным предупреждением легочных нагноений, совершенствованием реаниматологического и анестезиологического пособия, внедрением в клиническую практику достижений последнего десятилетия в лечении хирургического сепсиса. Литература
9. Hirshberg B, Sklair-Levi M, Nir-Paz R. et al. Factors Predicting Mortality of Patients With Lung Abscess // Chest. - 1999. - Vol. 115, N 3. - P. 746-750. 10. Yang P.-C. Ultrasound-guided transthoracic biopsy of the chest // Radiol. Clinics North Amer. - Vol. 38, N 2. - P. 571-578.  363 363     Рис. 18. Схема проведения окклюзии сегментарного бронха с помощью фибробронхоскопа при ЛК первой степени. Рис. 18. Схема проведения окклюзии сегментарного бронха с помощью фибробронхоскопа при ЛК первой степени.а - схема манипуляции; б - внешний вид фибробронхоскопа с окклюдером; 1 - коникостомический катетер; 2 - окклюдер 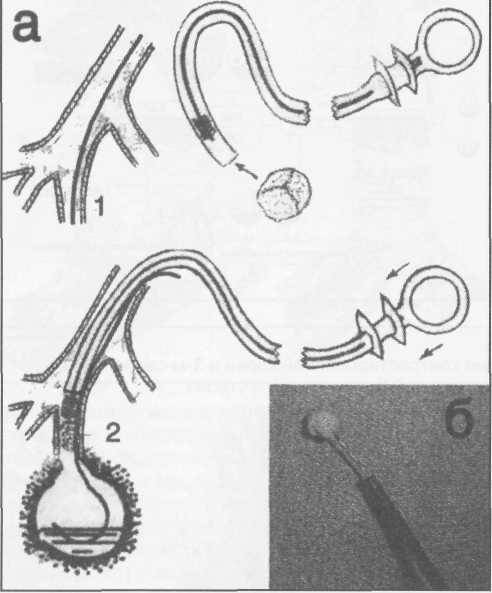 Легочное кровотечение Легочное кровотечение (ЛК) является жизнеуг-рожающим осложнением ОБДЛ. Его частота достигает 12-27% и не находится в прямой зависимости от массивности поражения легочной ткани. Что касается источника кровотечения, то в настоящее время принято считать, что как ветви легочной артерии, так и бронхиальные артерии (преимущественно), при их вовлечении в патологический процесс, могут стать причиной геморрагии различной интенсивности Ниже приведем классификацию легочных кровотечений, разработанную в клинике госпитальной ХИрурГИИ: I степень(кровохарканье) 1а - 50 мл в сутки; 16 - от 50 до 200 мл в сутки; 1в -от 200 до 500 мл в сутки. II степень (массивное кровотечение) Па - от 30 до 200 мл в час; Пб - от 200 до 500 мл в час III степень (профузное кровотечение) Ша - 100 мл и более одномоментно. Сопровождается выраженными нарушениями вентиляции легких Шб - острая обструкция трахеобронхиального дерева и асфиксия независимо от объема кровопо-тери. В зависимости от интенсивности ЛК придерживаемся следующего лечебно-диагностического алгоритма (рис.1б). В качестве основных мероприятий в алгоритм включены эндоскопическая окклюзия бронха и эн-доваскулярная окклюзия бронхиальных артерий. При I степени легочного кровотечения в лабора- Рис. 19. Ригидная трахеобронхоскопия при профузном легочном кровотечения с окклюзией главного бронха а - схема, 1- микроконикостома; 1 - окклюдер в экстракционных щипцах; 2 - окклюдер установлен в правый главный бронх; б - бронхиальная арте-риография больной Ч., контрастированная кровь поступает в левый главный бронх, огибая бронхо-окклюдер (3); в - внешний вид окклюдера в экстракционных щипцах и бронхоскопа. 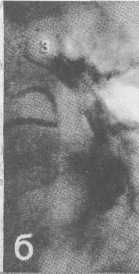 * .. ;■  т  орию эндоваскулярной хирургии направляются больные подгруппы В, а также пациенты подгрупп А и Б, в случае рецидива геморрагии. При 1в и Па степени легочного кровотечения после успешной эндоваскулярной окклюзии (рис.17) больные могут быть направлены в отделение пульмонологии или торакальной хирургии. орию эндоваскулярной хирургии направляются больные подгруппы В, а также пациенты подгрупп А и Б, в случае рецидива геморрагии. При 1в и Па степени легочного кровотечения после успешной эндоваскулярной окклюзии (рис.17) больные могут быть направлены в отделение пульмонологии или торакальной хирургии.В качестве эндоскопического пособия при первой степени легочного кровотечения отдавали селективной окклюзии сегментарных и субсегментарных бронхов с помощью фибробронхоскопа (рис. 18). При легочном кровотечении Пб, III степеней целесообразно транспортировать больного в лабораторию эндоваскулярной хирургии (минуя прочие подразделения), где синхронно выполняются эндоскопические и внутрисосудистые вмешательства. При профузных кровотечениях реанимация начинается немедленно у постели больного, а главной составляющей является интубация трахеи с постоянной аспирацией крови до выполнения ригидной трахеобронхоскопии с окклюзией главного или долевого бронха (рис.19). Организация работы в специализированном учреждении должна предполагать возможность выполнения реанимационной трахеобронхоскопии на всех этапах оказания помощи больным с массивными и профузными кровотечениями. На основании многолетнего опыта лечения больных с ОБДЛ считаем целесообразным проводить профилактическую ЭОБ, если предполагается абсцесс- или плевроскопия с эндоскопической некрсеквестрэктомией, при которых реально возникновение массивного легочного кровотечения. Практическую значимость приведенного положения иллюстрирует одно из наших наблюдений. Больной К, 47 лет, поступил в областной центр хирургической инфекции 27.08.95 через 3 нед от начала заболевания. Состояние тяжелое, обусловлено эн- 362  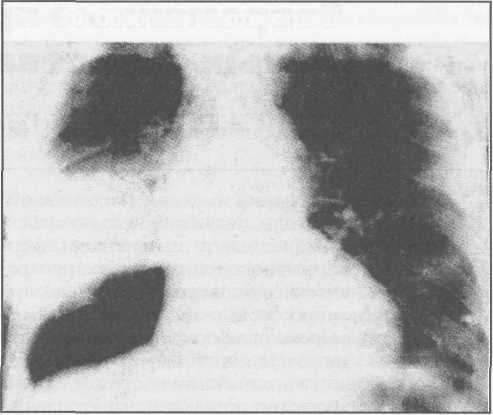 Рис. 20. Обзорная рентгенограмма больного К. догенной интоксикацией, гнойно-резорбтивной лихорадкой, дыхательной недостаточностью. Пациент выделяет большое количество зловонной мокроты с примесью крови. Частота дыхательных движений 28-30 в минуту в покое. Грудная клетка асимметрична, правая половина отстает при дыхании. При перкуссии: над передней поверхностью справа - тимпанит, сзади в нижних отделах - укорочение звука. Аус-культативно: ослабление дыхания справа. Тахикардия. В периферической крови гиперлейкоцитоз, сдвиг формулы влево, анемия. На обзорных рентгенограммах грудной клетки: распространенный гидропневмоторакс, легкое коллабировано на 1/3 объема (рис. 20). Диагноз: распространенная гангрена правого легкого, субтотальная острая парапневмоническая эмпиема плевры, множественные бронхоплевральные свищи. Плевральная полость дренирована, удален зловонный экссудат, мелкие легочные секвестры. Больному проводилось стандартное бронхологичес-кое исследование и медикаментозная терапия. В плане предоперационной подготовки решено провести торакоскопию с санацией плевральной полости под визуальным контролем и, возможно, некрсеквестрэк-томией. Учитывая обильное гноетечение с примесью крови и вероятность массивного кровотечения при эндоскопической операции, перед торакоскопией правый главный бронх окклюзирован поролоном. Процедура проводилась в операционной, развернутой для экстренной торакотомии. Плевра покрыта гнойно-фибринозными массами. Легочные сосуды и бронхи нижней и средней долей скелетированы. Множественные легочные секвестры. При удалении секвестров началось профузное кровотечение из нижней легочной вены. Сделана торакотомия, эвакуирован гемоторакс объемом 1200 мл. Выполнена пневмонэктомия. Выписан на 115-е сутки после госпитализации. Ретроспективный анализ рассмотренной ситуации показал, что профилактическая ОБ обеспечила нормальную вентиляцию легкого во время пуль-монэктомии и предотвратила развитие асфиксии. Заключение Анализ этиологии легочных деструкции позволяет утверждать, что это проблема не столько медицинская, а скорее социально-медицинская, отражающая неблагополучие современного российского общества. Поэтому важным этапом профилактики возникновения ОБДЛ является улучшение социальных условий жизни и санитарное просвещение населения. Опыт госпитальной хирургической клиники позволил нам осветить некоторые аспекты лечения ОБДЛ, но мы не претендуем на их бесспорность. Мы попытались акцентировать внимание на тех аспектах проблемы, которые, на наш взгляд, недостаточно освещены в литературе. Несмотря на успехи легочной хирургии, летальность среди больных с острыми абсцессами и особенно, гангреной легкого остается высокой. Внед- рение в клиническую практику антибиотикотера-пии, прогресс в реаниматологии, совершенствование техники оперативных вмешательств позволили снизить летальность при абсцессах до 2-8%. При распространенной гангрене легкого она остается на уровне 15-25%. Наиболее частыми причинами смерти являются пневмогенный сепсис и полиорганная недостаточность (около 30-45%), легочное кровотечение (до 10%). Анализ причин летальных исходов позволяет прийти к выводу, что прогресс в этом сложном разделе хирургии должен быть связан прежде всего со своевременным предупреждением легочных нагноений, совершенствованием реаниматологического и анестезиологического пособия, внедрением в клиническую практику достижений последнего десятилетия в лечении хирургического сепсиса. Литература
9. Hirshberg В., Sklair-Levi M., Nir-Paz R. et al. Factors Predicting Mortality of Patients With Lung Abscess // Chest. - 1999. - Vol. 115, N 3. - P. 746-750. 10. Yang P.-C. Ultrasound-guided transthoracic biopsy of the chest // Radio! Clinics North Amer. - Vol. 38, N 2. - P. 571 -578.  363 363хирургическая инфекция и гнойно-септическая хирургия Современные принципы лечения гнойных заболеваний мягких тканей А.П.Чадаев, АЛ.Зверев, М.САлексеев  За последние годы появились высокоэффективные антибиотики и антисептики, ферментные и иммунокорригирующие препараты, такие технические достижения, как ультразвук, лучи лазера, компрессионно-дистракционный ос-теосинтез и т.д. Произошли существенные изменения методологии лечения гнойных процессов - от вскрытия гнойника кратчайшим доступом, дренирования его марлевыми повязками, чаще с гипертоническим раствором поваренной соли и последующего открытого ведения раны, до закрытия гнойных ран первичными или первично-отсроченными швами после радикальной некрэктомии и наложения дренажно-промывных систем (80-е годы). Все это позволило существенно улучшить функциональные и эстетические результаты операций. Наиболее существенные в этом плане позитивные изменения произошли при лечении глубоких форм панарициев, флегмон кисти и лактационных маститов. Глубокие формы панариция и флегмоны кисти Этиопатогенез Возникновение острых гнойных процессов на пальцах и кисти чаще всего обусловлено золотистым стафилококком, который доминирует в 69-90% случаев, реже - в монокультуре, чаще — в ассоциациях. Растет частота смешанной грамполо-жительной и грамотрицательной микрофлоры. Для укушенных инфицированных ран как одной из причин развития панарициев и флегмон,особенно характерна анаэробная микрофлора. По частоте среди всех гнойных процессов гнойные заболевания пальцев и кисти занимают первое место, составляя свыше 30% всех первичных обращений к хирургу. Причиной их развития более чем в 60% случаев являются раны, в 25% - микротравмы и мозоли. В ряде случаев развитие флегмон кисти является следствием прогрессирования панариция. До 45% стационарных больных предварительно оперируются на амбулаторном этапе, причем многие - неоднократно. Клиническая семиотика Клиническая картина панариция достаточно яркая и описана во многих руководствах по гнойной хирургии. Главенствующим симптомом является боль - от ноющей при свищевых формах до пульсирующей и нестерпимой при абсцедирова-нии. В большинстве случаев пациенты отмечают повышение температуры тела и ухудшение общего самочувствия. Довольно быстро развивается отек пораженной фаланги или всего пальца. Интенсивность гиперемии зависит от глубины гнойного процесса, и ее отсутствие ни в коей мере не свидетельствует об отсутствии гнойного процесса. Нарушение функции пальца отме- чается практически всегда. Точечная пальпация пуговчатым зондом позволяет выявить зоны максимальной болезненности, типичные для поражения сустава или сухожилия. Флегмоны кисти получают наименование в зависимости от места локализации инфекции. Клиника проявляется отеком, гиперемией и болезненностью тканей в зоне пораженного клетчаточного пространства. Страдает функция примыкающих к гнойному очагу пальцев. Интенсивность боли при пассивных движениях в них в большой степени зависит от вовлечения в процесс сухожильных влагалищ. Практически при всех флегмонах кисти развивается отек тканей тыльной поверхности. Страдает общее самочувствие, возможна лихорадка; при развитии лимфангоита температура тела может повышаться до 40°С. Принципы лечения Наш опыт лечения глубоких форм панариция и флегмон кисти базируется на применении разработанных в клинике методик у 11 045 больных, оперированных в отделении хирургии гнойной кисти ГКБ №4 с 1984 по 2001 г. Лечение гнойно-воспалительных заболеваний пальцев и кисти включает несколько этапов, пренебрежение любым из них неизбежно осложняет течение воспалительного процесса. Перед операцией кисть должна быть несколько раз вымыта проточной водой с мылом и, при необходимости, выбрита. Наиболее часто операции выполняем под проводниковой анестезией вне очага воспаления 1-2% раствором новокаина или 1,5% раствором тримекаина, в том числе при локализации процесса на ногтевой или средней фаланге пальца - по Оберсту-Лукашевичу; при распространении процесса проксимальнее — осуществляем блокаду соответствующих нервов в нижней трети предплечья или анестезию по Усольцевой. При флегмоне пространства Пирогова-Парона проводниковую анестезию целесообразно выполнять в верхней трети предплечья или в подмышечной ямке. При известных противопоказаниях к местной анестезии операцию осуществляем под общим обезболиванием. Операцию необходимо выполнять с ассистентом при полном обескровливании операционного поля, что позволяет определить границы некроза и дифференцировать анатомические структуры. Выбор доступа к гнойному очагу - важный аспект оперативного лечения. Разрез, обеспечивая при оптимально выбранном направлении адекватный объем операции, должен максимально щадить "рабочие" поверхности кисти соответственно схеме J.TMetzger (1955). Скальпелем следует рассекать только кожу; все дальнейшие манипуляции на тканях выполняем путем их "раздвигания" под контролем глаза. 364 хирургическая инфекция и гнойно-септическая хирургия Следующим этапом операции является тщательная некрэктомия, при которой гнойный очаг должен иссекаться по типу первичной хирургической обработки. Оставшиеся даже незначительные участки нежизнеспособных тканей могут явиться причиной длительного течения заболевания и повторных операций. В то же время чрезмерный радикализм в такой сложной анатомической области, как пальцы кисти, может нанести непоправимый эстетический и функциональный ущерб. Во время не-крэктомии сосуды и нервы фактически скелетиру-ем. Максимально щадяще следует выполнять этот этап на сухожильном аппарате: не следует спешить резецировать сухожилие, если можно ограничиться удалением отдельных некротизированных волокон. Некрэктомия на костных и суставных структурах включает удаление лишь секвестрированных участков. Порой приходится удалять все губчатое вещество кости, оставив лишь кортикальный цилиндр. При вмешательствах на суставах при гнойных артритах или остеоартритах послеоперационный период ведем в режиме дистракции, что обеспечиваем компрессионно-дистракционным аппаратом или тракцией металлогипсовой конструкцией с использованием модифицированной спицы Киршнера. Некрэктомию завершаем вакуу-мированием, санацией раны антисептиками. Хорошо себя зарекомендовала обработка раны ультразвуком низкой частоты в растворе антибиотика. После некрэктомии и гемостаза каждое клетчаточное пространство дренируем отдельной перфорированной полихлорвиниловой трубочкой, которую фиксируем к коже. После вмешательства на суставах и сухожильных влагалищах указанные структуры требуют дополнительного дренирования. Выполнение радикальной некрэктомии и адекватного дренирования остаточной гнойной полости позволяет завершить операцию наложением первичных швов на кожу атравматическими нитями 3/0-7/0. При тяжелом поражении кисти применение микроирригаторов и частичное ушивание ран дополняем наложением марлевых повязок, пропитанных мазью на гидрофильной основе. При невозможности одномоментного ушивания кожного дефекта применяем различные варианты кожной пластики. При обнаженных сухожилии или кости используем несвободную кожную пластику по типу итальянской, перекрестную с пальца на палец или лоскутом на сосудисто-нервной ножке. Гранулирующие дефекты предпочитаем закрывать свободным расщепленным кожным трансплантатом. Все пластические операции выполняем после купирования острого гнойного воспаления, но в возможно более ранние сроки. При значительных кожных дефектах, полученных при первичной травме или после некрэктомии, при невозможности выполнения радикальной некрэктомии необходимо воздержаться от наложения первичных швов и следует вести рану открыто, применяя мази на гидрофильной основе, протео-литические ферменты или другие антисептики. Иммобилизацию в послеоперационном периоде мы считаем обязательной независимо от формы заболевания. Продолжительность иммобилизации определяют сроки купирования острых воспалительных явлений. Наряду с регулярной санацией ран на перевязках проводим антибактериальную и противовоспалительную терапию, физиотерапевтические процедуры, лечебную физкультуру. Ранняя активная разработка движений пальцев и кисти (после удаления дренажей и швов) способствует более полноценному восстановлению функции кисти. Лечение отдельных форм панариция Костный панариций Если заболевание протекает достаточно длительно и имеются сформированные свищи, то воспалительные явления в коже и подкожной клетчатке, как правило, не выражены. В этой ситуации проводим радикальную некросеквестрэктомию, удаляем патологические грануляции в мягких тканях и рану закрываем первичными швами с наложением дре-нажно-промывной системы. Пораженную костную ткань нежно выскабливаем острой костной ложечкой, что достаточно для удаления аваскуляризован-ных некротизированных участков. В случае секвестрации фаланги удаляем только свободно лежащие секвестры с сохранением основного массива кости. Сухожильный панариций (гнойный тендовагинит) Тактика оперативного вмешательства при сухожильном панариции определяется состоянием прилежащей к сухожильному влагалищу подкожной клетчатки. При интактной клетчатке (в случае развития тендовагинита после укола непосредственно во влагалище) оперативное пособие ограничиваем вскрытием сухожильного влагалища в дис-тальном (на средней фаланге) и проксимальном (в проекции головки соответствующей пястной кости) отделах. После эвакуации экссудата и промывания влагалища растворами антисептиков его полость на всю длину дренируем перфорированным микроирригатором, концы которого выводим через разрезы, а на кожу накладываем швы. Когда подкожная клетчатка также вовлечена в гнойно-деструктивный процесс, выполняем продольный разрез по боковой поверхности пальца с дугообразным продолжением на ладонь в проекции "слепого мешка" влагалища сухожилий. Кожно-подкожный лоскут отпрепаровываем от влагалища, которое, как правило, бывает частично или полностью не-кротизировано, обязательно сохраняем ладонные сосудисто-нервные пучки и выполняем тщательную некрэктомию подкожной клетчатки, иссекаем нежизнеспособные участки сухожильного влагалища и некротизированные волокна сухожилия. Полностью сухожилие иссекаем только при явном его некрозе, когда оно представлено бесструктурной массой. Суставной и костно-суставной панариций. При суставном или костно-суставном панариции, как правило, выполняем Z-образный разрез на тыльной поверхности пальца в проекции соответствующего сустава. Осуществляем артротомию, ревизию полости сустава и удаляем гнойный экссудат. При отсутствии очагов деструкции в костной ткани проводим санацию полости сустава растворами антисептиков и дренируем ее перфорированным микроирригатором, а кожную рану ушиваем. При выявлении костной деструкции выскабливаем пораженные участки надкостницы и кости острой костной ложечкой, а полость сустава также дрени- 365 хирургическая инфекция и гнойно-септическая хирургия руем. Чрезвычайно важным моментом является дальнейшая декомпрессия в суставе, в противном случае возможно прогрессирование деструкции. Декомпрессия сустава обеспечивает снижение внутрисуставного давления, при этом достигается диастаз между суставными концами, что способствует купированию воспалительных явлений и препятствует формированию внутрисуставных сращений. Наложение дистракционного аппарата возможно только при отсутствии воспаления в мягких тканях сочленяющихся фаланг. Пандактилит Нередко при пандактилите сохранение пальца считают бесперспективным и ампутируют его или пораженные фаланги. Однако при правильном хирургическом лечении сохранение пальца возможно. Разрез выполняем по боковой поверхности пальца с дугообразным продолжением на ладонную поверхность кисти в проекции головки соответствующей пястной кости. Ладонный кожно-подкож-ный лоскут отпрепаровываем от сухожилий сгибателей с сохранением сосудисто-нервных пучков, подобным же образом отпрепаровываем тыльный лоскут. Оба лоскута разворачиваем, что обеспечивает хороший доступ ко всем структурам пальца. Сложность возникает только при ревизии участка тыльно-боковой поверхности основной фаланги пальца на стороне, противоположной разрезу. Доступ к этой зоне, при необходимости, осуществляем из отдельного дугообразного разреза на тыле кисти в проекции пястно-фалангового сустава. Завершение операции при пандактилите также зависит от выраженности воспалительных явлений в мягких тканях, как и при других видах панариция. В условиях острого воспаления рану выполняем марлевыми полосками с мазью на водорастворимой основе и оставляем открытой. В дальнейшем, на перевязках, при необходимости выполняем этапную некрэкто-мию. Завершать оперативное пособие наложением дренажно-промывной системы и первичных швов можно только при полной уверенности в адекватно выполненной некрэктомии. По мере стихания воспаления и очищения раны кожные дефекты могут быть закрыты вторичными швами или одним из видов кожной пластики. Применение разработанной в клинике хирургической тактики позволило значительно улучшить как непосредственные, так и отдаленные результаты лечения. Наряду с сокращением продолжительности стационарного лечения удалось практически в 1,5-2 раза уменьшить сроки амбулаторного долечивания, значительно снизить процент калечащих операций (при пандактилите количество ампутаций пальцев на различных уровнях сократилось с 51,9 до 4,4%). В 4 раза снизилось количество повторных госпитализаций, а отдаленные результаты при различных формах заболевания улучшились в 3-4 раза. Лечение флегмон кисти Кисть - сложнейший анатомический орган, поэтому знание анатомии является непременным требованием, предъявляемым к хирургам, специализирующимся в этой области. При различной локализации гнойного очага на кисти существуют определенные оперативные доступы, которые должны быть наиболее короткими и щадящими. Следует особо отметить, что выполнение больших продольных разрезов недопустимо. Создание широкого доступа возможно, модифицировав разрез по типу S-образного, дугообразного или ломаного, помня о том, что рубец стягивает ткани по длине. При межпальцевой флегмоне выполняем дугообразный разрез на ладонной поверхности кисти по Bunnell с контрапертурой на тыле кисти. При вовлечении в воспалительный процесс нескольких межпальцевых промежутков выполняем один дугообразный разрез кожи с контрапертурами над каждым пораженным промежутком. Флегмону области тенара целесообразно вскрывать дугообразным разрезом, параллельно кожной складке тенара и отступя от нее кнаружи с контрапертурным разрезом на тыле кисти в зоне первого межпальцевого промежутка. Разрез при флегмоне области гипотенара проводим по внутреннему краю возвышения мышц гипотенара с контрапертурой на тыле кисти по наружному краю V пястной кости. Вскрытие надапоневротической флегмоны выполняем разрезом по Bunnell, идущим от II межпальцевого промежутка ладони до средней кожной складки области лучезапястного сустава на ладони, или разрезами, параллельными дистальной или проксимальным ладонным бороздам по Я.Золтану. Для вскрытия флегмон срединного ладонного пространства разрез целесообразно выполнять по дистальной кожной складке ладони от IV до II межпальцевого промежутка с дальнейшим его продолжением по кожной складке области тенара до "запретной зоны". Флегмоны тыла кисти лучше оперировать из нескольких небольших дугообразных разрезов, проведенных с учетом линий Лангера. Наконец, для вскрытия U-образной флегмоны выполняем боковые разрезы на средней фаланге V пальца и основной фаланге I пальца, из которых вскрываем соответствующие сухожильные влагалища. Боковыми продольными разрезами на предплечье вскрываем пространство Пирогова-Паро-на. При поражении клетчатки областей тенара и гипотенара к указанным выше доступам добавляем соответствующие разрезы. При комбинированных и сочетанных флегмонах кисти доступы, объем некрэктомии и дренирование ран индивидуальны и зависят от конкретной клинической ситуации. Классическое изолированное поражение только одного клетчаточ-ного пространства кисти встречается, по нашим наблюдениям, лишь в 40,6%. Сочетанное воспаление сразу нескольких пространств или комбинации панариция с флегмонами кисти мы диагностировали в 59,4%. Сложность лечения этих гнойных процессов обусловлена тем, что хирург сталкивается с необходимостью вскрытия на кисти сразу нескольких гнойных очагов, связанных между собой патогенетически. Оптимальным операционным доступом при сочетанных флегмонах кисти мы считаем модифицированный нами доступ Я.Золтана, Т-образный разрез или разрез по Канавелю. При комбинированных флегмонах мы выполняем разрез по боковой нейтральной линии пальца с дугообразным переходом на ладонную или тыльную сторону кисти (в т 366 хирургическая инфекция и гнойно-септическая хирургия зависимости от преимущественной распространенности гнойного процесса). Далее осуществляем некрэктомию и санацию гнойного очага. Дренирование послеоперационных полостей и вовлеченных в гнойный процесс клетчаточных пространств выполняем, по возможности, минимальным количеством перфорированных трубочек. Убежденность в полноценной некрэктомии и отсутствие признаков сомнительной жизнеспособности кожи позволяют наложить на раны первичные швы. Безусловно, наложение первичных швов ни в коей мере не является самоцелью, поэтому при малейших признаках ишемии кожных краев или невозможности одномоментного выполнения радикальной некрэктомии наложение дренажно-промывной системы мы сочетаем с введением в раны марлевых полосок, пропитанных мазью на гидрофильной основе, с последующим открытым ведением ран или наложением ранних вторичных швов. Внедрение в клинику разработанной нами тактики лечения флегмон кисти позволило сократить продолжительность стационарного лечения в среднем на 5-7 сут и в 2,4—3 раза - количество повторных оперативных вмешательств. Процент хороших и удовлетворительных отдаленных результатов лечения возрос с 1 до 92. Таким образом, при лечении гнойно-воспалительных заболеваний пальцев и кисти оперативные доступы должны обеспечивать оптимальную ревизию тканей в зоне патологического очага при максимально выгодном в функциональном и косметическом отношении их расположении. Адекватная анестезия и обескровливание области операции являются обязательным условием полноценной некрэктомии. При завершении операции следует отдавать предпочтение дренажно-промыв-ным системам с первичными швами, что способствует сокращению длительности послеоперационного периода и ранней реабилитации пациентов. Представленные выше результаты лечения глубоких форм панариция и флегмон кисти, безусловно, не дают оснований для прекращения поиска путей дальнейшего их улучшения. Напротив, ряд позиций определяет перспективы развития данной области хирургии. Основными среди них можно назвать следующие: внедрение и применение новых методов антисептики, оптимизация антибиотикотера-пии, активное применение пластических методов в хирургии гнойной кисти, применение шва сухожилий и имплантации синтетических суставов при тяжелой гнойной патологии пальцев и кисти. Острый гнойный лактационный мастит Лактационный мастит - воспаление молочной железы в послеродовом периоде на фоне лактации. Обычно заболевание возникает в первые 2—3 нед после родов. Значительно чаще (77,6%) маститом болеют первородящие женщины. Этиология Возбудителем гнойного мастита в 90,8% случаев является золотистый стафилококк. Молочные железы обычно инфицируются в родильном стационаре, где стафилококк может длительно (до 130 дней) сохранять свою вирулентность в воздухе, на белье и различных предметах. Входными воротами инфекции могут быть устья молочных протоков, реже - трещины и экскориации сосков. Единого мнения о непосредственном источнике инфицирования молочных желез нет. Однако большинство авторов считают, что им является новорожденный, который передает инфекцию матери при кормлении. Ребенок же инфицируется от медицинского персонала, белья и предметов ухода за ним. Возможно инфицирование молочных желез и без участия новорожденного. При сочетании значительного обсеменения молочной железы патогенной микрофлорой с какими-либо неблагоприятными факторами (лактостаз, снижение иммунологической реактивности организма родильниц и др.) реальна угроза развития мастита. Патогенез Лактостаз возникает при несоблюдении режима кормления ребенка грудью, недостаточном или нерегулярном сцеживании молочных желез и во всех случаях, когда сцеживание молока затруднено. В 85,8 % случаев он предшествует маститу. При лакто-стазе количество микробов в молочных протоках увеличивается в несколько раз, одновременно нарушаются венозное кровообращение и лимфоот-ток в молочной железе. Если лактостаз не купирован в течение 3-4 сут, то в большинстве случаев возникает мастит. Трещины сосков обнаружены нами у 13,5% больных гнойным маститом. Основными причинами их возникновения являются несоответствие между избыточным отрицательным давлением в ротовой полости ребенка и растяжимостью ткани соска, а также длительный и частый контакт соска с лифчиком, промокшим молоком. Молоко вызывает раздражение и мацерацию кожи, что способствует образованию или прогрессированию имеющихся микроповреждений соска и трещин. Кроме того, на появление трещин оказывают влияние втянутые соски, их неподвижность и недостаточная эрекция, несоблюдение времени кормления ребенка. Трещины сосков существенно нарушают функцию молочных желез, вынуждают женщин из-за болей недостаточно сцеживать их, что в свою очередь приводит к лактостазу. У всех больных гнойным маститом снижена реактивность иммунной системы. Известно, что при нормально протекающей беременности происходят существенные изменения в иммунной системе женщин, характеризующиеся ее угнетением, возрастанием активности факторов, блокирующих реакции клеточного иммунитета. Эти изменения являются закономерной реакцией, способствующей длительному сосуществованию двух генетически разных организмов -матери и плода, обеспечивающей нормальное течение беременности и родов. Все показатели реактивности иммунной системы родильницы восстанавливаются к 7-м суткам после родов. Однако при осложненном течении беременности или родов, а также при экстрагенитальной патологии происходят еще более глубокие и длительные по времени изменения иммунной системы родильницы. В то же время, как установлено нами, у больных гнойным маститом беременность или роды в 84,4% случаев протекали с различными осложнениями. Неблагоприятным фактором для нормального восстановления иммунологической реактивности является интоксикация, обусловленная развитием гнойного мастита. 367 хирургическая инфекция и гнойно-септическая хирургия Классификация По характеру воспалительного процесса различают негнойные (серозный и инфильтративный) и гнойные (абсцедирующий, инфильтративно-аб-сцедирующий, флегмонозный и гангренозный) формы острого лактационного мастита. В зависимости от локализации очага воспаления мастит бывает подкожным, субареолярным, интрамам-марным, ретромаммарным и тотальным, когда поражаются все отделы молочной железы. Клиническая семиотика Клинику и течение воспалительного процесса при мастите определяют особенности анатомического строения и резкое усиление функциональной активности молочной железы в послеродовом периоде. Молочная железа имеет дольчатое строение, большое количество естественных полостей, широкую сеть молочных протоков, обилие жировой клетчатки. Поэтому воспалительный процесс плохо отграничивается и имеет склонность к распространению на соседние участки. Кроме того, для мастита характерен быстрый переход серозной и инфильтративной стадии в гнойную, а также затяжной характер течения гнойно-воспалительного процесса. Заболевание начинается остро. В первые часы развития мастита появляется чувство тяжести в молочной железе, затем - боль. Ухудшается самочувствие больных, появляется слабость, повышается температура тела до 37,5—38,0°С. Железа незначительно увеличивается в объеме, гиперемия кожи умеренная или едва заметная. Сцеживание молока болезненное и не приносит облегчения, количество молока уменьшается. При пальпации определяются болезненность и умеренная инфильтрация тканей железы без четких границ, дольки ее теряют зернистую структуру. При прогрессировании процесс переходит из серозной стадии в инфильтра-тивную, когда в молочной железе начинает пальпироваться болезненный инфильтрат с четкими границами. Гиперемия кожи не усиливается, отека ее нет. При неэффективном или несвоевременном лечении через 3-4 дня от начала заболевания воспалительный процесс приобретает гнойный характер. При этом значительно ухудшается самочувствие больных, нарастает слабость, снижается аппетит, ухудшается сон. Температура тела чаще в пределах 38-40°С. Появляются озноб, потливость, бледность кожных покровов. Значительно усиливаются боли в молочной железе, которая напряжена, увеличена в размерах, с выраженной гиперемией и отечностью кожи. Инфильтрат резко болезненный при пальпации, увеличивается в размерах. В центре инфильтрата может появиться участок размягчения, а при наличии крупной гнойной полости — флюктуация. Молоко сцеживается с трудом, небольшими порциями, часто с ним выделяется гной. Количество лейкоцитов в крови повышается до 10 000-20 000, у 72,2% больных был снижен гемоглобин до 80-90 г/л, в моче появляются белок и гиалиновые цилиндры. Диагностика Основанием для оперативного лечения являются сочетание высокой температуры тела и наличие плотного болезненного инфильтрата в тканях мо- лочной железы. В то же время следует отметить, что при лактостазе температура тела может повышаться до 39—40°С. Это объясняется повреждением молочных протоков, всасыванием молока и его пиро-генным действием. Диагностика гнойного мастита на фоне выраженного лактостаза иногда затруднительна. Поэтому при лактостазе вопрос об оперативном лечении следует решать в течение 3—4 ч после тщательного сцеживания молока. Перед сцеживанием обязательно делаем ретромаммарную но-вокаиновую блокаду и внутримышечную инъекцию 2 мл но-шпы (за 20 мин) и 0,5 мл окситоцина или питуитрина (за 1-2 мин). Если имеется только лактостаз, то после опорожнения молочной железы боли в ней исчезают, пальпируются небольшого размера безболезненные дольки с четкими контурами и мелкозернистой структурой, снижается температура тела. Если на фоне лактостаза имеется гнойный мастит, то после сцеживания в тканях железы продолжает определяться плотный болезненный инфильтрат, сохраняется высокая температура тела, самочувствие больных не улучшается. При длительности заболевания менее 3-х сут температуре тела до 37,5°С, удовлетворительном состоянии больных, наличии инфильтрата в пределах одного квадранта железы и отсутствии других местных признаков гнойного воспаления возможна консервативная терапия. При отсутствии положительной динамики в течение 2-х сут консервативной терапии показано оперативное лечение. При длительности заболевания более 3-х сут консервативная терапия возможна только при удовлетворительном состоянии больных, нормальной температуре тела, наличии инфильтрата, занимающего не более одного квадранта железы без местных признаков гнойного воспаления, неизмененных показателях общего анализа крови и отрицательных данных пункции инфильтрата. При отсутствии положительной местной динамики процесса в течение максимум 3-х сут от начала лечения, также показана операция - иссечение нерассасывающегося инфильтрата, в толще которого в этих случаях часто обнаруживают мелкие абсцессы с густым гноем. При выраженных симптомах воспаления диагностика мастита не вызывает затруднений. В то же время, по нашим данным, в 13,8% случаев из-за недооценки ряда симптомов, характерных для гнойного процесса и переоценки отсутствия таких симптомов, как флюктуация и гиперемия кожи, больные лечились в поликлинике консервативно на протяжении от 5 дней до 2 мес после развития у них гнойного мастита. В 9,8% случаев в результате длительной антибактериальной терапии при имевшемся абсцедирующем или инфильтративно-аб-сцедирующем мастите возникает "стертая" форма заболевания, когда клинические проявления не соответствуют истинной тяжести воспалительного процесса в тканях молочной железы. В этих случаях температура тела бывает нормальной или слегка повышается к вечеру, а отдельные местные признаки гнойного воспаления не выражены или отсутствуют. Однако молочная железа остается умеренно болезненной как в покое, так и при пальпации, а в тканях ее определяется инфильтрат. Из анамнеза удается выяснить, что в первые дни заболевания температура тела была у таких больных высокой, у 368 хирургическая инфекция и гнойно-септическая хирургия многих определялись гиперемия кожи и выраженный отек молочной железы. Эти признаки воспалительного процесса купировались при назначении антибиотиков, но инфильтрат сохранял прежние размеры или постепенно увеличивался. При инфильтративно-абсцедирующем мастите, который встречается в 53,8% случаев, инфильтрат состоит из множества мелких гнойных полостей по типу "пчелиных сот" и симптом флюктуации определяется только у 4,3% больных. По этой же причине при диагностической пункции инфильтрата редко удается получить гной. Ее диагностическая ценность значительно повышается при "стертой" форме абсцедирующего мастита. Лечение Больные с гнойным маститом должны быть госпитализированы в стационар, где под наркозом выполняется операция. Основными принципами хирургического лечения острых гнойных лактационных маститов являются выбор рационального доступа к гнойному очагу, его радикальная хирургическая обработка, наложение дренажно-промывной системы, закрытие раны первичным швом, постоянное капельное промывание раны раствором антисептиков в послеоперационном периоде. При выборе доступа к гнойному очагу учитываются локализация и распространенность процесса, анатомические и функциональные особенности молочной железы. С нашей точки зрения, следует полностью отказаться от радиальных разрезов, при выполнении которых в верхних квадрантах остаются рубцы, недостаточно скрываемые одеждой, а в нижних часто возникает рубцовая деформация молочной железы. В зависимости от локализации процесса целесообразно выполнять следующие разрезы: параллельно и несколько отступя от края ареолы (при субареолярном мастите и локализации гнойника в верхневнутреннем квадранте); параллельно и на 2 см выше нижней переходной складки молочной железы (при локализации гнойника в нижних квадрантах); по ходу нижней переходной складки (при ретромаммарном мастите); дугообразно по наружному основанию молочной железы (при локализации процесса в наружных квадрантах). После выполнения разреза иссекают все нежизнеспособные гнойно-некротические ткани, что ускоряет купирование воспалительного процесса. Критерием полноценно выполненной некрэктомии является появление капиллярного кровотечения из здоровых тканей. Дополнительно гнойную полость промываем растворами антисептиков и вакуумируем электроотсосом. Далее накладываем дренажно-промывную систему, состоящую из разнокалиберных полихлорвиниловых трубок (микроирригатор и дренаж), имеющих боковые отверстия для орошения гнойной полости растворами антисептиков и оттока промывной жидкости. Микроирригатор проводим через верхний полюс полости, дренаж - через нижний. Положение трубок относительно друг друга может быть различным в зависимости от формы и локализации гнойной полости в молочной железе. Иссечение гнойно-некротической ткани и постоянное промывание полости в после- операционном периоде антисептиками позволяют закрыть рану первичным швом независимо от ее объема. На подкожную жировую клетчатку накладываем кетгутовые швы, на кожу -шелковые. В результате на месте имевшегося гнойного очага образуется замкнутая полость, которая сообщается с внешним пространством через дренажно-промывную систему. Развивающаяся грануляционная ткань, заполняя полость, сохраняет объем и форму молочной железы, что важно в эстетическом отношении. Противопоказанием к наложению первичных швов является наличие анаэробной инфекции и обширного дефекта кожи, из-за чего сблизить края раны не представляется возможным. Промывание полости растворами антисептиков начинаем с первых часов послеоперационного периода через систему для внутривенного переливания жидкостей со скоростью 15 капель в минуту. В общей сложности для осуществления адекватного промывного дренирования требуется не более 2— 3 л жидкости в сутки. Показанием к удалению дренажно-промывной системы являются купирование, воспалительного процесса, отсутствие в промывной жидкости гноя, фибрина и некротизирован-ных тканей, уменьшение объема полости до 5 мл. Швы снимаем на 8-9-е сутки после операции. После удаления ДПС в ранки, оставшиеся на месте стояния трубок, на 2—3 дня вводим резиновые полоски. Комплексное лечение гнойного мастита включает назначение антибиотиков и иммунокорректо-ров. При тяжелом течении гнойного воспалительного процесса проводим коррекцию метаболических и гемодинамических нарушений, детоксика-ционную терапию. Одна из важных задач послеоперационного периода - купирование лактостаза, который всегда сопровождает гнойный мастит. При мастите следует воздержаться от прикладывания ребенка и к больной, и к здоровой молочным железам. Естественное вскармливание можно продолжить только после купирования воспаления и при отрицательном посеве молока на микрофлору. Показаниями к прерыванию лактации являются тяжелое или затяжное течение воспалительного процесса в молочной железе, двухсторонний мастит, рецидивы заболевания, невозможность кормления ребенка молоком матери после ее выздоровления, настойчивое желание матери прекратить лактацию. Купирование лактации тугим бинтованием молочных желез крайне опасно, так как некоторое время еще продолжается продукция молока и всегда возникает лактостаз, а нарушение кровообращения в молочной железе способствует развитию тяжелых форм гнойного мастита. Купировать лактацию при мастите можно только после ликвидации лактостаза. Наиболее эффективными препаратами для прерывания лактации являются Parlodel (Швейцария) и Dostinex (США), которые ингибируют секрецию пролакти-на. Однако следует отметить, что Фармакологический государственный комитет Минздрава России рекомендовал применять парлодел для подавления лактации только при тяжелых септических маститах из-за возможного развития серьезных осложнений: инсульта, снижения остроты зрения, легоч- 369 ной эмболии и других, вплоть до летального исхода («Безопасность лекарств», бюллетень №1,1998 г., бюллетень № 1, 2000 г.). Парлодел назначают по половине таблетки (1,25 мг) два раза в сутки во время еды с обязательным постепенным уменьшением объема и частоты сцеживаний. С 5-х суток приема этого препарата сцеживание молочных желез следует сводить к минимуму. Курс лечения парлоделом составляет в среднем 12-15 дней. Хотим подчеркнуть, что мы на 80 случаев применения парлодела не наблюдали серьезных осложнений от приема препарата, кроме головокружения на фоне умеренного снижения АД у 5 пациентов. Достинекс, обладающий более длительным, чем парлодел, пролактин - снижающим действием (до 2-3 нед), назначают по половине таблетки (0,25мг) во время еды через каждые 12 ч в течение двух дней. Молочная железа тщательно сцеживается сразу после приема первой дозы препарата и еще раз - через 3 ч. В дальнейшем сцеживание молока выполняем в небольшом объеме только при необходимости (чрезмерная молокопродукция). При купировании лактации следует иметь в виду, что, с одной стороны, резкое прекращение сцеживания молочной железы при мастите может явиться причиной рецидива лактостаза, а с другой - сцеживание молока усиливает секрецию пролактина. Таким образом, терапия послеродового мастита должна быть комплексной, с учетом формы, распространенности и локализации воспалительного процесса, необходимости максимально сохранить внешний вид и функцию молочной железы. Профилактика мастита заключается в соблюдении санитарно-гигиенического режима в родильном доме, повышении иммунологической реактивности организма женщины, соблюдении личной гигиены во время беременности и в послеродовом периоде, правильном уходе за молочными железами, профилактике и своевременном лечении лактостаза и трещин сосков. Особому медицинскому наблюдению подлежат все первородящие женщины, а также имеющие анатомические нарушения молочной железы, родильницы с патологией беременности и родов. Литература
10. Чадаев А.П., Зверев АА Острый лактационный мастит // Рус. мед.жур, 2001, № 3-С 117-119.  370 370 |
