Метотрексат methotrexate 0,0025 по 1 т через 12 часов 1 раз неделю при ра
 Скачать 7.74 Mb. Скачать 7.74 Mb.
|
|
4. Пассивные эктопические ритмы. Пониженная активность СА-узла или полная блокада синусовых импульсов вследствие функционального или органического повреждения СА-узла вызывают включение в действие автоматич. центров II порядка (клетки водителей ритма предсердий, АВ–соединение), III порядка (система Гиса) и IV порядка (волокна Пуркинье, мускулатура желудочков). Автоматические центры II порядка вызывают неизмененные желудочковые комплексы (наджелудочковый тип), тогда как центры III и IV порядка генерируют расширенные и деформированные желудочковые комплексы (желудочкового, идиовентрикулярного типа). Замещающий характер имеют следующие нарушения ритма: предсердные, узловые, миграция водителя ритма по предсердиям, желудочковые (идиовентрикулярный ритм), выскакивающие сокращения. 5. Синоаурикулярная блокада (блокада выхода из СА–узла) – нарушение образования и/или проведения импульса от синусового узла к предсердиям. СА–блокада встречается у 0,16–2,4% людей, преимущественно у лиц старше 50–60 лет, чаще у женщин, чем у мужчин. 1,2,3 степени. 6. Остановка синусового узла (отказ синусового узла) – периодическая потеря синусовым узлом способности вырабатывать импульсы. Это приводит к выпадению возбуждения и сокращения предсердий и желудочков. На ЭКГ наблюдается длительная пауза, во время которой не регистрируются зубцы P, QRST и записывается изолиния. Пауза при остановке синусового узла не кратна одному интервалу RR (PP). 7. Остановка предсердий (асистолия предсердий, парциальная асистолия) – отсутствие возбуждения предсердий, которое наблюдается в течение одного или (чаще) большего числа сердечных циклов. Предсердная асистолия может сочетаться с асистолией желудочков, в таких случаях возникает полная асистолия сердца. Однако во время предсердной асистолии обычно начинают функционировать водители ритма II, III, IV порядка, которые вызывают возбуждение желудочков. Выделяют три основных варианта остановки предсердий:а) остановка предсердий вместе с отказом (остановкой) СА–узла; б) отсутствие электрической и механической активности (остановка) предсердий при сохранении автоматизма СА–узла, продолжающего контролировать возбуждение АВ– узла и желудочков. Такая картина наблюдается при выраженной гиперкалиемии (>9–10 мм/л), когда появляется правильный ритм с уширенными комплексами QRS без зубцов Р. Этот феномен получил название синовентрикулярного проведения; в) сохранение автоматизма СА–узла и электрической активности предсердий (зубцы Р) при отсутствии их сокращений. 8. Синдром брадикардии/тахикардии (синдром тахи/бради). При этом варианте происходит чередование редкого синусового или замещающего наджелудочкового ритма с приступами тахисистолии. Диагностика Проба Вальсальвы. Простейшие вагусные пробы с задержкой дыхания на глубоком вдохе (в том числе и проба Вальсальвы), проводимые изолированно или в сочетании с натуживанием, иногда позволяют выявить синусовые паузы, превышающие 2,5–3,0 с, которые необходимо диф. с паузами, обусловленными нарушениями АВ–проведения. Выявление таких пауз указывает на повышенную чувствительность синусового узла к вагусным влияниям. Если такие паузы сопровождаются клиникой, требуется проведение углубленного обследования пациента с целью определения тактики лечения. Массаж каротидного синуса - в физиологических условиях вызывает брадикардию и гипотонию вследствие раздражения блуждающего нерва и сосудистого регуляторного центра в продолговатом мозге. При сверхчувствительном каротидном синусе надавливание на него может вызывать синусовые паузы более 2,5–3,0 с, сопровожд. кратковременным расстройством сознания. Важно подчеркнуть, что синдром каротидного синуса может, с одной стороны, развиваться на фоне нормальной функции синусового узла, а с другой, – не исключает наличия СССУ. Тилт–тест (пассивная ортостатическая проба) рассматривается сегодня как «золотой стандарт» в обследовании пациентов с синкопальными состояниями неясной этиологии. Нагрузочное тестирование (велоэргометрия, тредмил–тест). Нагрузочное тестирование позволяет оценить способность синусового узла учащать ритм в соответствии с внутренним физиологическим хронотропным стимулом. Холтеровское мониторирование. Чередующееся появление бради. и тахиаритмий у больных с СССУ часто не обнаруживается на обычной электрокардиограмме в покое. Изучение функции синусового узла методом ЧПЭС. Показателем автоматической активности синусового узла является продолжительность синусовой паузы от момента прекращения стимуляции (последней артефакт электростимула) до начала первого самостоятельного зубца Р. Этот период времени называется временем восстановления функции синусового узла (ВВФСУ). В норме длительность этого периода не превышает 1500–1600 мс. Кроме ВВФСУ рассчитывается еще один показатель – корригированное время восстановления функции синусового узла (КВВФСУ), которое учитывает длительность показателя ВВФСУ по отношению к исходной частоте синусового ритма. Лечение СССУ Экстренную терапию собственно СССУ проводят в зависимости от его тяжести. В случаях асистолии, приступов МАС необходимы реанимационные мероприятия. Выраженная синусовая брадикардия, ухудшающая гемодинамику и/или провоцирующая тахиаритмии, требует назначения атропина 0,5–1,0 мл 0,1% раствора п/к до 4–6 р./сут., инфузии дофамина, добутамина или эуфиллина под контролем кардиомонитора. С профилактической целью м.б. установлен временный эндокардиальный стимулятор. Абсолютные показания к имплантации электрокардиостимулятора: 1. Приступы МАС в анамнезе (хотя бы однократно). 2. Выраженная брадикардия (менее 40 в мин.) и/или паузы более 3 с. 3. ВВФСУ более 3500 мс, КВВФСУ – более 2300 мс. 4. Наличие обусловленных брадикардией головокружений, пресинкопальных состояний, коронарной недостаточности, застойной сердечной недостаточности, высокая систолическая артериальная гипертензия – независимо от ЧСС. 5. СССУ с нарушениями ритма, требующими назначения антиаритмических препаратов, которое в условиях нарушенной проводимости невозможно. Вопрос 97. Фибрилляция предсердий. Понятие. Причины, варианты, клинико-ЭКГ-критерии, диагностика, терапия. ФП — несогласованное возбуждение отдельных волокон предсердий с частотой 350–600 в минуту вследствие процесса microreentry, который сопровождается выпадением механической систолы предсердий и приводит к неправильному и, как правило, частому ритму желудочков. КЛАССИФИКАЦИЯ Согласно принятой в 2001 г. клинической классификации ACC/AHA/ESC выделяют: •пароксизмальную ФП (длится не более 7 дней, спонтанно купируется); •персистирующую (устойчивую) ФП (длится более 7 сут, может быть купирована только с помощью медикаментозной или электрической кардиоверсии); •постоянную ФП, которая не поддаётся устранению. Выделяют также впервые возникшую и рецидивирующую ФП. Если эпизоды ФП любой формы повторяются, такой вариант аритмии называется рецидивирующим. ЭТИОЛОГИЯ Выделяют преходящие причины ФП, которые не приводят к развитию устойчивых форм (гипокалиемия, анемия, ТЭЛА, открытые операции на сердце), и действующие длительно (встречаются чаще, ведут к развитию всех форм ФП): •АГ (при наличии гипертрофии и диастолической дисфункции ЛЖ); •ИБС (имеют значение снижение сократительной и диастолической функции ЛЖ, митральная регургитация; первый пароксизм ФП может быть проявлением ИМ); •врождённые и приобретённые пороки сердца (особенно митральные; следует помнить о возможности активного ревмокардита); •кардиомиопатии (в первую очередь ДКМП); •амилоидоз (в том числе изолированное поражение предсердий в старческом возрасте); •гемохроматоз (ФП сочетается с АВ-блокадами, желудочковыми аритмиями); •мио- и перикардиты, в том числе хронические (ФП может быть единственным проявлением); в рамках диффузных болезней соединительной ткани; •инфекционный эндокардит (в том числе с иммунокомплексным миокардитом); •гипертиреоз, в том числе амиодарониндуцированный; гораздо реже — феохромоцитома; •алкогольная миокардиодистрофия (в том числе без дилатации камер сердца); •другие миокардиодистрофии: дисгормональная, лучевая, химиотерапевтическая и т.д.; •пролапс митрального клапана (непосредственную роль играет митральная регургитация); •хроническое лёгочное сердце; •опухоль сердца (миксома, ангиосаркома и др.); •«спортивное сердце»; •синдром сонного апноэ (имеют значение вагусный рефлекс, лёгочная и системная гипертензия, гипоксия), ожирение (возрастание ИМТ на 1 единицу приводит к увеличению относительного риска ФП на 4%); •синдром Вольфа–Паркинсона–Уайта (появление ФП — абс. показание к операции); •синдром Бругада. При отсутствии названных причин ФП расценивается как идиопатическая (частота около 10–30%). Эта форма распадается на различные патогенетические варианты: •катехоламинзависимая ФП (несколько чаще страдают женщины, ФП возникает днём, при физической и эмоциональной нагрузке, после употребления чая, кофе, алкоголя; ей могут предшествовать учащённое сердцебиение, экстрасистолия; сопровождается потливостью, внутренней дрожью, подъёмом АД, похолоданием конечностей, тошнотой; может заканчиваться учащённым мочеиспусканием); •вагусиндуцированная (чаще страдают мужчины среднего возраста, отмечена провоцирующая роль алкоголя, ФП возникает ночью на фоне брадикардии); нередки смешанные формы; •генетические формы ФП (дефекты генов белков калиевых каналов, коннексина 40); •ряд больных с идиопатической ФП не подпадает ни под одну из этих категорий. ПАТОГЕНЕЗ В основе ФП лежит процесс microreentry, возникающий при наличии критической мышечной массы и патологического субстрата (фиброз, воспаление, растяжение кардиомиоцитов), который сопровождается неоднородностью проведения импульса по предсердию; ФП приводит к дополнительному ремоделированию предсердий (изменения в экспрессии Са-каналов, межклеточных контактов, миолиз). Важным показателем готовности предсердия (преимущественно левого) к развитию и поддержанию ФП служит его величина (линейные размеры, объём). По мере формирования субстрата роль триггера (импульсации из устьев лёгочных вен, других зон) снижается. Отсутствие «предсердной добавки», тахикардия и аритмия ведут к снижению сердечного выброса, вторичной дилатации камер сердца, к тромбообразованию (преимущественно в ушке ЛП) с тромбоэмболиями в сосуды большого круга кровообращения, в том числе нормализационными (вскоре после трансформации ФП в синусовый ритм). КЛИНИЧЕСКАЯ КАРТИНА При пароксизмальной ФП больные жалуются на внезапные приступы учащённого неритмичного сердцебиения длительностью от нескольких минут до нескольких суток, одышку, боли в грудной клетке, головокружение, слабость, подъём или снижение АД, изредка —синкопе (вследствие выраженной тахи- или брадиаритмии либо паузы «на выходе» из приступа). Обстоятельства возникновения пароксизма позволяют отнести ФП к катехоламин- или вагусзависимому типу. Вагусными пробами ФП не купируется. При постоянной или персистирующей форме ФП неритмичное сердцебиение возникает или усиливается при нагрузках, обычно сопровождается одышкой, может восприниматься как перебои в работе сердца. В покое больной может полностью утрачивать ощущение аритмии и считать ритм нормальным, что затрудняет определение давности последнего эпизода ФП. Ведущие синдромы в клинике: •синдром сердечной недостаточности; •тромбоэмболический синдром (может стать первым проявлением ФП). ДИАГНОСТИКА В анамнезе обращают внимание на случаи ФП и заболеваний сердца у родственников, нарушения в гинеколог. сфере, совпадение сроков появления ФП с периодом климакса, перенесённой инфекцией, на хронические заболевания ЛОР-органов, щитовидной железы, эрозивно-язвенные заболевания ЖКТ, аллергические реакции. Учитывают давность возникновения первого эпизода ФП, предшествовавшие и сопутствующие нарушения ритма и проводимости, длительность предшествовавших пароксизмов, их циркадный ритм, переносимость и способы их купирования, электроимпульсная терапия в анамнезе, поддерживающая антиаритмическая и урежающая ритм терапия, приём антикоагулянтов и антиагрегантов, геморрагические и тромбоэмболические осложнения. При наличии на момент осмотра ФП её диагностируют с помощью пальпации пульса. Аускультация сердца позволяет точно определить ЧСС за минуту, выявить дефицит пульса (отражает гемодинамическую неэффективность ФП). Обращает на себя внимание меняющаяся громкость I тона. В периоды между пароксизмами ФП оценивают частоту синусового ритма, число экстрасистол. Показаны проведение общего анализа крови (Hb, лейкоциты, СОЭ), определение липидного спектра, маркёров воспаления, в том числе C-реактивного белка, сердечных тропонинов Т или I, антител к миокарду, кардиотропным вирусам, стрептококкам. Обязательно определение уровня гормонов щитовидной железы (тироксина) и тиреотропного гормона. Во время пароксизма или при постоянной форме ФП диагноз ставят с помощью стандартной ЭКГ по сочетанию следующих признаков: •отсутствие зубцов Р; •нерегулярный ритм желудочков (полностью различные между собой интервалы R–R); •волны фибрилляции ff (лучше всего различимы в отведении V1, но видны не всегда). По величине периода (обратного частоте) выделяют волны ff малых (0,12–0,14 с), средних (0,15–0,17 с) и крупных периодов (0,18 с и более), по амплитуде: крупные (≥2 мм), средние и мелкие (<1 мм), которые чаще всего свидетельствуют о неревматической этиологии ФП или выраженном фиброзе предсердий (чем чаще волны ff, тем хуже они проводятся через АВ-соединение). Выделяют бради- (<60 в минуту), нормо- (60–80 в минуту) и тахисистолический (>80 в минуту) варианты ФП, кот. часто меняют друг друга. ФП с выраженной, относительно ритмичной тахиаритмией (ЧСС 150–200 в минуту) характерна для алког. интоксикации, гипертиреоза, синдрома Вольфа–Паркинсона–Уайта. При развитии на фоне ФП полной АВ-блокады (синдром Фредерика) волны ff сочетаются с правильным желудочковым ритмом. Для идентификации волн ff можно использовать чреспищеводную запись ЭКГ. При подозрении на пароксизмальную ФП и при отсутствии ЭКГ, записанных во время приступа, проводят (до назначения антиаритмических средств) холтеровское мониторирование; ЭхоКГ (всем больным), чреспищеводную ЭхоКГ (исключение тромбоза предсердий), рентгенографию органов грудной клетки, спирографию, сцинтиграфию, нагрузочные тесты, КТ сердца (анатомия лёгочных вен), МРТ, КАГ (при наличии других симптомов ИБС), биопсию миокарда, сомнографию. Всем больным перед назначением антикоагулянтов/антиагрегантов проводят ФГДС. ЛЕЧЕНИЕ Во всех случаях, когда это возможно, следует стремиться к проведению этиотропного и патогенетического лечения. Существуют две принципиальные стратегии в лечении ФП: •стратегия контроля ритма: восстановление синусового ритма с последующей профилактикой рецидивов аритмии при помощи постоянной медикаментозной антиаритмической терапии или методов катетерной аблации; •стратегия контроля ЧСС: сохранение ФП (отказ от восстановления синусового ритма) с достижением адекватного урежения ЧСС и постоянной полноценной антикоагулянтной терапией. 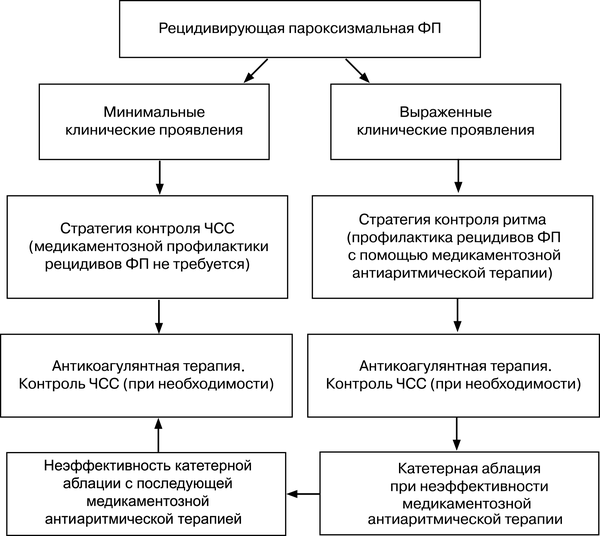 Рис. 18-3. Выбор тактики лечения при рецидивирующей пароксизмальной ФП  Рис. 18-4. Выбор тактики лечения при рецидивирующей персистирующей ФП При постоянной форме ФП единственной оптимальной тактикой лечения является тактика контроля ЧСС. При всех формах ФП необходимо проведение профилактики тромбоэмболических осложнений. ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ •впервые возникший пароксизм ФП; •пароксизмальная форма ФП длительностью менее 48 ч, не поддающаяся медикаментозной кардиоверсии на догоспитальном этапе; •пароксизмальная форма ФП длительностью менее 48 ч, сопровождающаяся выраженной тахисистолией желудочков (>150 в минуту), острыми расстройствами гемодинамики (артериальная гипотензия, сердечная астма, отёк лёгких) или выраженной коронарной недостаточностью (ангинозные боли, признаки ишемии миокарда на ЭКГ); •пароксизмальная форма ФП длительностью более 48 ч и персистирующая форма ФП вне зависимости от ЧСС, наличия либо отсутствия признаков острой левожелудочковой и коронарной недостаточности. Цель госпитализации - решение вопроса о целесообразности восстановления синусового ритма и подготовка к нему; •постоянная форма ФП, сопровождающаяся выраженной тахисистолией желудочков (>150 в минуту), острыми расстройствами гемодинамики (артериальная гипотензия, сердечная астма, отёк лёгких) или выраженной коронарной недостаточностью (ангинозные боли, признаки ишемии миокарда на ЭКГ). Цель - коррекция мед. терапии; •наличие тромбоэмболических и геморрагических осложнений. МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ Медикаментозное лечение пароксизмальной формы ФП Купирование пароксизма ФП. Выбор антиаритмического препарата зависит от характера основного заболевания, длительности существования ФП, наличия либо отсутствия признаков острой левожелудочковой и коронарной недостаточности. Для медикаментозной кардиоверсии могут использоваться либо антиаритмические препараты с доказанной эффективностью, относящиеся к I (флекаинид, пропафенон) или к III (дофетилид ибутилид, нибентан, амиодарон) классу, либо так называемые «менее эффективные или недостаточно изученные» антиаритмические препараты I класса (прокаинамин, хинидин). Нельзя использовать сердечные гликозиды и соталол. Если пароксизм ФП длится менее 48 ч, то его купирование можно осуществлять без полноценной антикоагулянтной подготовки, однако оправдано введение либо нефракционированного гепарина 4000–5000 ЕД внутривенно, либо низкомолекулярных гепаринов (надропарина кальция 0,6 или эноксапарина натрия 0,4 п/к). Если пароксизм ФП длится более 48 ч, то риск развития тромбоэмболических осложнений резко возрастает; в этом случае перед восстанавлением синусового ритма необходимо начать полноценную антикоагулянтную терапию (варфарин). При этом необходимо учитывать, что ФП может закончиться спонтанно (пароксизмальная форма) намного раньше, чем с помощью варфарина удастся достичь терапевтического значения МНО, равного 2,0–3,0. В таких случаях перед восстановлением синусового ритма наиболее целесообразно начинать одновременную терапию варфарином и НМГ (надропарин, эноксапарин в дозе 0,1 мг/кг каждые 12 ч). Тяжёлые нарушения гемодинамики (шок, коллапс, стенокардия, отёк лёгких) во время пароксизма ФП требуют немедленного проведения электроимпульсной терапии. При непереносимости или многократной неэффективности (в анамнезе) антиаритмических препаратов купирование пароксизма также проводят с помощью электроимпульсной терапии. •Прокаинамид (новокаинамид) вводят внутривенно струйно медленно в дозе 1000 мг в течение 8–10 мин (10 мл 10% раствора, разведённые до 20 мл изотоническим раствором хлорида натрия) или внутривенно капельно (при наличии тенденции к артериальной гипотензии, при первом введении) под постоянным контролем АД, ЧСС и ЭКГ. В момент восстановления синусового ритма введение препарата прекращают. В связи с возможностью снижения АД его нужно вводить в горизонтальном положении больного, имея рядом приготовленный шприц с 0,3–0,5 мл 1% раствора фенилэфрина (мезатона). Эффективность прокаинамида в отношении купирования пароксизмальной формы ФП в первые 30–60 мин после введения относительно невысока и составляет 40–50%. Повторное введение в дозе 500–1000 мг возможно только в условиях стационара. Одним из редких, но потенциально опасных для жизни побочных эффектов применения прокаинамида м.б. трансформация ФП в трепетание предсердий с высоким коэффициентом проведения на желудочки сердца и развитием аритмогенного коллапса. К побочным эффектам прокаинамида относят аритмогенное действие, желудочковые нарушения ритма вследствие удлиннения интервала Q–T; замедление атриовентрикулярной проводимости, внутрижелудочковой проводимости (возникают чаще в повреждённом миокарде, проявляются на ЭКГ уширением желудочковых комплексов и блокадами ножек пучка Гиса); артериальная гипотензия (вследствие снижения силы сердечных сокращений и вазодилатирующего действия); головокружение, слабость, нарушение сознания, депрессия, бред, галлюцинации; аллергические реакции. Противопоказания к применению прокаинамида: артериальная гипотензия, кардиогенный шок, ХСН; синоатриальная и АВ-блокады II и III степени, внутрижелудочковые нарушения проводимости; удлинение интервала Q–Т и указания на эпизоды пируэтной тахикардии в анамнезе; выраженная почечная недостаточность; системная красная волчанка; повышенная чувствительность к препарату. •Нибентан, отечественный антиаритмический препарат III класса, существует только в форме раствора. Вводят внутривенно капельно или струйно медленно в дозе 0,125 мг/кг (10–15 мг) под постоянным мониторным контролем ЭКГ, который проводят не менее 4–6 ч после окончания введения препарата и продлевают до 8 ч при возникновении желудочковых аритмий. При неэффективности первого введения нибентана возможно повторное введение препарата через 20 мин в той же дозе. Эффективность нибентана в отношении купирования пароксизмальной формы ФП в первые 30–60 мин после введения составляет около 80%. Поскольку вероятно развитие таких серьёзных проаритмических эффектов, как полиморфная ЖТ типа «пируэт», применение нибентана возможно только в стац., в условиях блоков интенсивного наблюдения и отд. кардиореанимации. •Амиодарон, если учитывать особенности его фармакодинамики, не может быть рекомендован как средство быстрого восстановления синусового ритма у больных с пароксизмальной формой ФП. Максимальный его эффект развивается через 2–6 ч. С целью купирования пароксизмальной формы ФП амиодарон сначала вводят в виде болюса внутривенно из расчёта 5 мг/кг, а затем продолжают вводить капельно в дозе 50 мг/ч. При такой схеме введения амиодарона у 70–80% больных с пароксизмальной формой ФП в течение первых 8–12 ч восстанавливается синусовый ритм. •Пропафенон (в/в введение 2 мг/кг в течение 5 мин, при необходимости — повторное введение половины исходной дозы через 6–8 ч). У ряда больных без серьёзных органических поражений сердца одномоментный приём 300–450 мг пропафенона внутрь может успешно применяться для самостоятельного купирования пароксизма ФП в амбулаторных условиях. Но прежде чем рекомендовать больному этот способ устранения ФП, эффективность и безопасность его должны быть неоднократно проверены в стационарных условиях. •Хинидин 0,2 (пролонг. форма) по 1 таблетке один раз в 6–8 ч, в сумме не более 0,6 в сутки. При синдр. предвозбуждения желудочков, при острых формах ИБС, тяж. поражении миокарда желудочков (гипертрофия ≥14 мм, ФВ <30%) медикаментозное купирование МА проводят с помощью амиодарона или прокаинамида. Чреспищеводная стимуляция сердца для купирования ФП неэффективна. После успешного купирования пароксизмальной формы ФП необходимо начать или скорригировать профилактическую антиаритмическую терапию. После первого пароксизма ФП длительность медикаментозной терапии может составлять 1,5–2 мес, при рецидивирующих эпизодах ФП в большинстве случаев медикаментозная терапия должна быть постоянной. Профилактическую антиаритмическую терапию при пароксизмальной ФП проводят во всех случаях, за исключением: •редких (один раз в несколько месяцев или лет), хорошо переносимых приступов, которые легко купируются в пределах 2 сут; •при неэффективности или непереносимости всех антиаритмических средств и их комбинаций; •при наличии противопоказаний к приёму антиаритмических средств (СССУ с брадикардией менее 50 уд/мин, паузами более 3 с, увеличение P–Q до 0,24 с и более, АВ-блокада II степени 2-го типа или III степени) либо возникновении этих нарушений на фоне терапии; последней категории больных показана имплантация ЭКС с последующим назначением антиаритмических препаратов. Из применяемых в России с целью профилактики рецидивов ФП антиаритмических средств наиболее эффективными считают препараты IA класса (хинидин, дизопирамид), IC класса (этацизин, этмозин, пропафенон, аллапинин) и III класса (амиодарон, соталол). В качестве профилактической антиаритмической терапии при ФП применяют: •хинидин 0,2 г (ретардная форма) по 1 таблетке 2–3 раза в сутки; •дизопирамид 0,1 г по 1 таблетке 3–4 раза в сутки; •пропафенон 0,15 г по 1 таблетке 3–4 раза в сутки или по 2 таблетки 3 раза в сутки; •этацизин 0,05 г по 1/2–1 таблетке 3–4 раза в сутки; •аллапинин 0,025 г по 1/2–1 таблетке 3–4 раза в сутки; •соталол 0,08–0,32 г в сутки (на 2 или 3 приёма); •амиодарон в поддерживающей дозе 0,2–0,4 г в сутки. При тенденции к брадикардии предпочтительно назнач. Преп. с холинолитическим (хинидин, дизопирамид) или симпатомиметическим (аллапинин) действием. После первого в жизни приступа ФП в качестве профилактической антиаритмической терапии можно назначать β-адреноблокаторы или блокатор кальциевых каналов верапамил. Если эпизоды ФП продолжают возникать, переходят на антиаритмические средства IA, IC или III класса. В целях безопасности после назначения нового антиаритмического препарата контроль ЭКГ в течение первых 10 дней проводят не реже одного раза в 3–5 дней. Наиболее важный показатель возможной аритмогенности — удлиннение интервала Q–Tc >450 мс или увеличение его более чем на 25% от первоначального значения. При неэффективности антиаритмических препаратов и при сохраняющихся частых, плохо переносимых пароксизмах ФП следует рассматривать вопрос о проведении радиочастотной аблации. При отсутствии эффекта от радиочастотной катетерной аблации показано назначение урежающей ритм терапии (дигоксин 0,125–0,25 мг/сут с β-блокатором) для уменьшения тахисистолии во время пароксизма в сочетании с антикоагулянтами/аспирином. |
