Лабораторный-практикум-по-технологии-сахара. Практикум по технологии сахара утверждено научнометодическим советом итпм 28 декабря 2002 года
 Скачать 0.79 Mb. Скачать 0.79 Mb.
|
ВведениеПолная (общая) обменная емкость катионита определяется при нейтрализации раствором NaOH или КОН в статических или динамических условиях и выражается в эквивалентах на 1 г сухого или 1 дм3 набухшего катионита. Реакции обмена катионов (К- катионит) имеют вид: Вещества, не диссоциирующие в растворах, адсорбируются ионитами, как на активном угле, по законам молекулярной адсорбции. Полная обменная емкость различных марок сильнокислотных катионитов, применяемых в сахарной промышленности, колеблется от 4 до 6 мг-экв/г. Например, отечественный катионит КУ-2-8/Н, Na ионная форма/ имеет полную обменную емкость 5,1 /Н/мг-экв/г. Цель анализа- оценить качество и пригодность катионита для очистки сахарных растворов. Принцип метода анализа основан на титровании образовавшейся в результате реакции ионного обмена кислоты Реактивы: - 5%-ный раствор NaCl; - 0,1 н. раствор NaOH; Индикатор - метилоранж. Приборы и материалы: - стеклянная колонка диаметром 18 мм, высотой 250см с оттянутым концом; - капельная воронка; - мерная колба вместимостью 200 см3; - мерный цилиндр вместимостью 100 см3; - бюретка для титрования; - химический стакан; - катионообменная смола. Ход определения5 г приготовленного для анализа катионита в Н-форме переводят в стеклянную колонку диаметром 18 мм с помощью дистиллированной воды, избыток воды спускают через резиновую трубку с зажимом, одетую на оттянутый конец нижней части колонки. Для предотвращения уноса катионита на стеклянную решетку колонки помещают тампон из стеклянной ваты. После этого из капельной воронки, установленной над колонкой с катионом, в течение 30 мин равномерно пропускают 100 см3 5%-ного раствора химически чистого NaCl, поддерживая уровень раствора над слоем катионита равным 1 см. Затем катионит промывают двойным по его объему количеством воды. Фильтрат и промывные воды собирают в мерную колбу, где доводят их объем до 200 см3. Из этого объема отбирают 50 см3 в отдельный стакан и титруют 0,1н. раствором NaОН в присутствии метилоранжа как индикатора. Расчеты:1. Для получения сравнимых результатов обменную емкость катионита выражают через миллиграмм-эквивалент ионов / или число активных групп/, приходящихся на 1 г сухого ионита. Поэтому, если расход 0,1н. раствора NaOH для нейтрализации кислоты, выделенной 1 г абсолютно сухого катионита, можно выразить формулой 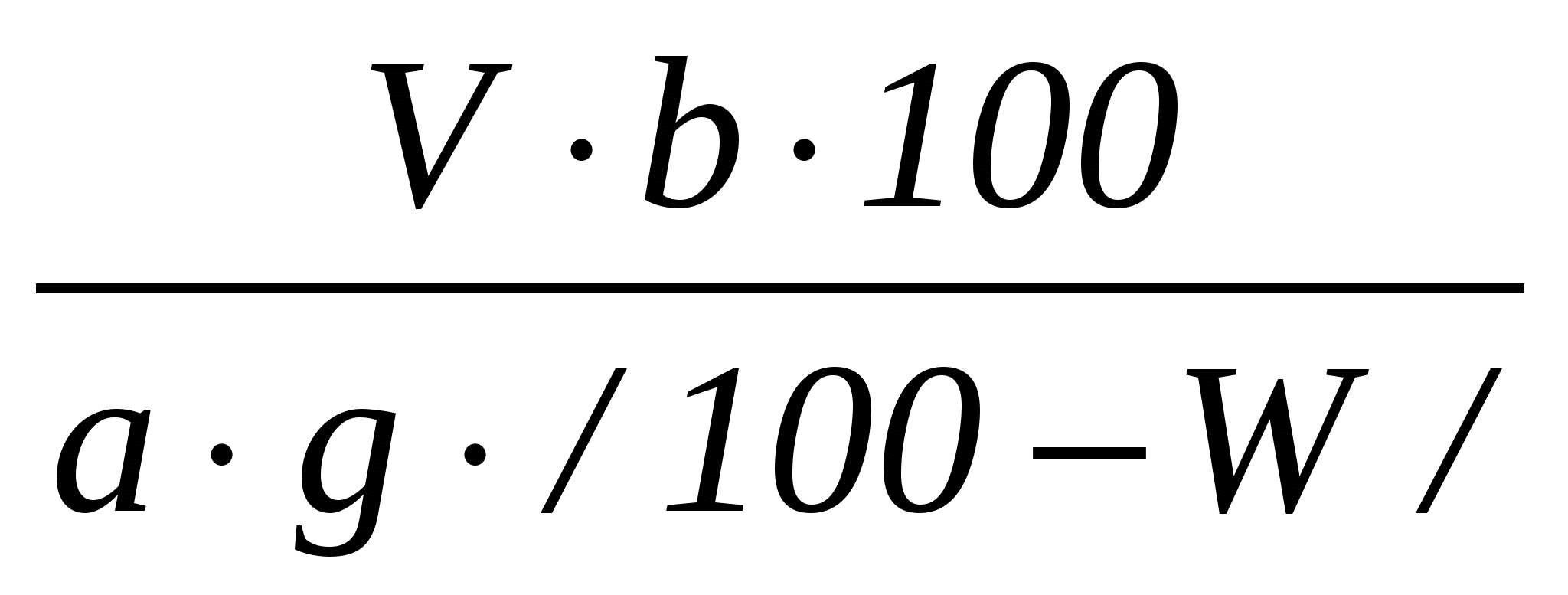 , ,а в 1 см3 1 н. раствора NaОН содержится 0,1 мг-экв, то полная обменная емкость катионита может быть рассчитана из формулы 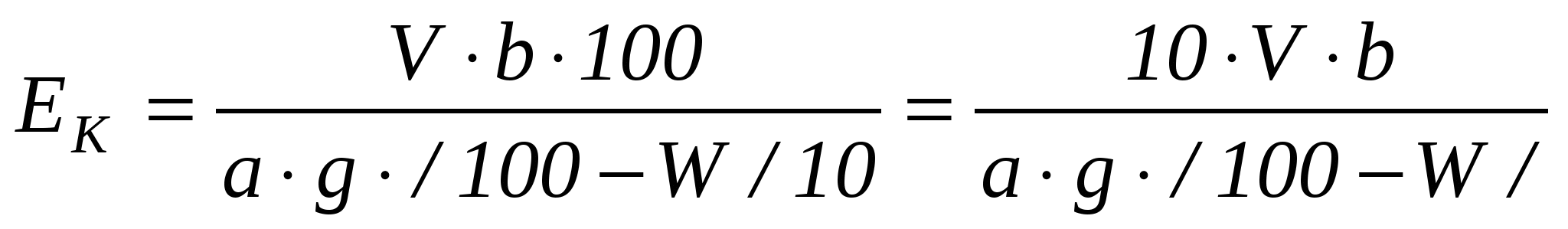 , ,где Ек - полная обменная емкость, в мг-экв/г абсолютно сухого катионита; b - общее количество фильтрата, см3; V - количество 0,1 н. раствора NaOH, пошедшее на титрование фильтрата, см3; a– количество фильтрата, отобранного для титрования, см3; g– количество сухогого катионита, взятого для определения его полной обменной емкости, г; W – влажность катионита, %. Определяют методом высушивания в течение 3-х часов при температуре 95-100ºС. 2. Обменную емкость катионита можно выразить также по натрию. В этом случае расчет ведется по формуле  или, так как 1 см3 0,1 н. раствора NaОН содержит 0,0023 г натрия, то или, так как 1 см3 0,1 н. раствора NaОН содержит 0,0023 г натрия, то 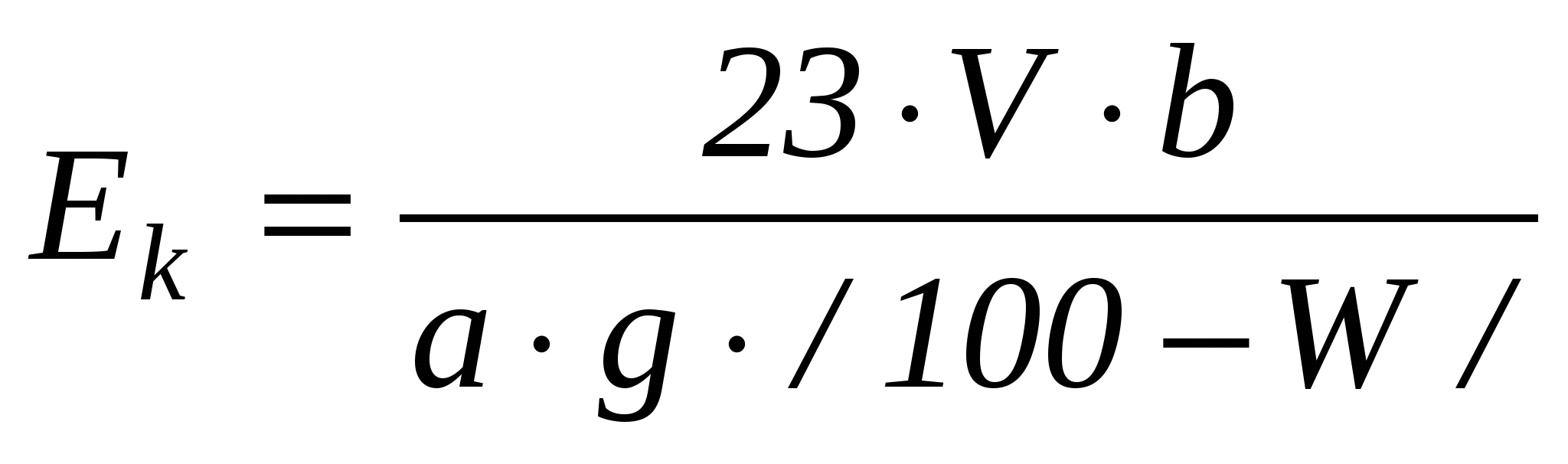 . .6.2. Определение полной обменной емкости анионитаВведениеПолная обменная емкость анионита определяется при его нейтрализации раствором HCl или H2SO4 в статических или динамических условиях и выражается в эквивалентах на 1г сухого или набухшего анионита. Реакции обмена анионов / А-анионит/ имеют вид: А. /OH/ A. /OH/ Помимо обменной емкости к основным показателям пригодности анионита относят: обесцвечивающую способность, степень набухания, способность к старению, нерастворимость в воде и органических растворителях, простоту регенерации, термическую и механическую прочность. Полная обменная емкость различных марок анионитов, используемых в сахарной промышленности, может быть 1 - 10 мг-экв/г. Применяемый для обесцвечивания сахарных растворов отечественный макропористый анионит АВ-17-2П имеет полную обменную емкость по 0,1 н. раствору HCl 3,8 мг-экв/г, а по 0,1 н. раствору NaCl 3,4 мг-экв/г. Цель анализа - оценить качество анионита для обесцвечивания сахарных растворов. Принцип метода анализа основан на титровании непоглощенного анионитом раствора кислоты 0,1 н. раствором NaOH. Реактивы: - 0,1 н. растворы HCl и NaOH. Приборы и материалы: - стеклянная колонка диаметром 18 мм, высотой 250 мм с оттянутым в нижней части концом, на который надевают резиновую трубку с винтовым зажимом; - стеклянная воронка; - мерная колба на 500 см3; - бюретка для титрования; - химический стакан; - анионообменная смола. |
