РУКОВОДСТВО ПО ОБЩЕЙ ХИРУРГИИ. Руководство по общей хирургии Учебное пособие. М. Оао Издательство Медицина
 Скачать 9.28 Mb. Скачать 9.28 Mb.
|
|
Часть из них (фактор некроза опухолей-альфа, фактор активации тромбоцитов, тромбоксан) в значительной степени ответственны за развитие синдрома внутрисо-судистого диссеминированного свертывания, другие (ИЛ-1, лейкотриены, эндоте-лиальный фактор релаксации, эндотелии-1, тромбоксан А2, интерферон-у) способствуют повышению проницаемости сосудистой стенки при сепсисе. Нарушение функции эндотелия является центральным звеном распространения системного воспаления за границы сосудистого русла и его неблагоприятного действия на печень, почки, легкие, центральную нервную систему. Вслед за повреждением эндотелия нарушается метаболическая активность клеток этих и других органов, проявляющаяся снижением тонуса сосудов, нарушением режима микроциркуляции — признаками полиорганной недостаточности. Иммунная система организма, помимо различных активирующих цито-кинов, способна продуцировать и их инактиваторы, противовоспалительные агенты (ИЛ-4,10,13, ИЛ-1 и ИЛ-2 растворимый рецептор, белки, связывающие липополисахариды, трансформирующий фактор роста-р\ адреналин, ФНО-а растворимый рецептор, антагонист рецептора лейкотриена В4, белок «теплового шока»). В случае нормального течения инфекционного процесса достигается равновесие активности провоспалительных и противовоспалительных цито-кинов. Разбалансированный иммунный ответ может проявляться активацией про-и противовоспалительных агентов и постоянными их колебаниями, что клинически обычно соответствует фазе синдрома полиорганной недостаточности. Длительно существующие нарушения иммунных реакций обусловливают постепенный переход сепсиса в форму под острого и далее хронического. Клиническая картина сепсиса в большой степени обусловлена характером резистентности организма больного, выраженностью ответной реакции на внедрение и распространение микроорганизмов, их количеством и вирулентностью. Классические проявления системной воспалительной реакции, составляющие симптомокомплекс сепсиса (лихорадка, тахикардия, одышка и лейкоцитоз), недостаточно чувствительны и специфичны для точной диагностики. Клиническая картина, подобная сепсису, нередко наблюдается у пациентов со стерильными формами панкреонекроза, тяжелой травмой, ожога- 496 (^pg!2^2Ј^ 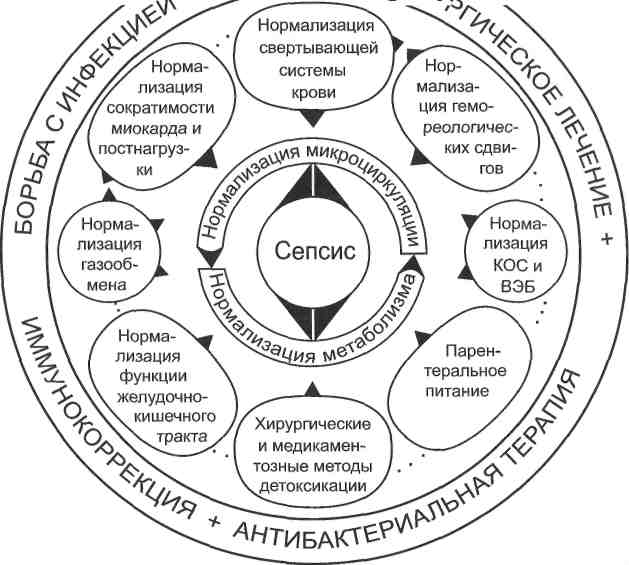 Рис. 17.21. Основные компоненты интенсивной терапии сепсиса. ми, лекарственной реакцией, после обширных хирургических вмешательств и даже при тяжелой сердечной недостаточности. Одним из наиболее частых симптомов, присущих сепсису, является изменение терморегуляции в сторону гипертермии (чаще всего) или гипотермии (реже). Повышение температуры тела вызывают пирогенные цитокины (прямое и опосредованное действие на гипоталамус), которые выделяют в кровь преимущественно моноциты и макрофаги в ответ на внедрение инфекции. Наиболее типична для сепсиса нестабильная гипертермия в течение суток: характерны внезапные кратковременные подъемы температуры тела один или несколько раз в течение суток с последующим литическим снижением, проливными потами, слабостью, тахикардией и одышкой. Озноб свидетельствует о массивной инвазии тканевых и микробных антигенов. Данный период является наиболее благоприятным для диагностического посева крови на гемокультуру. Прогностически неблагоприятным признаком является неожиданное снижение температуры тела у таких больных до нормы (или даже ниже нормы) при отсутствии положительной динамики общего состояния. Бактериемия и сепсис. Бактериемия — присутствие микроорганизма в системном кровотоке — не является обязательным проявлением сепсиса. Обнаружение микроорганизмов у лиц без клинико-лабораторных подтверждений синдрома системного воспалительного ответа, но при наличии 497 факторов риска должно расцениваться не как сепсис, а как транзиторная бактериемия. Ее возникновение описано после лечебных и диагностических манипуляций, таких как бронхо- и фиброгастроскопия, колоноско-пия, стоматологические манипуляции. Даже при самом скрупулезном соблюдении техники забора крови и использовании современных технологий идентификации микроорганизмов частота положительных результатов при посевах крови не превышает 55 %. Традиционным методом диагностики сепсиса является посев крови, при этом частота выделения гемокультуры существенно варьирует (от 22,5 до 87,5 %) и в значительной степени зависит от методики исследования. Лечение хирургического сепсиса, основу которого составляет гнойный очаг, инициирующий генерализованную инфекцию, должно быть комбинированным (рис. 17.21). Хирургическая санация — прекращение поступления микроорганизмов из очага инфекции посредством вскрытия очага с удалением гноя и некроти-зированных тканей, а также адекватного дренирования гнойной полости, занимает ведущее место. 17.8.2. Приоритетные методы интенсивной терапии сепсиса Рациональный выбор режима антибактериальной терапии сепсиса определяется локализацией источника (очага) инфекции и условиями возникновения инфекции (внебольничная или госпитальная). Если есть основания предположить внебольничный характер инфекции, то препаратами выбора могут быть целофалоспорины III поколения (цефотаксим, цефтриак-сон). Допустимо также использование цефалоспоринов II поколения или защищенных пенициллинов в комбинации с аминогликозидами. Инфузионная терапия при сепсисе способствует восстановлению адекватной тканевой и органной перфузии, повышению потребления кислорода тканями, коррекции гомеостатических расстройств, снижению концентрации токсических субстанций и медиаторов септического каскада. Инфузионная программа зависит от степени гиповолемии, фазы ДВС-синдрома, уровня альбумина крови, тяжести респираторного дистресс-синдрома. Плазмозаменители (декстраны, желатиноль, гидроксиэтиламидоны) показаны при выраженном дефиците ОЦК, сочетающемся с артериальной гипотензией. Переливание альбумина имеет преимущество перед искусственными плазмозаменителями при уровне альбумина менее 25—30 г/л. Применение криоплазмы (15 мл/кг массы) показано при дефиците антитромбина III (AT III) или плазменных факторов коагуляции. Восстановлению адекватной тканевой и органной перфузии способствуют инфузионно-трансфузионная терапия в режиме гемодилюции и использование гепарина (10—20 тыс. ЕД/сут внутривенно), трентала — 10—20 мл/сут. При сердечной недостаточности начинают инфузию добутрекса (5— 7,5 мкг/кг/мин) или допамина (5—10 мкг/кг/мин). При развитии септического шокового синдрома показано введение адреналина (0,05—0,1 мкг/кг/мин). Адекватная и своевременная респираторная поддержка — один из главных моментов лечения сепсиса. Для купирования респираторного дистресс-синдрома используют механическую вентиляцию легких, кортикостероиды, му-колитические средства, синтетические и естественные сурфактанты. При тяжелом течении сепсиса наблюдается развитие вторичного иммунодефицита, наиболее типичного для хирургической инфекции. Направленная иммунокоррекция проводится в соответствии с выявленным дефек- том конкретного звена иммунитета — заместительная (взвесь лейкоцитов, интерферон, гипериммунная антистафилококковая плазма, иммуноглобулины для внутривенного введения и др.), иммуностимулирующая (стафилококковый анатоксин, тималин и др.) терапия. Ингибиторы свободных радикалов показаны в силу активации при сепсисе процессов свободнорадикального окисления и развития дисбаланса в системе перекисного окисления липидов — антиоксидантной системы, усиливающего структурные органные повреждения. Наибольшее увеличение скорости свободнорадикального окисления наблюдается при сепсисе, сочетающемся с респираторным дистресс-синдромом. Для повышения антиокислительного потенциала к терапии добавляют унитиол, витамин С, токоферол, синтетические антиоксиданты (эмоксипин, мексидол и др.). Современные методы лечения сепсиса предусматривают цитокиновую терапию [ронколейкин (ИЛ-2), беталейкин (ИЛ-ip), рекомбинантный гра-нулоцитарно-макрофагальный колониестимулирующий фактор и др.)]. Восстановление функции печени осуществляют внутрипортальной оксиге-нацией, введением эссенциальных фосфолипидов, даларгина, трансплантации изолированных гепатоцитов. Тяжелый сепсис, как правило, сопровождается проявлениями гиперметаболизма. В этой ситуации покрытие энергетических потребностей происходит за счет деструкции собственных клеточных структур («аутоканниба-лизм»), что усугубляет органную дисфункцию и усиливает эндотоксикоз. Поэтому проведение искусственной питательной поддержки является очень важным компонентом лечения. Оптимальное суточное потребление энергии — 30—35 ккал/кг. Назначают энтеральное питание специальными смесями, которые сбалансированы по основным питательным компонентам, высококалорийны, содержат добавки микроэлементов и витаминов. Энтеральное питание предупреждает транслокацию микрофлоры из кишечника, развитие дисбактериоза, повышает функциональную активность энтероци-та и защитные свойства слизистой оболочки, снижая степень эндотоксико-за и риск возникновения вторичных инфекционных осложнений. Наиболее эффективными методами детоксикации при сепсисе являются экстракорпоральные — обменный плазмаферез, перфузия крови через свиную селезенку, плазмосорбция. 17.8.3. Клинические формы хирургического сепсиса Клинические формы хирургического сепсиса вариабильны. Абдоминальный сепсис является системной воспалительной реакцией организма в ответ на развитие первоначально деструктивного процесса в органах брюшной полости и/или забрюшинного пространства. Основу абдоминального сепсиса в подавляющем числе случаев составляет распространенный перитонит на почве деструктивных процессов или перфораций органов брюшной полости, а также в результате закрытой травмы и ранений живота, реже — послеоперационный. Основную роль играет неэффективная хирургическая санация гнойно-воспалительного очага в брюшной полости, продолжающийся перитонит или несвоевременное хирургическое и интенсивное лечение (позднее поступление больных в стационар). Схема комплексного лечения абдоминального сепсиса предусматривает воздействие на все звенья его патогенеза. После поступления больных в стационар проводят экстренную адекватную предоперационную подготовку 499 до стабилизации гемодинамики, уменьшения сгущения крови, разгрузки верхних отделов желудочно-кишечного тракта. Через 2—4 ч выполняют экстренную хирургическую операцию, направленную на удаление источника перитонита и тщательную санацию брюшной полости. Важная роль в лечении абдоминального сепсиса отводится рациональной интенсивной терапии, основные принципы которой изложены в начале настоящей главы. Сепсис с локализацией первичного очага в сосудистом русле (катетериза-ционный сепсис) возникает, если патогенные возбудители генерализованной инфекции и их токсины поступают в кровоток, минуя биологические барьеры организма. Проблема ангиогенного сепсиса в хирургии обусловлена широким внедрением в клиническую практику различных инвазивных методов диагностики и лечения заболеваний. Нарушение целости сосудистой стенки инструментами из синтетических материалов (катетеры, сосудистые трансплантаты, сердечные клапаны) повысило риск развития генерализованной инфекции. 17.9. Специфическая хирургическая инфекция 17.9.1. Столбняк Столбняк (tetanus) — раневая инфекционная болезнь, вызываемая токсином анаэробной спороносной палочки Clostridium tetani при ее проникновении в организм через дефект кожи или слизистой оболочки, характеризующаяся поражением нервной системы, приступами тонических и тетани-ческих судорог, гипоксией и сердечно-легочной недостаточностью. Заболеваемость столбняком во всем мире сохраняется на достаточно высоком уровне, несмотря на широкий охват населения вакцинопрофилакти-кой. Частота осложнений ран столбняком составляет 0,6—0,7 на 1 тыс. ранений. Летальность составляет 25—50 % среди больных молодого возраста и 70—80 % среди лиц пожилого возраста. Возбудитель столбняка cl. tetani — строго анаэробный, спорообразую-щий, грамположительный микроб. Споры его высокоустойчивы, они могут выжить при кипячении и сухом нагревании до 150 °С в течение 1 ч; в обычных условиях сохраняются десятилетиями. Входными воротами для столбняка могут служить любые, даже самые незначительные раны. В военное время это, как правило, огнестрельные раны, а в мирное — микротравмы, особенно содержащие инородные тела. Распространяется столбнячный токсин из места его образования или введения несколькими путями: по окружающим тканям, по лимфатической и кровяной системе, по нервным стволам. При распространении столбнячного токсина по регионарному невральному пути возникает относительно локальное поражение соответствующих нервных центров, которое проявляется развитием местного столбняка соответствующих мышц. Если количество столбнячного токсина значительно, он может далее распространяться по спинному мозгу в восходящем направлении, охватывая новые нервные центры (восходящий столбняк). При поступлении столбнячного токсина первоначально в кровь он разносится по всему организму (гематогенный путь распространения), попадает в мышцы и затем по двигательным нервам, составляющим общий невральный путь, достигает различных двигательных центров. Время поступления его в центры находится в прямой за- 500 висимости от длины каждого нерва. Поэтому вначале столбнячный токсин достигает двигательных центров мимических и жевательных мышц, затем мышц шеи, спины, а на более поздних этапах поражаются центры мышц рук и ног. Нисходящее движение столбнячного токсина имеет место в том случае, когда возникает депо столбнячного токсина в верхних отделах спинного мозга (при лицевом столбняке). При генерализованном процесе в последнюю очередь вовлекаются дыхательные мышцы, в частности диафрагма. Клиническая картина. Поражение вегетативных центров проявляется в виде проливного пота, гиперпирексии, тахикардии, наклонности к гипо-тензии. Меньшую роль играет прямое патологическое влияние токсина на сердце, легкие, кровь, печень. Лимфатические узлы при столбняке могут выполнять роль временных резервуаров столбнячного экзотоксина. Различают общую и местную форму столбняка. Последняя встречается редко и сопровождается длительной ригидностью конечности, на которой имеется рана. Такая форма заболевания не опасна для жизни, так как судороги самостоятельно ликвидируются на фоне лечения раны. Типичной местной разновидностью является лицевой столбняк Розе, при котором наряду с тризмом на пораженной стороне развивается паралич мышц лица, нередко и мышц глазного яблока, а на противоположной стороне обычно отмечается напряжение мышц лица и сужение глазной щели. Однако местные формы столбняка могут привести и к летальному исходу из-за развития ларингоспазма. Классическое описание клинической картины столбняка было дано еще Гиппократом, сын которого умер от этой грозной инфекции. Болезнь всегда проявляется триадой симптомов: тризмом, дисфагией и ригидностью затылочных мышц. Наиболее ранним и имеющим особое диагностическое значение симптомом столбняка является тризм — тоническое сокращение жевательных мышц. В начале заболевания тризм проявляется умеренным затруднением при жевании и открывании рта, а затем прогрессирует вплоть до полной невозможности разомнуть зубы. При этом отмечаются боли в горле и расстройства глотания. Для клинической картины столбняка также характерна сардоническая улыбка, возникающая вследствие тонического сокращения мимических мышц и придающая лицу своеобразное выражение одновременно улыбки и плача. К тризму и дисфагии последовательно в нисходящем порядке присоединяются «тянущие» боли и ригидность затылочных мышц, которая распространяется на длинные мышцы спины, поясницы, передней брюшной стенки и проксимальных отделов конечностей. Судороги вначале проявляются в виде спастической ригидности, распространяющейся сверху вниз и постепенно захватывающей мышцы туловища и нижних конечностей. На фоне тонического гипертонуса возникают приступы болезненных клонических судорог, провоцируемых любыми, даже незначительными раздражителями (свет, звук, прикосновение). Быстрое нарастание клинических симптомов столбняка свидетельствует о глубокой степени интоксикации организма и тяжести заболевания. А При столбняке I степени тяжести продолжительность инкубационного периода составляет 3 нед, начального — 5 сут и более, а средние сроки обращения больных за медицинской помощью — 5—7 дней заболевания. Судорожный синдром в основном проявляется в виде умеренного гиперто- 501 нуса мышц спины, брюшного пресса. Непостоянные легкие клонические судороги не вызывают расстройств дыхания. Больные полностью сохраняют способность жевать и проглатывать пищу. Все симптомы самостоятельно исчезают за 2—3 нед. А Инкубационный период при столбняке II степени тяжести составляет 2 нед, начальный — 4 сут и более, больных госпитализируют на 4—5-й день заболевания. Клиническая картина либо вовсе не нарастает, либо прогрессирует очень медленно. Мышечный гипертонус выражен умеренно, редкие клонические судороги практически не сопровождаются нарушением дыхания. Жевание и глотание пищи затруднены в значительной степени. Общая продолжительность болезни не превышает 3 нед. Л При столбняке IIIстепени тяжести инкубационный период колеблется от 9 до 15 сут, начальный период составляет 3—4 сут, а больных обычно госпитализируют на 2—3-й день заболевания. Уже при поступлении возможны сильные приступы клонико-тонических судорог с опасными расстройствами дыхания. Поэтому врач, принимающий больного, должен быть готов к оказанию помощи при внезапном приступе апноэтического криза. Частота и сила судорог прогрессируют очень быстро, буквально по часам. Температура тела часто поднимается до 39 °С и выше, хотя может быть и субфебрильной. Пульс достигает 120—140 уд/мин. Резко выраженный тризм, расстройства глотания полностью исключают возможность кормления через рот. Введение нейролептической смеси, седуксена, гексе-нала, хлоралгидрата и других противосудорожных средств ликвидирует судороги при сохранении достаточного уровня спонтанного дыхания. А Столбняк IV степени тяжести характеризуется наиболее коротким инкубационным периодом (5—8 сут), начальный период в большинстве наблюдений не превышает 1—1,5 сут, больных госпитализируют в 1-й день заболевания с уже выраженной клинической картиной и приступами судорог, ежеминутно угрожающими асфиксией. В ближайшие 1—2 сут, несмотря на введение предельно высоких доз наиболее сильных противосудорожных средств, приступы судорог усиливаются и учащаются, поэтому возникает необходимость систематического введения миорелаксантов с переводом больного на режим постоянной ИВЛ. Предельно высокий подъем температуры тела (40—41 °С) с тенденцией к дальнейшему росту может стать непосредственной причиной остановки сердца, если вовремя не прибегнуть к гипотермии — искусственному охлаждению больного. Тахикардия до 120—160 уд/мин может приводить к сердечной недостаточности. Тоны сердца глухие, отмечается наклонность к гипотензии. На ЭКГ регистрируют признаки ишемии и токсического поражения миокарда. При физикаль-ном и рентгенологическом исследовании легких определяется картина очаговой, сливной пневмонии, прогрессирующего застоя и начинающегося отека. Стул и мочеиспускание нередко задержаны. |
