Пат физиология. Учебные пособия для студентов высших учебных заведений
 Скачать 7.09 Mb. Скачать 7.09 Mb.
|
|
Глава 17. ПАТОЛОГИЧЕСКАЯ ФИЗИОЛОГИЯ ДЫХАНИЯ Доставка кислорода клеткам органов и тканей животного организма обеспечивает аэробное окисление углеводов, жиров и белков. Сгорание субстратов сопровождается освобождением энергии, необходимой для жизнедеятельности теплокровных животных, поддержания полезной человеку продуктивности. Газообмен между атмосферным воздухом и внутренней средой организма осуществляют органы дыхания. У млекопитающих обмен газами почти полностью происходит в легких. Через кожу обменивается только 1—2%, но у лошади, например, во время интенсивной мышечной нагрузки кожное дыхание возрастает до 8 %. Акт дыхания происходит благодаря сокращению и расслаблению дыхательных мышц, легкие играют пассивную роль. Во время вдоха (инспирация) объем грудной клетки увеличивается, легкие расширяются, во время выдоха (экспирация) объем грудной клетки уменьшается, легкие спадаются. Спаданию способствует эластичная тяга легочной ткани, противодействующая растяжению их воздухом. Частоту и глубину дыхания регулирует дыхательный центр, представляющий собой совокупность нейронов, расположенных в разных отделах центральной нервной системы. В узком понимании дыхательный центр, где группы инспираторных и экспираторных нервных клеток генерируют импульсы, обеспечивающие смену фаз дыхательного цикла, находится в продолговатом мозге. Оттуда посылаются эффекторные импульсы к мотонейронам спинного мозга, иннервирующим дыхательные мышцы. Сам центр находится под влиянием вышележащих отделов центральной нервной системы, коры головного мозга, обеспечивающей возможность произвольного дыхания. Афферентная импульсация поступает к дыхательному центру от рецепторных образований, расположенных в синокаротидных и аортальных рефлексогенных зонах, от рецепторов легких, дыхательных и скелетных мышц. Центральные структуры воспринимают изменения в химическом составе притекающей крови, особенно насыщенность ее двуокисью углерода. Доставка кислорода клеткам обеспечивается внешним и внутренним дыханием. Под внешним дыханием понимают обмен газами между внешней средой и кровью, под внутренним дыханием — обмен газами между кровью и клетками. Внешнее дыхание слагается из прохождения воздуха через носовые ходы, носоглотку, гортань, трахею, бронхи, бронхиолы, попадания в альвеолы, из обмена газами через аэрогематический барьер, выведение двуокиси углерода других продуктов метаболизма с выдыхаемым воздухом. Внутреннее дыхание обеспечивается циркуляцией крови по большому кругу кровообращения. Поступая по капиллярной сети к тканям, кровь благодаря диффузии газов через капиллярную систему отдает кислород и поглощает двуокись углерода. Напряжение кислорода в крови капилляров равно 100 мм рт. ст., в тканевой жидкости — 20—40 мм рт. ст., а в протоплазме клеток оно еще ниже, приближаясь к нулю при функциональной нагрузке. Напряжение же двуокиси углерода в клетках может достигать 60 мм рт. ст., в тканевой жидкости — около 46, а в притекающей крови — 40 мм рт. ст. Благодаря разности давлений кислород диффундирует в ткани, двуокись углерода поступает из тканей в кровь и во внешнюю среду. Сложная система регуляции дыхания, доставки и утилизации кислорода, выведение двуокиси углерода порождают множество причин, ведущих к нарушению газообмена. Расстройства функции дыхания являются следствием многих заболеваний сельскохозяйственных и домашних животных. К ним следует отнести нарушения функциональной активности дыхательного центра, непосредственное поражение органов дыхания в виде воспалительных процессов (ринит, бронхит, пневмония, бронхопневмония, плеврит). Они довольно часто встречаются у животных под воздействием инфекционных факторов (туберкулез, перипневмония крупного рогатого скота, контагиозная плевропневмония, сап, мыт лошадей), инвазионных начал (личиночные формы аскарид, половозрелые формы диктиокаулюсов), при попадании в дыхательные пути инородных тел, пылевых частиц органического и неорганического происхождения, раскаленных газов при пожарах. Возникновению патологических процессов в органах дыхания способствуют содержание животных в сырых, холодных, плохо вентилируемых помещениях, количественное и качественное голодание (гиповитаминоз А). Поражение органов дыхания может быть и вторичного происхождения как осложнение болезней сердца, почек, желудочно-кишечного тракта (тимпания у жвачных). Под влиянием упомянутых и других причин возникает недостаточность дыхания — такое состояние, когда потребность в кислороде не обеспечивается его поступлением в организм. Различают недостаточность внешнего и внутреннего дыхания. Такое деление условно, так как поступление кислорода и поглощение его клетками взаимосвязаны и взаимозависимы. 17.1. НАРУШЕНИЯ ВНЕШНЕГО ДЫХАНИЯ Недостаточность внешнего дыхания представляет собой патологическое состояние, при котором не обеспечивается оксигенация крови, адекватная метаболическим потребностям организма. Она чаще проявляется как сочетанная патология, определяемая функциональной активностью дыхательного центра, пропускной способностью воздухоносных путей, нарушениями диффузии газов через аэрогематический барьер, характером кровотока через сосуды малого круга кровообращения, состоянием плевры и плевральной полости, дыхательных мышц. По интенсивности развития и продолжительности выделяют острую и хронически протекающую недостаточность внешнего дыхания. Острая недостаточность возникает у животных внезапно и продолжается несколько минут или часов. Она может быть результатом острых воспалительных процессов, отека легких, попадания инородных тел в дыхательные пути, вздутия рубца у животных, пережатия трахеи веревкой, цепью при привязном содержании животных, пневмоторакса. Хронически протекающая недостаточность внешнего дыхания определяется месяцами и годами. Сопровождает хронические патологические процессы в трахее и легочной ткани, например катарально-гнойную пневмонию у овец, эмфизему легких у лошадей, туберкулез у крупного рогатого скота, паразитозы (диктиокаулез), опухоли. Нарушение регуляции дыхания обусловлено прежде всего состоянием дыхательного центра. Изменение его деятельности может быть результатом прямого повреждения, опухоли, кровоизлияния, склеротического перерождения стенок сосудов, питающих область дыхательного центра, их тромбоза и эмболии, недостаточности кровоснабжения из-за падения артериального давления. Характер дыхания может быть изменен под воздействием патологических рефлексов с внутренних органов и гуморальных влияния. Меняются частота, глубина, ритм дыхательных движений. Полипноэ — частое поверхностное дыхание. Наблюдается у лихорадящих животных, при воспалительных процессах в легких, застойных явлениях. Учащение ритма дыхательных движений определено повышением концентрации двуокиси углерода в крови, раздражающей дыхательный центр, а поверхностный характер дыхания, особенно при уменьшении числа функционирующих альвеол, объясняется преждевременным выдохом из-за перерастяжения стенок альвеол, не затронутых патологическим процессом. Рефлекторная реакция препятствует чрезмерному растяжению легких при вдохе, имеет защитное значение. Гиперпноэ — глубокое и частое дыхание. Характерно для повышенной мышечной нагрузки, быстро развивающейся лихорадочной реакции, тиреотоксикоза, эмоционального стресса, анемий разного происхождения, пониженного содержания кислорода во вдыхаемом воздухе. Брадипноэ — редкое дыхание. Наблюдают при угнетении функции дыхательного центра. Апноэ — временная остановка дыхания, вызванная понижением возбудимости дыхательного центра. Снижение чувствительности дыхательного центра к рефлекторным и гуморальным воздействиям возникает в результате гипоксии, тяжелой интоксикации, травматических повреждений, действия наркотических препаратов. Диспноэ (одышка) — изменение частоты, глубины и ритма дыхательных движений. Различают инспираторные одышки, вызванные затруднением акта вдоха, экспираторные одышки, возникающие при затруднении акта выдоха, и смешанные, когда нарушен и вдох, и выдох. Инспираторную одышку наблюдают у животных при сужении верхних дыхательных путей (стенотическое дыхание). Из-за возникновения препятствий для нормального прохождения воздуха вдох более продолжителен, чем обычно. Альвеолы заполняются воздухом медленно, тормозится реализация рефлекса Геринга — Брейера. Дыхание будет редким и глубоким. Инспираторную одышку наблюдают у животных при стенозе верхних дыхательных путей разной этиологии. Например, она возникает у животных, больных ринитом первичного (аллергия) или вторичного (фарингит, бронхопневмония) происхождения. Симптоматические риниты, сужение носовых ходов и инспираторную одышку наблюдают у лошадей и свиней, больных гриппом, у крупного рогатого скота, пораженного злокачественной катаральной горячкой. Экспираторная одышка характерна удлинением фазы выдоха. Чаще всего ее наблюдают у лошадей, реже — у других сельскохозяйственных и домашних животных, страдающих эмфиземой легких. При этом заболевании понижена эластичность легочной ткани. Для удаления остаточного воздуха дополнительно вовлекаются вспомогательные мышцы брюшного процесса, поэтому во время выдоха вдоль границы реберной дуги у больных лошадей, коров образуется углубление, называемое «запальным желобом». Кашель возникает как ответная реакция на раздражение нервных окончаний (механо-, барорецепторов), расположенных в гортани, трахее, бронхах, легких. Реакция направлена на удаление из органов дыхания посторонних раздражителей в виде скопления слизи, фибринозных пленок, инородных частиц, занесенных с вдыхаемым воздухом. Раздражение рецепторов рефлексогенных зон, расположенных в органах дыхания, по блуждающему нерву передается дыхательному центру, в котором формируется эфферентная многоуровневая реакция с участием различных групп мышц. Начинается кашлевой акт глубоким вдохом, затем смыкается голосовая щель и сокращаются мышцы экспираторной группы. Создаются условия для повышения внутриплеврального давления до 100 мм рт. ст., тогда как в обычных условиях оно равно 17—35 мм рт. ст. На высоте вдоха открывается голосовая щель и воздух под повышенным давлением устремляется наружу, выбрасывая мокроту, посторонние механические частицы. Очищаются воздухоносные пути, улучшается дыхательная функция легких. Кашель возникает не только от раздражения рецепторов рефлексогенных зон дыхательных путей, но и при наличии патологических очагов в других органах. Позывы на кашель могут возникать из очагов, расположенных в печени, брюшине, кишечнике, глотке, других органах. Кашель возможен от раздражения, исходящего из самой центральной нервной системы, вызван воспалительными процессами (энцефалит) или произвольно. Кашель является защитной реакцией, направленной на поддержание проходимости дыхательной системы. Однако длительный, чрезмерный кашель сопровождается повышением внутригрудного давления, способствует перерастяжению альвеол, потери ими эластичных свойств, ослабляет присасывающую силу сердца, ведет к венозному застою. Чихание — ответная реакция организма на раздражения, исходящие из слизистой оболочки носовых ходов. От механо- и хеморецепторов центростремительные импульсы по тройничному нерву передаются в дыхательный центр. Эфферентная импульсация обеспечивает вовлечение в ответную реакцию тех же механизмов, что и при кашле. Разница в том, что поток воздуха направляется через носовые ходы, освобождая их от инородных влияний. Чихание, как и кашель, — эволюционно выработанный защитный физиологический механизм, направленный на избавление организма от вредоносного начала. Периодическое дыхание. Характеризуется изменениями ритма дыхательных движений. При тяжелых поражениях нейронов дыхательного центра вдох и выдох чередуются с периодами остановки дыхания (апноэ). Различают несколько типов периодического дыхания. Выделяют дыхание Чейна — Стокса, Биота и Куссмауля (рис. 28). 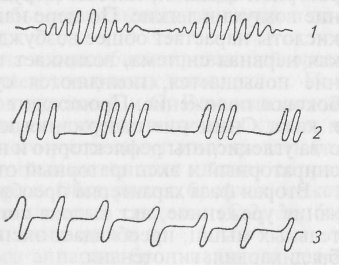 Рис. 28. Схема патологических ритмов дыхания: 1 - Чейна-Стокса; 2 - Биота; 3 - Куссмауля Дыхание Чейна — Стокса характерно тем, что период апноэ чередуется с нарастающими по глубине дыхательными движениями, которые по достижении определенного предела вновь затухают. Наступает пауза (апноэ) продолжительностью 30—45 с, а затем вновь очередной цикл. Этот тип периодического дыхания появляется у животных при таких заболеваниях, как петехиальная горячка, кровоизлияние в продолговатый мозг, при уремиях, отравлениях разного генеза. Дыхание Биота характерно тем, что паузы (апноэ) появляются на фоне дыхательных движений нормальной частоты и глубины. Может возникать при органических поражениях головного мозга (опухоли, травмы, воспалительные процессы, кровоизлияния), при эндогенных и экзогенных интоксикациях. Дыхание Куссмауля относится к терминальному типу. Периоды остановки дыхательных движений чередуются с редкими, глубокими, судорожными вдохами. Этот тип дыхания возникает в результате гипоксии мозга, предшествует клинической смерти. Прогноз при появлении дыхания Куссмауля у больных животных неблагоприятный. Устранение причин и реанимационные меры могут восстановить нормальный ритм дыхания. Патогенез периодического дыхания сводится в основном к тому, что дыхательный центр под влиянием чрезвычайных раздражителей теряет чувствительность к обычным концентрациям углекислоты. Во время остановки дыхания содержание углекислоты в крови нарастает, после достижения критического уровня ее возбуждается дыхательный центр, его функция на какое-то время восстанавливается. Эта цикличность повторяется. Устранение причин и реанимационные меры могут восстановить нормальный ритм. Удушье (асфиксия) — патологическое состояние, определяемое недостаточным или полным прекращением доступа кислорода в организм и накоплением в его тканях углекислоты. Причины, вызывающие асфиксию у сельскохозяйственных и домашних животных, многообразны. Они могут быть результатом:
В развитии асфиксии механического происхождения выделяют четыре быстротечные фазы. Первая фаза протекает с изначальным преобладанием инспираторной одышки, так как затруднено или прекращено поступление воздуха в легкие. По мере накопления в тканях и крови углекислоты нарастает общее возбуждение, активируется симпатическая нервная система, возникает тахикардия, артериальное давление повышается, появляются судороги, животные принимают боковое положение. Происходит непроизвольное отделение мочи и кала. Снижение содержания кислорода и повышение количества углекислоты рефлекторно и непосредственно возбуждают ин-спираторный и экспираторный отделы дыхательного центра. Вторая фаза характерна преобладанием вагусного влияния. Дыхание уреженное, акт выдоха сопряжен с вовлечением дополнительных мышц, преобладает экспираторная одышка. Отмечаются брадикардия,гипотензия. Третья фаза сопряжена с торможением дыхательного центра под влиянием непрекращающейся гипоксии, остановкой дыхания, дальнейшим падением артериального давления. Животное находится в предтерминальном состоянии. Четвертая фаза — терминальная, во время которой у погибающего животного можно наблюдать несколько конечных вдохов. Полное прекращение дыхания не сопровождается одновременной остановкой сердечной деятельности. Сердце продолжает сокращаться еще несколько минут, затем наступает клиническая смерть, во время которой еще возможно оживление животного. Расстройства дыхания, вызванные поражением легких. Бронхиальная астма — рецидивирующее неспецическое заболевание, сопровождающееся периодическими приступами удушья. Заболевание наблюдается у лошадей, крупного атого скота, особенно у телят в возрасте 2—3 мес, у животных тих видов. Основная причина — гиперреактивность дыхательных путей на специфические и неспецифические раздражители, терреактивность появляется как результат сенсибилизации животных аллергенами неинфекционной природы (астма бронхиальная атоническая) или как обусловленная инфекционным процессом, протекающим в дыхательных путях (астма инфекционно-аллергическая). Может развиваться смешанная форма, с участием аутоиммунных процессов. В качестве этиологических факторов, ведущих к развитию атопической бронхиальной астмы у животных, называют некачественные заплесневелые корма, поедание ядовитых растений, избыточное потребление концентратов при гиповитаминозе В1, попадания в дыхательные пути пыльцы растений (поллиноз). Цветочная пыльца уже спустя несколько минут экспозиции сенсибилизирует эпителий слизистой оболочки дыхательных путей. Так же быстро при повторном попадании пыльцы появляются признаки бронхиальной астмы. К аллергенам микробного происхождения, способным вызвать инфекционно-аллергическую астму, относят стафилококки, стрептококки, пневмококки, грибы рода кандида, кишечную палочку, протей. Вторичное внедрение антигена в сенсибилизированный организм сопровождается образованием иммунных комплексов. Повышен синтез иммуноглобулинов классов Е и G. В подслизистом слое бронхов сосредоточено большое количество тучных клеток, в свет бронхов из циркуляторного русла могут мигрировать базофилы. Реакция антигена с антителами на этих клетках сопровождается выделением медиаторов. Обструкция бронхов может быть вызвана компонентами комплемента системы (С.2, За, 5а, 5-9), гистамином, серетонином, кининами и др. Сокращение гладкомышечного аппарата бронхиального дерева, отек слизистой оболочки, гиперсекреция желез и скопление экссудата препятствуют нормальному доступу кислорода к альвеолам. Недостаточная оксигенация крови, повышение концентрации углекислоты, других продуктов метаболизма нарушает деятельность дыхательного центра. Развиваются признаки респираторного удушья. Для выведения воздуха из альвеол вовлекается вспомогательная мускулатура. Бронхиты— воспаления слизистой оболочки бронхов. Заболевания довольно широко распространены среди сельскохозяйственных и домашних животных. Причинами являются вирусы (грипп, чума, аденовирусные инфекции), бактерии (протей, кишечная палочка), микоплазмы, паразиты (анкилостомы, стронгиляты, кокцидии), аллергены. Появлению заболеваний способствуют неблагоприятные условия содержания: переохлаждение, неполноценное кормление, поение холодной водой, содержание в сырых, плохо вентилируемых помещениях. Хронические бронхиты чаще вторичного происхождения — как следствие сердечно-сосудистой недостаточности, заболеваний почек, других органов. Основная причина дыхательной недостаточности при бронхитах — уменьшение просвета воздухоносных путей (крупных и малых бронхов), вызванного гиперемией и набуханием слизистой оболочки, гиперсекрецией катарального экссудата, диапедеза лейкоцитов. В тяжелых случаях воспалительный процесс распространяется на подслизистый и мышечный слои, перибронхиальную ткань. Для бронхита аллергического происхождения характерно появление эмфиземы легких со смешанной инспираторно-экспираторной одышкой. Пневмония, пневмонит — воспаление легких. По этиологии различают пневмонию вирусного (чума собак, перипневмония крупного рогатого скота), бактериального (пневмококки, стафилококки, стрептококки), микоплазменного, паразитарного, микозного происхождений. Пневмония может быть обусловлена попаданием в дыхательные пути кормов, рвотных масс, жидкости, тромбоэмболией легочных артерий. Развитие у животных пневмонии, обусловленной активацией микрофлоры, особенно факультативной, тесно связано с состоянием организма, развитием, в частности, сенсибилизации к аутоантигенам при поражении легочной паренхимы разного происхождения. Выявлено, например, что в генезе спонтанных, колимикоплазменных пневмоний у кур важное место занимают аутоиммунные процессы. Причем ведущим пусковым механизмом, как полагают, служат микоплазмы, антигенные субстанции которых активируют «запрещенные» клоны В-лимфоцитов — продуцентов аутоантител. Кислородная недостаточность при пневмониях обусловлена уменьшением дыхательной поверхности легких за счет выпотевания в просвет альвеол экссудата, слущивающегося эпителия. Заполненные экссудатом альвеолы не участвуют в газообмене. Общая дыхательная поверхность легких сокращена. Вдох укороченный из-за перерастяжения оставшихся нормальных альвеол. Окончания волокон блуждающего нерва со стенок функционирующих альвеол посылают афферентную импульсацию еще до оптимального расширения грудной клетки. Преждевременная благодаря рефлексу Геринга — Брейера остановка акта вдоха предохраняет не вовлеченные в патологический процесс альвеолы от перерастяжения и разрыва. Дыхание при пневмонии учащено из-за стимуляции дыхательного центра углекислым газом и нервно-рефлекторного влияния. Бронхопневмония — поражение воспалительным процессом бронхов и альвеолярного аппарата. Наиболее часто встречается у крупного рогатого скота, овец, коз, свиней, реже — у лошадей, собак. Особенно восприимчив молодняк животных всех видов. Болезнь чаще возникает на фоне ослабления общей резистентности животных при нарушении режима кормления матерей и новорожденных. Бронхопневмония возникает под воздействием неспецифической микрофлоры легких, но может осложнять многие болезни животных инфекционного (сальмонеллез) и инвазионного (диктиокаулез) происхождения. Развитие неспецифической бронхопневмонии сочетается с иммунодефицитом. Так, у больных свиней выявлен дефицит Т-системы иммунитета: на 39 % падает содержание Т-лимфоцитов в крови; более чем в 2 раза снижается коэффициент дифференцировки субпопуляций Т-лимфоцитов за счет клеток с хелперной функцией. Падает фагоцитарная активность альвеолярных макрофагов, снижена их окислительная способность. Применение в комплексной терапии больных иммуностимуляторов сокращает фазу выздоровления, предотвращает хронизацию воспалительных процессов. Бронхопневмония опасна обтурацией бронхов катаральным экссудатом, развитием ателектазов, инфицированием спавшихся участков легких, появлением гнойно-некротических очагов. Особенно часто катарально-гнойная бронхопневмония наблюдается у овец, находящихся в неблагоприятных условиях содержания (холод, дождь, сырые помещения, несбалансированное кормление). Развивающаяся у больных животных нетоксическая гипоксия сочетается с токсической. Частично компенсируется смешанной, инспираторно-экспираторной одышкой. Отек легких (oedema pulmonum). Наблюдается у животных разных видов. Заболевание полиэтиологично. Рассматривают два основополагающих фактора в развитии отека у разновозрастных животных: застойные явления в системе малого круга кровообращения и токсикоз. Гемодинамические, застойные отеки легких возникают при декомпенсации пороков левой половины сердца, таких, как стеноз отверстия аорты, митральный стеноз, при обширных инфарктах миокарда. Затруднения перемещения массы крови из малого круга кровообращения в большой ведут к венозной гиперемии легочных сосудов Токсический отек обязан своим появлением экзогенно поступающим ядовитым соединениям (бактериальные токсины, яды насекомых, растительные алкалоиды, БОВ), избыточному образованию в самом организме гистамина, серотонина, ацетилхолина, других биологически активных веществ, особенно при аллергических состояниях. Отек легких развивается под влиянием и других причин: скученного содержания животных, особенно при транспортировке, перегревания, солнечного удара, травм головного мозга и др. В основе отека любого происхождения ведущим фактором является повышение проницаемости капилляров. Образующийся транссудат проникает в альвеолярные пространства, препятствуя их вентиляции. Парциальное давление кислорода в капиллярах малого круга кровообращения резко снижается, что еще больше повышает их проницаемость, способствует прогрессированию транссудации. Отечная жидкость способна заполнить не только альвеолы, но и попасть в бронхи, трахею, гортань, выводиться из полости носа и рта в виде пенистой жидкости. Наполненные жидкостью легкие не в состоянии следовать движениям грудной клетки. Медленно развивающийся, хронически протекающий отек легких может осложняться трудно поддающейся лечению гипостатической пневмонией. Нарушения функции плевры. Плевра представляет собой серозную оболочку, покрывающую легкое снаружи (висцеральная плевра) и выстилающую стенку грудной полости (костальная плевра). Щелевидное пространство между ними называется плевральной полостью; она содержит серозную жидкость. Правая и левая половины легкого расположены в изолированных друг от друга полостях, между которыми находится средостение. Нарушения внешнего дыхания возникают в результате воспалительных процессов, попадания в плевральную полость жидкости (гидроторакс) или воздуха (пневмоторакс). Плеврит — это воспаление плевры. Болеют животные всех видов. Первичные плевриты наблюдаются после переохлаждения; травматизации у жвачных животных инородными колющими предметами, проникающими из сетки; в результате проникновения инфекции; при ранениях грудной клетки или распадающейся опухоли; аллергии. Вторичные плевриты сопровождают пневмонию, перитонит, туберкулез, повальное воспаление легких у крупного рогатого скота, другие инфекционные болезни. При плеврите повышается проницаемость сосудов, питающих плевру, выпотевает экссудат. По характеру экссудата выделяют серозный, гнойный, геморрагический, гнилостный плеврит. Чаще экссудат бывает смешанного типа — серозно-гнойный. В плевральной полости может накапливаться у лошадей 15—20л экссудата, у свиней 2—10, у собак до 5л. Он сдавливает легкие, в результате затрудняется их заполнение воздухом, снижаются внут-ригрудное давление, приток венозной крови к сердцу. Выпот фибринозного экссудата ведет к образованию спаек между висцеральным и костальным листками плевры. Спайки мешают нормальной экскурсии грудной клетки, вызывают чувство боли. Разрастающаяся фиброзная ткань способна заполнить всю плевральную полость, сдавливая легкие, вплоть до остановки дыхания. 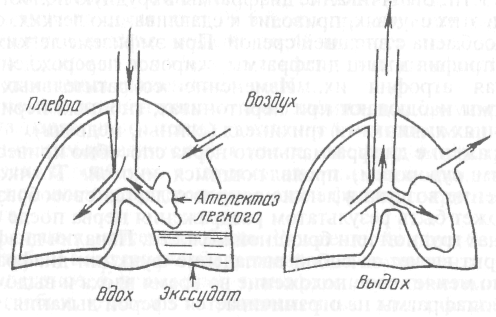 Рис. 29. Схема пневмоторакса и гидроторакса Пневмоторакс — скопление в плевральных полостях воздуха. У млекопитающих он чаще односторонний (рис. 29). Воздух в плевральные полости может попадать через проникающие повреждения грудной клетки или висцеральной плевры. В последнем случае пневмоторакс вызван проникновением воздуха из легких в результате кавернозного распада туберкулезного очага, вскрытия абсцесса. Выделяют три разновидности пневмоторакса:
Полное спадание одного легкого при пневмотораксе приводит, к смещению средостения, находящегося там сердца, магистральных кровеносных сосудов, нервных образований. Нарушается кровообращение, возникают патологические рефлексы, меняющие функции внутренних органов. Жизнь сохраняется за счет викарной компенсации, усиления функциональной активности второго легкого. Учащенное, поверхностное дыхание и тахикардия — элементы компенсаторно-приспособительной реакции целостного организма, предупреждающей тотальную гипоксемию. Двусторонний пневмоторакс несовместим с жизнью животного. Нарушения функции дыхательных мышц. Внешнее дыхание зависит от состояния мышц, участвующих во вдохе и выдохе. Их функция может быть нарушена в результате патологических процессов непосредственно в мышечной ткани или поражения нервов, обеспечивающих ритмичность и глубину дыхательных движений. Дыхательные мышцы могут быть подвержены травматическим повреждениям, воспалительным процессам (миозиты), дистрофии и атрофии. Травмы мышц, переломы ребер вызывают болевую реакцию, которая рефлекторно ограничивает движение грудной клетки. Дыхание становится поверхностным, аритмичным. Особо важное значение в реализации дыхательных движений имеет состояние диафрагмы. Ее функция у животных нарушается при вздутии рубца у жвачных, метеоризме кишечника, водянке брюшной полости. Выпячивание диафрагмы в грудную полость, наблюдаемое в этих случаях, приводит к сдавливанию легких, ограничению газообмена с внешней средой. При эмфиземе легких выражены гипотрофия мышц диафрагмы, жировое перерождение и последующая атрофия их. Изменение сократительных свойств диафрагмы наблюдают при перитонитах, гнойных перикардитах, поражениях личинками трихинелл (свиньи, медведи). Раздражение диафрагмального нерва способно привести к кло-ническим судорогам, проявляющимся икотой. Толчкообразное поступление воздуха в легкие сопровождается своеобразным звуком. Может быть результатом раздражения нерва после операции на органах грудной или брюшной полости. Паралич диафрагмального нерва влечет за собой выпадение функции диафрагмы; она пассивно меняет свое положение во время вдоха и выдоха. Роль диафрагмы не ограничивается сферой дыхания. Ее состояние сказывается на кровообращении. Сжимая и расслабляя кровеносные и лимфатические сосуды органов брюшной полости, диафрагма опорожняет их венозную систему, проталкивает кровь к грудной клетке. Поэтому она справедливо может быть названа вторым (венозным) сердцем. Изменяя своими сокращениями внутрибрюшное давление, диафрагма обеспечивает кровоток в печени, воздействует на все ее функции, направляет поток желчи в пиечник, а лимфы — от ворсинок в лимфатическую и венозную системы. Таким образом, расстройства функциональной активности ди-афрагмальной мышцы способны вызвать многосторонние изменения в организме. 17.2. НАРУШЕНИЯ ВНУТРЕННЕГО ДЫХАНИЯ Расстройства внутреннего дыхания определяются нарушениями транспорта кислорода от легких к тканям, использования кислорода тканями (тканевое дыхание) и переноса углекислоты от тканей к легким. Нарушение транспорта кислорода. Из легких, преодолевая аэро-гематический барьер, кислород поступает в кровь, где с гемоглобином эритроцитов образует непрочное, легко диссоциирующее соединение — оксигемоглобин. При обычном парциальном давлении кислорода в альвеолах 1 г гемоглобина способен связать до 1,34 мл кислорода. В крови млекопитающих количество гемоглобина колеблется в пределах 130—160 г/л. Кислородная емкость составляет 19,3—21,3 об.%. Снижение кислородной емкости крови и ограничение доставки кислорода тканям возникают в результате следующих причин: 1) падения парциального напряжения кислорода в альвеолярном воздухе. Так, если при обычном атмосферном давлении парциальное напряжение кислорода равно 100 мм рт. ст., окисляемость гемоглобина составляет 98,6 %, то при падении парциального давления в воздухе альвеол до 40 мм рт. ст. насыщенность кислородом будет менее 75 %. Она станет недостаточной для нормального снабжения тканей кислородом; 2) снижения концентрации гемоглобина в циркулирующей крови. Она падает при анемии, вызванной гемолизом эритроцитов; при постгеморрагической анемии; анемиях алиментарного происхождения, особенно у поросят; анемии, развивающейся как следствие подавления эритропоэтической функции красного костного мозга; 3) образования метгемоглобина. Ряд веществ способен окислять гемоглобин в метгемоглобин, превращая двухвалентное железо в трехвалентное. К веществам, трансформирующим гемоглобин в метгемоглобин, относятся промышленные яды (нитробензол, анилин и др.), а также нитриты и нитраты, поступающие животным с растительными кормами. Метгемоглобин представляет coбой стойкое соединение, не обладающее способностью транспортировать кислород, передавать его тканям; 4) образования карбоксигемоглобина. Вдыхание воздуха, содержащего даже небольшое количество окиси углерода (СО, «угарного газа»), приводит к образованию карбоксигемоглобина. В этом соединении, образованном по тому же принципу, что и оксигемоглобин, окись углерода связывается с гемоглобином в 300 раз прочнее, чем кислород. Почти весь гемоглобин блокируется окисью углерода даже при содержании нескольких десятков объемных процентов СО во вдыхаемом воздухе. В результате развивается гипоксемия (снижение О2 в крови) и гипоксия (снижение О2 в тканях). Окись углерода может оказаться в воздухе, вдыхаемом животными, во время пожаров, при работе моторов автомашин, тракторов в животноводческих помещениях. Снижение снабжения тканей кислородом может быть результатом нарушения сродства гемоглобина к кислороду. Сдвиг кривой диссоциации оксигемоглобина вправо наблюдается при лихорадке, гиперемии, накоплении кислых продуктов (ацидоз). Сдвиг влево наблюдается при переохлаждении организма, всех формах. алкалоза. Ухудшается диссоциация оксигемоглобина в тканях, затруднена передача кислорода клеткам. Замедление скорости кровотока, ишемизация тканей — также одна из причин, вызывающих кислородное голодание. Нарушение тканевого дыхания. Окислительные процессы, происходящие в межклеточном веществе и клетках, осуществляются путем отдачи водорода, присоединения кислорода и переноса электрона или перемены валентности. Начинается окисление с дегидрирования, затем водород окисляется до образования воды. Кроме дегидраз и оксигеназ в окислительных процессах участвуют и другие ферменты — пероксидазы, переносчики водорода — цитохромы и флавопротеиды; переносчики фосфата, аминогрупп, другие ферменты. Недостаточное поступление кислорода нарушает окислительно-восстановительные процессы в клетке. Гипоксия (от лат. hypo — мало, oxygenium — кислород) — состояние, возникающее в организме при недостаточном поступлении кислорода тканям или затруднении использования его клетками. Гипоксию принято считать типичным патологическим процессом. Несмотря на многообразие порождающих ее причин, ее проявление, компенсаторные реакции во многих случаях протекают однотипно. В зависимости от этиологии и патогенеза выделяют следующие разновидности кислородного голодания тканей:
Нарушение транспорта двуокиси углерода. Как продукт тканевого дыхания двуокись углерода приносится к легким венозной кровью, находясь в составе солей (в бикарбонате калия и натрия 80 об.%), карбгемоглобина (10об.%) и будучи физически растворимым в плазме и эритроцитах (10об.%). Угольная кислота из двуокиси углерода образуется в эритроцитах под влиянием карбоангидрата — катализатора, определяющего реакцию гидратации (О2+Н2О = Н2СО3 ). Фермент способен катализировать реакцию не только в направлении синтеза углекислоты, но и дегидратации ее до исходных продуктов. В тканях, где напряжение СО2 высокое, происходит образование Н2СО3, а в легких, где оно низкое, карбоангидраза ускоряет реакцию дегидратации, способствующей освобождению СО2 и выведению во внешнюю среду. Поступление диоксида углерода в эритроциты сопряжено с отдачей оксигемоглобином кислорода, превращением его в редуцированный гемоглобин. Угольная кислота вытесняет из гемоглобина ионы калия и натрия, образуя бикарбонаты (НКСО3, HNCO3). В альвеолярном воздухе парциальное давление диоксида углерода ниже, чем в венозной крови, поэтому путем диффузии он перемещается из легочных капилляров в полость альвеол, а кислород — в кровь капиллярной сети легких. Гемоглобин превращается в оксигемоглобин, вытесняет угольную кислоту из бикарбонатов. Она, в свою очередь, подвергается расщеплению карбоангидразой на Н2О и СО2. Двуокись углерода диффундирует альвеолы и выводится. Нарушение транспорта углекислоты из тканей в легкие и выведение СО2 во внешнюю среду может быть результатом:
Повышение парциального давления диоксида углерода в крови (гиперкапния) сопровождается респираторным ацидозом, наблюдаемым у животных, страдающих эмфиземой легких, бронхитами, бронхиальной астмой. Повышение в крови органических кислот нередко наблюдают у продуктивных животных как результат нарушений межуточного обмена веществ в тканях (метаболический ацидоз) при многочисленных заболеваниях (кетоз, послеродовой парез, рахит, остеодистрофия, атония желудков и др.). Снижение парциального давления диоксида углерода в крови (гипокапния) возникает как результат интенсивной гипервентиляции легких, повышенного выделения СО2. Наблюдают при перегревании животных, горной болезни, воспалительных и опухолевых поражениях головного мозга. Недостаток углекислоты и избыток щелочей ведут к респираторному алкалозу. Компенсаторно-приспособительные реакции при кислородной недостаточности. Гипоксия воспринимается как чрезвычайный раздражитель рецепторными образованиями, улавливающими изменения химического гомеостаза. Формирование защитных ответно-приспособительных реакций организма зависит от ряда факторов. Животные разных видов неодинаково переносят недостаток кислорода. Чем выше стоит животное на «эволюционной лестнице», чем более организована его центральная нервная система, тем чувствительнее организм к гипоксии. Молодые животные, особенно в ранний постнатальный период, менее чувствительны к кислородному голоданию, чем взрослые. Низкая температура окружающей среды делает организм более устойчивым к недостатку кислорода, чем температура, превышающая оптимальные величины. Характер изменений, возникающих при недостатке кислорода в тканях, обусловлен во многом формой гипоксии. При ее острой форме компенсаторные механизмы направлены преимущественно тему транспорта кислорода, при хронической ферме — в основном на адаптационные системы утилизации кислорода тканями. Острая форма гипоксии (обильная кровопотеря, полицитемическая гиповолемия при остром отравлении коров хлоридом натрия) вызывает прежде всего ответную компенсаторную реакцию со стороны органов дыхания и кровообращения. Повышение концентрации диоксида углерода и ионов водорода возбуждает дыхательный центр и хеморецепторы, заложенные в стенках кровеносных сосудов, прежде всего аортальной и синокаротидной зон. Раздражение хеморецепторов происходит также за счет снижения парциального давления кислорода в крови, что характерно для «горной» болезни. В ответ на прямое и опосредованное (через афферентную импульсацию) возбуждение дыхательный центр отвечает учащением и углублением дыхания. Тем самым усиливается вентиляция легких. В газообмен вовлекаются резервные альвеолы. Снижается содержание СО2 в циркулирующей крови, возрастает ее оксигенация. Повышается функциональная активность системы кровообращения. Рефлекторно и путем прямого действия гипоксии на сердце стимулируется его деятельность. Развивается тахикардия. Возрастает скорость кровотока, улучшается легочное кровообращение. В кровоснабжение вовлекаются нефункционирующие капилляры. Перераспределяется ток крови. Более интенсивно снабжаются кровью жизненно важные органы (головной мозг, сердце, почки) за счет других менее важных для жизнедеятельности организма. Сосуды мозга, сердца расширяются, в то время как артериолы мышц, органов брюшной полости суживаются. Усиливается выброс депонированных эритроцитов из селезенки, особенно у лошадей, печени, других органов, что повышает кислородную емкость крови, поддерживаемую в последующем усиленным эритропоэзом. Стимулируют эритропоэз эритропоэтины, освобождаемые разрушающимися эритроцитами, и эритропоэтины почечного происхождения. При гипоксии возрастает способность эритроцитов, гемоглобина связывать кислород в летких и более интенсивно отдавать его тканям. Эритроциты в большей степени, чем обычно, насыщены аденозинтрифосфорной кислотой и 2,3-дифосфоглицеридом, что облегчает утилизацию кислорода клетками. Хроническая гипоксия не может быть компенсирована только аварийной гиперфункцией дыхания и кровообращения. Недостаток кислорода приводит к структурным перестройкам. Активируется синтез нуклеиновых кислот и белков, лежащих в основе наблюдаемых процессов гипертрофии и гиперплазии в системах транспорта кислорода. В кровоток вовлекаются нефункционирующие капилляры, увеличиваются их просвет и длина, дыхательные мышцы и миокард гипертрофируется, повышается общая площадь газообмена в легких за счет вовлечения резервных альвеол. Напряженность механизмов доставки кислорода клетками снижается. Одновременно проявляются адаптационные возможности тканей в более рациональной утилизации кислорода. Так, повышаются процессы гликолиза и бескислородного освобождения энергии. Накопление недоокисленных продуктов способствует более интенсивной диссоциации оксигемоглобина. Ингибиция ресинтеза аденозинтрифосфорной кислоты в митохондриях сти-лулирует генетический аппарат клетки к биосинтезу дополнительных митохондрий. Возрастающая мощность системы митохондрий на единицу массы тканей ведет к устранению дефицита денозинтрифосфорной кислоты. Ее энергия используется клетками для восстановления своих специфических функций в условиях недостатка поступления кислорода. Адаптационные механизмы обеспечивают прежде всего функциональную активность органов, ответственных за жизнеобеспечение организма: коры головного мозга, подкорковых образований, сердца, красного костного мозга, дыхательных мышц. При гипоксии в тканях головного мозга более интенсивно протекает «целительное фосфорилирование, что объясняют повышением сопряженности фосфорилирования с окислением. Гипоксия стимулирует гипоталамо-гипофизарно-надпочечниковую систему. Показано, что глюкокортикоиды активируют некоторые ферменты дыхательной цепи. Возможности организма к адаптивным реакциям, вызванным недостаточной обеспеченностью тканей кислородом, весьма велики. Устойчивая адаптация к гипоксии может сохраняться длительное время. Установлено даже, что адаптированный к кислородному голоданию организм менее реактивен по отношению ко многим стрессорным факторам. Однако возможности организма небеспредельны, и в условиях декомпенсации начинает проявляться повреждающий эффект гипоксии. Декомпенсация кислородного голодания системного и местного характера сопровождается функциональными изменениями и структурными преобразованиями в тканях. Основа всех функциональных нарушений клеточных структур, обусловленных кислородной недостаточностью, — снижение синтеза макроэргических соединений, в числе которых аденозинтрифосфорная, пиро- поли- и креатинфосфорная кислоты, фосфопировиноградная кислота, нуклеозидтрифосфорная и нуклеозиддифосфорная кислоты. Аккумулированная в макроэргических соединениях энергия используется клеткой для обеспечения всех видов ее деятельности. Недостаток кислорода прерывает процесс окисления субстратов (углеводов, жиров и белков) до конечных ) продуктов (углекислота, вода, аммиак, мочевина, некоторые другие соединения). Углеводы начинают распадаться по анаэробному типy, в организме накапливаются недоокисленные продукты в виде пировиноградной, молочной кислот. Окисление жиров останавливается на стадии образования преимущественно кетоновых тел (ацетон, бета-оксимасляная и уксусная кислоты); их накопление ведет к тяжелому заболеванию — кетозу. Нарушается энергозависимый процесс всасывания аминокислот в кишечнике. Развивающийся отрицательный белковый баланс влечет за собой нарушение метаболизма белка, задержку роста молодняка, полового созревания, снижение продуктивности (мясной, молочной, шерстной) сельскохозяйственных животных, естественной резистентности, повышение заболеваемости. Неполный распад углеводов, жиров, белков сопровождается снижением щелочного резерва и развитием ацидоза. Избыточное накопление анионов, снижение рН крови негативно сказываются на функционировании органов и систем. Головной мозг крайне чувствителен к гипоксии. Его потребность в кислороде составляет около 20 % по отношению к нему количеству, используемому организмом. Гипоксию мозга первичного происхождения у животных наблюдают при некоторых вирусных инфекциях (инфекционный (энцефаломиелит лошадей), незаразных болезнях (опухоли головного мозга, кровоизлияния). Чаще недостаточное кровоснабжение мозга отмечается как вторичный процесс, сопровождающий порок сердца, дистрофию миокарда, миокардиты, гипотензию при шоке, коллапсе разного происхождения. Основной субстрат окисления, а следовательно, и главный источник энергии в нервных клетках головного мозга — глюкоза. Недостаток кислорода ведет к снижению содержания в клетках макроэргических соединений, их синтеза. Энергозависимые процессы, определяющие генерацию и передачу нервных импульсов, затухают. В самих нервных клетках идет прогрессивное накопление недоокисленных продуктов обмена (молочная и пировиноградная кислоты, кетоновые тела, аммиак). Ацидоз сопровождается повышенной проницаемостью капиллярной сети мозга, явлениями отека, что усугубляет нарушение функциональной активности нейронов. Первоначально в случаях острой гипоксии она клинически проявляется у животных общим возбуждением, но очень скоро начинают преобладать признаки тормозных процессов. У животных можно наблюдать общее угнетение, слабость, атаксию; условные и врожденные рефлексы затухают. Животное может принимать боковое положение, оно не реагирует на болевые раздражения, свет, звук. Острая гипоксия (обильная кровопотеря, удушье) сопровождается коматозным состоянием. Установлено, что прекращение поступления кислорода к клеткам коры больших полушарий мозга и мозжечка уже спустя 3—4 мин приводит к появлению очагов некроза, а через 5—8 мин наступает клиническая смерть с остановкой дыхания и падением артериального давления до нулевой отметки. Сердце, как и мозг, чрезвычайно чувствительно к гипоксии. Сердечная мышца бедна гликогеном, слаба ее способность к энергообеспечению за счет анаэробных процессов. Прогрессирующее снижение макроэргических соединений ведет к ограничению активности всех функций сердечной мышцы, но особенно к его сократимости, требующей затрат большого количества энергии, аккумулированной в молекулах АТФ, других макроэргических соединениях. Возникающий дефицит этих соединений сопровождается нарушениями проницаемости клеточных мембран. Перемещение ионов энергозависимо; в результате снижения энергопотенциала митохондрий наблюдается избыточное проникновение в клетку кальция, натрия и выход из нее калия. Ионы кальция, активируя внутриклеточную фосфолипазу, способствуют расширению билипидного слоя мембран. Снижение функциональной активности сердца при развивающейся гипоксии сопровождается недостаточностью кровообращения с вытекающими последствиями. Почки при гипоксемии и гипоксии снижают свою фильтрационную способность из-за падения артериального давления в почечных клубочках. Кроме того, около 80 % потребляемого почкой кислорода идет на обеспечение канальцевой реабсорбции, особенно Na+. Кислородное голодание негативно отражается на реабсорбционной и секреторной функциях нефрона, особенно его дистальной части, где энергозависимые процессы в значительной степени определяют гомеостатическую способность почек. Печень весьма чувствительна к гипоксии, особенно протекающей хронически. Кислородное голодание гепатоцитов, обусловленное застойными явлениями, порождаемыми правосторонней сердечной недостаточностью, приводит к ацидозу, дестабилизации клеточных мембран. Нарушаются основные функции печени; погибшие гепатоциты замещаются элементами соединительной ткани. Развивается цирроз печени — тяжелое неизлечимое заболевание. |
