Пат физиология. Учебные пособия для студентов высших учебных заведений
 Скачать 7.09 Mb. Скачать 7.09 Mb.
|
|
18.5. НАРУШЕНИЯ ПИЩЕВАРЕНИЯ В ПРЕДЖЕЛУДКАХ У ЖВАЧНЫХ Особенность пищеварительных процессов в преджелудках жвачных — присутствие симбионтной микрофлоры и микрофауны. У полигастричных животных расщепление питательных субстратов осуществляют до 150 видов бактерий и до 60 разновидностей простейших, представленных классом реснитчатых инфузорий. Представители микрофлоры выполняют такие функции, как сбраживание клетчатки, молочной и янтарной кислот, переваривание крахмала, расщепление белков, безбелковых азотистых продуктов, липидов. Отдельные виды рубцовых бактерий специализируются на утилизации целлюлозы, глюкозы, белков, липидов. Одновременно за счет субстратов кормовых масс идет интенсивный бактериальный синтез. Бактерии способны синтезировать белок, превращая непротеиновый азот в протеиновый. Около 10 % белка содержимого рубца представлено бактериями. Инфузории формируют свое тело за счет бактерий, которые они поглощают, и фрагментов поступающей в преджелудки растительной массы. Простейшие превращают сахар и растительный крахмал в гликоген, растительный белок — в животный, делая его более полноценным. При хорошо развитой микрофауне рубца ее белок составляет около 20 % общего белка рубца. Перемещение пищевых масс из преджелудков в сычуг, а затем в кишечник дает возможность организму использовать полноценный белок бактерий и инфузорий. Рубцовое пищеварение, во многом обусловленное состоянием микрофлоры и микрофауны, может изменяться, если условия их существования не будут адекватными потребностям. Нарушения в кормлении, недостаточно полноценный и несбалансированный рацион, заболевания, вызывающие расстройства моторной функции преджелудков, изменяют среду обитания бактерий и инфузорий, подавляют их деятельность. Бесконтрольное применение антибиотиков, сульфаниламидных препаратов, других лекарственных средств также неблагоприятно сказывается на рубцовом пищеварении. Нарушение биохимического равновесия в рубце. Обитатели рубца в процессе своей жизнедеятельности утилизируют клетчатку, обеспечивают ее превращение через глюкозу и пировиноградную кислоту в низкомолекулярные жирные кислоты, метан, диоксид углерода. Полноценное кормление животных, дача достаточного количества грубых кормов (люцерновое сено) сопровождается образованием в составе летучих жирных кислот около 70 % уксусной кислоты, около 18 % пропионовой, около 8 % масляной, 4 % других кислот (изомасляная, валериановая, изовалериановая). Ацетат представляет собой продукт, используемый организмом для синтеза липидов в жировых депо (подкожный, мезентериальный) и молочного жира. Пропионат служит для ресинтеза глюкозы, глицерина. Обычные условия содержания и кормления обеспечивают образование в рубце лактирующих коров 2,5—5 кг летучих жирных кислот, в рубце овец — 0,2—0,5 кг, что почти на 70 % удовлетворяет энергетические потребности организма. На общее количество летучих жирных кислот и их соотношение в рубцовом содержимом влияет состав рациона. Дача больших количеств монокорма, представленного концентратами (комбикорм, ячмень), существенно меняет соотношение низкомолекулярных жидких кислот. Так, содержание масляной кислоты возрастает до 15 %, пропионовой — до 21, количество ацетата падает с 70 до 57 %. Такое понижение уровня уксусной кислоты негативно сказывается на жирности молока, а повышение уровня масляной кислоты в рубцовом содержимом — на его общей кислотности. Избыточное образование молочной кислоты в рубце наблюдают тогда, когда животные поедают корма, богатые сахарами: свеклу, капусту, турнепс, картофель, кукурузу. Избыточное поступление крахмала усиливает активность амилолитических и молочнокислых бактерий, но неблагоприятно отражается на состоянии целлюлозолитических ввиду повышения кислотной среды до рН 5,5—6,0, тогда как оптимальный показатель рН 6,5. Высокая кислотность среды тормозит продвижение кормовых масс из преджелудков в сычуг, из сычуга — в кишечник, что негативно сказывается на пищеварении. Кетоз (ацетонемия). Источник образования кетоновых тел в рубце — летучие жирные кислоты. Кетогенным действием обладает масляная и отчасти уксусная кислоты. У здоровых коров содержится 1,6 мг кетоновых тел на 100 мл, у овец — 3,7 мг на 100 мл. Кетозом называют заболевание высокоудойных коров, суягных овец, характеризующееся повышенным содержанием кетоновых тел в крови (гиперкетонемия), моче (кетонурия), молоке (кетонолактия), гипогликемией. К наиболее частым причинам, вызывающим кетоз, относят избыток концентрированных кормов в рационе, сочетающийся с недостатком легкопереваримых углеводов, однообразное кормление силосом, жомом, содержащими повышенное количество уксусной и масляной кислот. У жвачных животных существует видовая предрасположенность к этому заболеванию, так как в кровь из пищеварительного канала поступают не углеводы, а летучие жирные кислоты, две из которых (масляная, уксусная) обладают кетогенным свойством. У жвачных, кроме того, из преджелудков в кровь может поступать избыточное количество аммиака, замедляющего реакции трикарбонового цикла, что стимулирует кетогенез. Накопление кетоновых тел, уменьшенное количество глюкозы, развитие ацидоза приводят к возникновению дистрофических процессов в паренхиматозных органах, нарушению функций центральной нервной системы. Больные животные отличаются снижением аппетита, нервными расстройствами с первоначальным возбуждением и последующим угнетением, падением молочной продуктивности, прогрессирующим истощением. Кетоновые тела преодолевают плацентарный барьер, поэтому новорожденные телята от больных кетозом коров недостаточно жизнеспособны, склонны к токсической диспепсии. Нарушение моторной функции преджелудков. Пищеварение в преджелудках жвачных обеспечивается не только симбионтными микроорганизмами, но и последовательными сокращениями сетки, книжки, рубца. В результате сокращений кормовые массы перемешиваются, пропитываются слюной и питьевой водой, частицы корма разволокняются, мацерируются. Механическая обработка корма происходит на фоне непрекращающихся биохимических процессов. Координация сложных движений преджелудков осуществляется блуждающим нервом, в составе которого проходят афферентные и эфферентные волокна. Генерируют возбуждение рецепторы растяжения — тензиорецепторы. Дорсальные ядра блуждающих нервов в продолговатом мозгу представляют собой основной центр регуляции моторики преджелудков. Помимо вагусных влияний на моторику воздействуют адренергические структуры преджелудков, биологически активные вещества. Участвуют в регуляции моторики кора головного мозга и подкорковые образования (ретикулярная формация, гипоталамус и др.). Расстройство моторики преджелудков связано прежде всего с гипотонией и атонией рубца, что приводит к быстрому накоплению газов — тимпании. Вздутие рубца — тимпания (от греч. tympanon — барабан). Болезнь жвачных животных, характеризующаяся чрезмерным скоплением газов в рубце. Избыточное скопление газов может быть результатом усиленного газообразования и их недостаточного выведения, в других случаях возникает только как следствие прекращения отрыгивания газов, образующихся при естественных бродильных процессах. Наиболее часто болеют крупный рогатый скот и овцы, реже — козы. Болезнь возникает спорадически или приобретает массовый характер. Причиной заболевания может быть обильное поедание легкобродящих кормов, таких, как клевер, люцерна, трава, покрытая росой или инеем, смоченная дождем, скошенная и пролежавшая в валках, капустные и свекольные листья, отходы зерна. Заболевание может возникнуть при резком переходе от одного корма к другому, от стойлового содержания к пастбищному, от скармливания заплесневевших, прокисших, промороженных кормов. Особое значение придают образованию в преджелудках пенистых масс, появление которых объясняют наличием сапонина и цитоп-лазматических протеинов, содержащихся в бобовых растениях. Вещества типа сапонинов стимулируют бурное развитие микроорганизмов, продуцирующих слизь, которая повышает вязкость содержимого рубца и образование устойчивой пены. Обильное ценообразование в кормовой массе рубца и сетки не обеспечивает раздражения рецепторного аппарата, приводит к частичному или полному блокированию нервно-рефлекторного механизма отрыгивания. Слюна, содержащая муцин, тормозит пенообразование. Поэтому факторы, понижающие рефлекс слюноотделения (отсутствие сухого, грубого корма), способствуют развитию тимпании. На выведение газов влияет уровень стояния жидкой массы в руб- це, оно затрудняется, если этот уровень расположен выше входного отверстия пищевода. Тимпания нередко возникает как следствие полной или частичной закупорки пищевода инородными телами, при сужениях, эктазиях, дивертикулах пищевода, опухолях типа папиллом, фибром, сарком. Выведение газов из рубца может быть результатом расстройства актов отрыжки и жвачки на почве нарушения проводимости блуждающего нерва. Переполнение рубца газами и кормовыми массами ведет к рефлекторному изменению деятельности внутренних органов. Развивается тахикардия, дыхание становится учащенным, поверхностным, развивается цианоз слизистых оболочек, дефекация прекращается. Животные стонут, топчутся на месте, изгибают спину, часто оглядываются на живот. Переполненные газом преджелудки оказывают механическое давление на диафрагму, легкие, сердце. Возникающая гипоксемия усугубляется интенсивным всасыванием газов из желудочно-кишечного тракта в кровь. В случае отсутствия квалифицированной помощи (прокол рубца, выведение пенистых масс через пищеводный зонд) животное погибает от асфиксии. Хронически протекающая тимпания проявляется умеренным вздутием рубца, возникающим после очередного кормления, с расстройствами функции преджелудков. Заболевание наблюдают у взрослых животных и молодняка, оно может появляться спорадически или носит массовый характер (безоарная болезнь овец). Развитие болезни определяется стойким нарушением проходимости пищевода за счет сдавливания увеличенными лимфатическими железами (лейкоз, актиномикоз), опухолями, за счет спаек сетки и рубца с диафрагмой (травматический ретикулит). Наличие спаек затрудняет перистальтику, перемешивание кормовых масс, их перемещение в ротовую полость для пережевывания и эвакуации в нижележащие отделы. Описанные и другие причины создают периодическое несоответствие между уровнем газообразования и темпом отрыгивания газов. Часть их остается в рубце, вызывая умеренное вздутие. Это ведет к нарушениям активности бактерий и простейших, образованию и всасыванию продуктов ферментации кормовых масс. Снижается их питательная ценность. Неэффективное использование кормов, хроническая аутоинтоксикация приводят к задержке роста молодняка, снижению продуктивности (мясной, шерстной, молочной), кахексии. Не исключена гибель животного после очередного приступа тимпании, перешедшей из хронической в остро протекающую. Травматический ретикулит. Воспаление стенки сетки, возникающее в результате травмирования острыми предметами. Ретикулоперитонит — воспаление стенки сетки с переходом патологического процесса на брюшину. Инородный колющий предмет способен перфорировать сетку, диафрагму, поражать легкое, ткани сердца (травматический перикардит, травматический миокардит), печень, селезенку. Болеют крупный рогатый скот и очень редко овцы, козы. Непосредственная причина травматических поражений сетки и близлежащих органов — различные инородные тела, проглатываемые вместе с кормом. Сведения о природе таких тел, обнаруживаемых в преджелудках жвачных, многочисленны. Заболевание вызывают проглоченные куски проволоки, гвозди, швейные иглы, вязальные спицы и крючки, другие инородные предметы. Заболеваемость животных значительно повышена в тех хозяйствах, где; скот выпасается вблизи промышленных предприятий, помойных ям, свалок мусора, печной золы. Крупный рогатый скот плохо пережевывает корм и быстро его проглатывает. Попаданию инородных тел способствуют недостаточное и нерегулярное кормление, невысокая чувствительность слизистой оболочки ротовой полости, обилие сосочков, направленных в сторону глотки. Инородные тела, в том числе колющие, попадают в преджелудки быков, коров, телят при извращенном аппетите, особенно вызванном минеральным и витаминным голоданием. У коз и овец травматический ретикулит бывает очень редко, так как они пережевывают корм более тщательно, проглатывают его малыми порциями; у этих животных более чувствительная слизистая оболочка, что позволяет им обнаружить инородное тело и выбросить его изо рта. Степень повреждения внутренних органов зависит от характера предмета, вызывающего травму, места внедрения, силы сокращения сетки. Причиняемая острыми предметами рана инфицируется микроорганизмами содержимого преджелудков. Развивается гнойное и купируемое, если инородное тело (короткий гвоздь) не вышло за пределы стенки книжки, воспаление. Однако оно может распространиться на те органы, которые были повреждены перфорирующим стенку сетки более травматичным предметом. Развитие воспаления в последнем случае сопровождается образованием спаек из плотной рубцовой ткани. Спайки механически затрудняют перистальтику преджелудков. Развитию гипотонии и атонии способствует рефлекторное торможение сократительной активности преджелудков, исходящее из травмированной ткани сетки и рецепторов брюшины. Одновременно с ослаблением моторики преджелудков возникает гипотония кишечника. Заболевание может протекать остро, но чаще оно хроническое и сопровождается периодически возникающими случаями обострения. Больное животное худеет, продуктивность существенно снижена, аппетит ослаблен, нарушено отрыгивание жвачки. Острые и хронические травматические ретикулит, ретикулоперитониты, осложняются периодически возникающим вторичным вздутием (тимпанней) рубца. В последние годы у крупного рогатого скота все больше регистрируют расстройства моторной функции преджелудков, вызванные скоплением в них инородных предметов типа целлофана, полиэтилена, резины, тряпок и особенно шпагата из синтетического волокна, которым заменили металлическую проволоку, укрепляющую тюки сена и соломы. Вместе с грубым кормом шпагат попадает в кормушки; животные захватывают его, длительно пережевывают И заглатывают. Нарушается проходимость преджелудков, расстраивается пищеварение. Клинические признаки такой патологии выражены слабо. Течение хроническое, проявляется плохой поедаемостью корма, резким снижением упитанности, молочной продуктивности. 18.6. НАРУШЕНИЯ ФУНКЦИЙ ЖЕЛУДКА . Пищеварение в сычуге жвачных и желудке моногастричных животных осуществляется их секреторной и моторной функция ми. Секреторная функция обеспечивает дальнейший гидролиз компонентов корма, моторная — перемешивание и эвакуацию содержимого в кишечник. Помимо пищеварительной желудок выполняет и другие функции: всасывательную, инкреторную, экскреторную. Нарушение секреторной функции желудка. В составе секрета желудочных желез здоровых животных содержатся эндопептидазы — пепсин, ренин (химозин), хлористоводородная кислота (НС1), небольшое количество желудочной липазы. Содержание хлористоводородной кислоты, переводящей пепсиноген в активный пепсин, зависит от вида животных, возраста, индивидуальных особенностей, характера принимаемого корма, состояния внутренней и внешней среды. У лошадей количество свободной хлористоводородной кислоты в составе желудочного сока равно 0,12—0,22 %, у коров 0,10—0,12 %, тогда как у плотоядных (собак) ее значительно больше — 0,5—0,6 %. Основные секреторные нервы — блуждающие, их перерезка при «мнимом кормлении» ведет к прекращению отделения желудочного сока. Патологические процессы в желудке (воспаления, эрозии, опухоли) сопровождаются количественными и качественными изменениями секреции. Секреторная функция может быть усиленной (гиперсекреция) или ослабленной (гипосекреция). Расстройство секреторной функции проявляется также в повышении кислотности (гиперацидис), понижении ее (гипоацидис) или полном прекращении отделения хлористоводородной кислоты (анацидис), которое может сочетаться с отсутствием ферментов (желудочная ахилия). Возможно сочетание количественных и качественных показателей секреции, отражающихся на переваривающей активности желудочного сока. Гиперсекреция (от греч. hyper — над, сверх, secretio — выделение) сопровождается, как правило, повышением кислотности и переваривающей способности желудочного сока. Причиной патологически усиленного сокоотделения может быть воспаление слизистой оболочки желудка — гипертрофический гастрит, повышение возбудимости секреторного нерва за счет висцеро-висцеральных патологических рефлексов, поражений центральных отделов нервной системы функционального и органического происхождения. Так, недостаточное образование нейросекрета гипоталамуса — соматостатина приводит к избыточному синтезу гастрина, который, в свою очередь, стимулирует образование хлористоводородной кислоты, повышает ее концентрацию в желудочном соке. Изначальная гиперсекреция и гиперхлоргидрия сопровождаются появлением компенсаторных реакций, направленных на нейтрализацию хлористоводородной кислоты. Ингибируется секреция гастрина, увеличивается выброс бикарбонатов со слизью, забрасывается в желудок содержимое двенадцатиперстной кишки, имеющее щелочную реакцию. Повышение проницаемости сосудов стенки желудка приводит к усиленной транссудации жидкости в его полость, ведущей к снижению концентрации хлористоводородной кислоты. Негативные последствия гиперсекреции желудочного сока и гиперхлоргидрии сводятся к задержке содержимого в желудке из-за более длительной нейтрализации пищевого комка в двенадцатиперстной кишке. Спазм привратника затрудняет перемещение химуса из желудка в кишечник. Он подвергается интенсивной ферментации, ослабляются его свойства раздражать механорецепторы желудка и кишечника. Возрастание переваривающей силы желудочного сока, сочетающейся со снижением активности обкладочных желез по образованию слизистого секрета, способно вызвать эрозивные поражения стенок желудка. Кроме того, возможно забрасывание кислого содержимого желудка в кардиальную часть пищевода, появление там септических язвенных поражений. Гипосекреция, ахлоргидрия, ахилия (отсутствие желудочного сока) сопровождают атрофические формы хронического гастрита, характеризующиеся структурными перестройками железистого аппарата, доброкачественные и злокачественные новообразования. Причины угнетения секреции желудочного сока не сводятся только к последствиям хронических гастритов, опухолей. Снижение секреции и переваривающей силы желудочного сока может быть функционального происхождения. Гипосекрецию наблюдают при лихорадке, многих инфекционных заболеваниях, обезвоживании различного генеза, белковой, витаминной недостаточности, снижении тонуса блуждающего нерва, гиперсекреции слюны. Ахлоргидрия сопровождается тяжелыми для организма последствиями. Недостаточность пищеварения при этой патологии определяется падением активности пепсина, неспособностью желудочного сока переваривать белки. В отсутствие хлористоводородной кислоты начинаются процессы брожения и гниения. Нейтрализация желудочного содержимого в двенадцатиперстной кишке происходит очень быстро, привратник открыт. Ускоренная эвакуация из желудка в кишечник недостаточно обработанного химуса ведет к перераздражению механорецепторов, усилению перистальтики. Недостаток или отсутствие хлористоводородной кислоты, пепсина ведет к проникновению эндогенной микрофлоры в кишечник, развитию дисбактериоза, инфекционно-токсическому поражению желудочно-кишечного тракта, явлениям диспепсии. Недостаточность хлористоводородной кислоты тормозит продукцию секретина, поджелудочная железа не получает достаточного стимула для секреции ферментов. Нарушение двигательной функции желудка. Моторная функция желудка обеспечивается мышечным тонусом, т. е. способностью его стенок обжимать содержимое, перистальтикой гладких мышц и эвакуацией кормовой массы в двенадцатиперстную кишку. Регулируется двигательная функция нервно-рефлекторным путем посредством волокон блуждающего нерва, усиливающего перистальтику, и симпатическим, понижающим силу и ритмичность сокращений. Аналогично симпатическому влиянию проявляют свое действие адреналин и норадреналин. Помимо катехоламинов на двигательную функцию желудка существенно влияют кислотность, интестинальные полипептиды, гистамин, другие факторы гуморальной регуляции. Нарушение двигательной функции желудка сопряжено с усилением перистальтики (гиперкинез) или снижением моторики (гипокинез). Усиление перистальтики и эвакуаторной функции желудка обусловлено чаще всего гипохилией или ахилией. Быстрая нейтрализация пищевого комка в двенадцатиперстной кишке сопровождается реализацией энтерогастрального рефлекса, направленного на раскрытие привратника, сокращение желудка и поступление внеочередной порции содержимого в тонкий кишечник. Возрастание тонуса стенок желудка наблюдают также при язвенной болезни, гастритах, висцеро-висцеральных патологических рефлексах. Особенности желудочного пищеварения у сельскохозяйственных животных разных видов накладывают свой отпечаток и на расстройство моторной функции этого полого органа. Так, у лошадей острое переполнение желудка кормовыми массами (зерно ячменя) сопровождается перерастяжением стенок, спастическим сокращением гладких мышц, симптомокомплексом колик. Эвакуация содержимого становится невозможной. Разбухающее зерно и рефлекторный гиперкинез способны привести к разрыву желудка, перитониту, скоропостижной смерти животного. Снижение двигательной активности и эвакуаторной способности желудка наблюдают при повышении кислотности желудочного сока. Избыточное количество хлористоводородной кислоты в содержимом желудка, поступившем в кишечник, более длительно нейтрализуется и, таким образом, тормозится рефлекторное раскрытие желудочного сфинктера. Эвакуация очередной порции химуса в двенадцатиперстную кишку задерживается. Существенное значение в ослаблении эвакуаторной функции желудка имеет сужение пилоруса. Оно может быть функционального (пилороспазм) или органического происхождения, результатом гипертрофического гастрита, доброкачественных (полипоз, липома) или злокачественных опухолей. У собак встречается заворот желудка, появляющийся после быстрых движений животного (преодоление препятствий, дрессировка). Заболевшие собаки угнетены, наблюдаются вздутие желудка, болезненность при пальпации. Без квалифицированной помощи (срочная операция) собака гибнет. Жвачные животные (овцы, крупный рогатый скот) страдают безоарной болезнью, существенно затрудняющей перистальтику и эвакуацию содержимого. У телят, в частности, нередко обнаруживают три вида безоаров: комки и шары из волос (пилобезоары), остатков растительного корма (фитобезоары), крупные казеиновые сгустки (лактобезоары). Лактобезоары появляются в раннем постнатальном периоде после обильного принятия молозива. Перевариваются они медленно, неделями и месяцами, вызывая атрофию слизистой оболочки, язвенные поражения, токсикоз. Попавшие в сычуг телят, ягнят комочки шерсти, волос, грубые остатки растений образуют сетку, в которой застревают грубые остатки из непереваренного корма. Перистальтическими движениями они скатываются в комочки — безоары. Они могут вклиниться в пилорическую часть сычуга, создавая непроходимость, вызывая резкие спастические боли и скопление газов. Тимпания сычуга ведет к интоксикации и асфиксии. У взрослого рогатого скота (дойных коров) наблюдают левостороннее или правостороннее смещение сычуга. Различают паралитическую (плоские язвы, хроническая ацетонемия) и механическую (проглатывание больших количеств жома) формы заболевания. В том и другом случае возможен заворот сычуга с поворотом вокруг своей оси до 450°. Смещение и заворот завершаются вздутием как самого сычуга, так и рубца. Аппетит и дефекация у больных животных отсутствуют. Прогноз неблагоприятный. Язвенная болезнь желудка и двенадцатиперстной кишки. Язвенная болезнь — хроническое рецидивирующее заболевание, проявляющееся очаговым морфологическим дефектом слизистой оболочки желудка и двенадцатиперстной кишки, воспалительной реакцией окружающей ткани, расстройством пищеварения. У здоровых животных равновесие между агрессивными кислотами — пептическими факторами и защитными механизмами слизистой оболочки желудка и кишечника обеспечивают стабильность пищеварения, сохранность слизистой оболочки. Ведущую роль в защите от кислотно-пептических факторов и экзогенных агрессивных воздействий играет бикарбонатный барьер. Защита обеспечивается:
К агрессивным факторам, приводящим к деструкции слизистой оболочки, относят хлористоводородную кислоту, кислые пептидазы, компоненты желчи, дисмоторику желудка и кишечника и, как выявлено в последнее время, геликобактер пилори (Helicobacter pylori) — группа бактерий, заселяющих клетки слизистой оболочки и обкладочных желез желудка. Обнаружение этих спиралевидных бактерий привело к фундаментальным изменениям в понимании природы желудочных болезней, в том числе язвенной. Развитие язвенной болезни — следствие нарушения естественного равновесия между факторами агрессии, воздействующими на слизистую оболочку, и факторами ее защиты. Нарушение этого равновесия и возникновение заболевания зависят от многих причин, среди которых можно выделить основные:
К настоящему времени установлено, что большинство (85— 100 %) гастродуоденальных язв у человека связано с инфицированием Helicobacter pylori. Эти грамотрицательные спиралевидные бактерии паразитируют в слизи, легко передвигаются в вязкой среде, формируют в области дна желудка колонии, нарушают баланс между клетками, производящими соматостатин и гастрин, вызывают повышенную секрецию гастрина и соответственно хлористоводородной кислоты. Патогенное действие Helicobacter pylori осуществляют с помощью уреазы, которая трансформирует мочевину до аммиака и углекислого газа. Аммиак блокирует окисление в митохондриях, угнетает клеточную репродукцию, оказывает прямое цитотоксическое действие. Протеазы и липазы, выделяемые микроорганизмами, нарушают целостность и вязкость желудочной слизи, открывают доступ к эпителию слизистой оболочки хлористоводородной кислоты и пепсина. Существует предположение и о том, что антитела к Н. pylori и обкладочным клеткам — главные «виновники» энтеропатий, к которым относят гастрит, язвенную болезнь и рак желудка. Найдено, что образующиеся иммуноглобулины высокоспецифичны, не дают перекрестных реакций. Снижено число Т-лимфоцитов, увеличено число недифференцированных лимфоидных клеток; накопление противо-t желудочных антител способствует хронизации процесса. Изучение взаимосвязи Helicobacter с язвенной болезнью животных пока существенно осложнено паразитированием у каждого из них нескольких видов этих бактерий. Так, у собак выявлено 4 вида, у кошек — 3. Не исключено, что широкое распространение этой инфекции у собак, кошек, других животных может служить резервуаром для последующей передачи возбудителя людям. Эксперименты по изысканию вакцин против инфекции Helicobacter, проведенные на мышах, зараженных Н. felis, оказались успешными как по профилактике, так и по устранению имеющейся инфекции. Острое течение язвенной болезни проявляется у животных сильной болевой реакцией, рвотой, часто с примесью крови, особенно у больных собак, пушных зверей. Аппетит снижен или отсутствует. Запоры могут чередоваться с поносами, причем в фекалиях обнаруживается кровь. Больные худеют, резко снижаются рост молодых животных, продуктивность у взрослых. При язвенной болезни могут быть осложнения, наиболее частое из них — кровотечение. Оно проявляется кровавой рвотой, темным цветом каловых масс, анемией, общей слабостью. Однако наибольшую опасность представляет перфорация стенки желудка или двенадцатиперстной кишки. Содержимое этих полых органов попадает в брюшную полость, развивается прогрессирующей перитонит. Возможна пенетрация — распространение процесса в толщу соседнего органа, т. е. печени, поджелудочной железы, сальника. Так, перфорация медиальной стенки сычуга у крупного рогатого скота сопровождается поступлением его содержимого в полость сальника и завершается ограниченным перитонитом. На месте зажившего язвенного дефекта слизистой оболочки формируется рубец, ведущий к деформации стенок и стенозу. У свиней чаще выявляют эрозивные поражения слизистой оболочки желудка. 18.7. НАРУШЕНИЯ КИШЕЧНОГО ПИЩЕВАРЕНИЯ Пищеварение в кишечнике здоровых животных обеспечивается его секреторной, моторной, всасывающей, экскреторной и инкреторной функциями. Кишечное пищеварение осуществляется путем внутриполостного и пристеночного гидролиза белков, жиров и углеводов корма. Внутриполостное пищеварение определяется энзимами поджелудочной железы, кишечного сока, желчью, ферментативной активностью симбионтной микрофлоры. Мембранный гидролиз осуществляется ферментами энтероцитов. Нарушение секреции поджелудочной железы. Причины нарушений внешней секреции поджелудочной железы: затруднение выведения панкреатического сока в двенадцатиперстную кишку из-за сдавливания протока извне или его закупорки; уменьшение образования секретина, стимулирующего продукцию ферментов; снижение тонуса секреторного блуждающего нерва; поражение железы воспалительным процессом (острые, хронические панкреатиты), опухолью; аллергические и аутоаллергические реакции; острые отравления (свинец, ртуть, фосфор). Расстройство пищеварения определяется дефицитом ферментов, входящих в состав панкреатического сока. Протеазы поступают в кишечник в неактивной форме. Энтерокиназа, содержащаяся в кишечном соке, активирует трипсиноген, превращает его в активный фермент — трипсин. Трипсин, в свою очередь, превращает остальные пептидазы (химотрипсин, эластаза, карбоксипептидаза, калликреин) в активные формы. Недостаток протеолитических ферментов поджелудочной железы снижает эффективность использования белков корма, до 60—70 % непереваренного протеина выводится из организма. Отсутствие или недостаток поджелудочной липазы приводит к тому, что значительная часть жира не усваивается и выделяется с фекальными массами (стеаторея). Недостаточное содержание амилазы ведет к потере крахмала, его непереваренные зерна обнаруживаются в фекалиях больных животных. Затруднение в выходе секрета, повышение давления в протоке поджелудочной железы, попадание туда желчи, содержащей энтерокиназу, могут привести к самоперевариванию (аутолиз) ткани железы активированными протеолитическими ферментами. Аутолиз ткани железы сопровождается образованием большого количества биологически активных веществ, поступающих в кровоток. Пептидазы, кинины, лизолецитин, другие соединения вызывают тяжелые расстройства нервной регуляции, сердечной деятельности, гемодинамики, дыхания, приводящие к панкреатическому шоку. Нарушение выделения желчи. Функции желчи многообразны. В ее состав входят желчные кислоты (холевая, хенодезоксихолевая), желчные пигменты (билирубин), жирные кислоты, холестерин, лецитин. Желчеобразование стимулирует блуждающий нерв и гуморальные факторы — гастрин, секретин, хлористоводородная кислота, прием богатого белками и жиром корма. Активация симпатического нерва и голодание тормозят образование и выведение желчи. К этиологическим факторам, определяющим недостаточное поступление желчи в кишечник, относят воспаление желчного пузыря (холецистит), дискинезию желчных протоков, желчнокаменную болезнь, гепатит, гепатоз, цирроз печени. Затруднения в оттоке желчи могут возникнуть из-за сдавливания выводящих путей опухолями, наличия в их просвете паразитов (фисциолез крупного рогатого скота, описторхоз плотоядных). Снижение выделения желчи (гипохолия) или полное прекращение ее поступления в кишечник (ахолия) приводят к нарушениям кишечного пищеварения. В наибольшей степени расстраивается усвоение жира. Он не подвергается эмульгированию желчными кислотами, поджелудочная липаза не активируется, жирные кислоты не образуют с желчными кислотами водорастворимых комплексов. Организм не получает необходимого количества липидов, жирорастворимых витаминов, холестерина. Недостаток желчи негативно сказывается и на усвоении белка, углеводов. Клеточная мембрана представляет в своей основе билипидный слой, поэтому белки и углеводы без разрушения мембран не могут быть объектом воздействия протеолитических и амилолитических ферментов. Кроме того, желчь, нейтрализуя желудочное содержимое, поступившее в кишечник, создает оптимальные условия для ферментов дуоденального сока, ее недостаточность ингибирует активность протеаз и амилаз. Дефицит желчи негативно отражается на пристеночном пищеварении, поскольку снижена адсорбция энтероцитами ферментов химуса. Желчные кислоты, воздействуя на хеморецепторы, стимулируют перистальтику и обладают бактерицидностью. Гипо- и ахолия сопровождаются гипокинезией кишечника, усилением процессов брожения, гниения, газообразования. Развивается интоксикация. Нарушение секреторной функции кишечника. В просвет кишечника выделяют свои секреты брюннеровы железы, расположенные в подслизистой оболочке двенадцатиперстной кишки, либеркюновые железы и бокаловидные клетки. Основными же источниками ферментов кишечного сока являются эпителиоциты слизистой оболочки. Слущиваясь с вершины ворсинки, они представляют собой комок слизи с обилием энзимов: пептидаз, гликозидгидролаз, кишечной липазы, щелочной фосфатазы, энтероки-назы. Переваривающая способность кишечного сока и активность отдельных ферментных систем имеют возрастные и видовые особенности. Так, активность кишечной мальтазы у жвачных почти в 50 раз ниже, чем у свиней. Молодняк млекопитающих остро переносит недостаток лактазы — фермента, обеспечивающего гидролиз молочного сахара — лактозы. Этот дефект наблюдают у гипотрофичных, физиологически незрелых молодых животных (телят, поросят). Лактоза становится достоянием микрофлоры толстого кишечника, ферменты которой гидролизуют молочный сахар до молочной, пировиноградной, уксусной кислот. Эти кислоты осмотически активны. Их появление в избыточном количестве способствует развитию диареи, интоксикации организма. Недостаток «фермента ферментов» энтерокиназы ингибирует превращение трипсиногена в трипсин, сказывается на усвоении белка организмом. Полостное кишечное пищеварение обеспечивает разрушение тканевых и клеточных структур корма, разрыв химических связей в молекулах биополимеров. Образовавшиеся промежуточные продукты элиминируются в зону щеточной каймы энтероцитов, на мембранах которых гидролиз завершается образованием конечных продуктов, чаще всего в виде мономеров. Этот процесс получил название мембранного (пристеночного) пищеварения. На мембранах энтероцитов молекулы передаются с гидролитических на транспортные системы кишечной клетки. Оттуда они поступают в лимфатические и кровеносные сосуды ворсинки, а, затем в общий лимфо- и кровоток. Таким образом, гидролиз завершается всасыванием. Ферменты, участвующие в пристеночном пищеварении, двоякого происхождения. Одни из них, преимущественно панкреатические, адсорбируются на поверхности щеточной каймы (альфа-амилаза, липаза, трипсин, химотрипсин, эластаза), другие ферменты — энтерального происхождения. Поэтому дефекты мембранного гидролиза и последующего транспорта (всасывания), зависят от количества и активности ферментов панкреатического: сока, а также от патологических изменений структуры и ультраструктуры кишечной поверхности. Такие изменения обнаружены, у животных после оперативных вмешательств на желудочно-кишечном тракте, при кишечной непроходимости, заболеваниях печени, многих инфекционных болезнях и болезнях паразитарного происхождения. Существенно нарушаются мембранное пищеварение и всасывание при лучевой патологии, воздействии эмоционального стресса, гиповитаминозах, нарушениях обмена веществ. Так, обнаружено, что у коров, страдающих остеодистрофией, пептидазная активность слизистой оболочки существенно подавлена. У родившихся от них телят, больных диспепсией (простая и токсическая), значительно уменьшен синтез основных ферментов энтероцитами, снижена скорость транслокации энзимов на наружную поверхность мембраны кишечного эпителия. Показано, что: диспепсия у новорожденных телят обусловлена прежде всего нарушением мембранного пищеварения. Опытами на овцах выявлена регулирующая роль в мембранном пищеварении вегетативной нервной системы и ретикулярной формации мозга, стимулирующей или тормозящей процессы гидролиза в тонкой кишке. Заражение овец ассоциацией кишечных нематод трех родов сопровождалось ингибицией активности трипептидазы, мальтазы и щелочной фосфатазы при полисубстратном мембранном гидролизе. После дегельминтизации активность гидролаз повышалась. При многих заболеваниях нарушение во взаимоотношениях пищеварительных и транспортных функций эпителия тонкой кишки возникает в ее проксимальных отделах. Поражение последних, например, за счет токсических веществ, поступающих с кормом (соли тяжелых металлов), приводит к тому, что дистальная область как резервная зона становится главной в гидролизе и ассимиляции компонентов корма. Найдено, что период молочного питания у всех млекопитающих характеризуется редукцией резервной зоны и именно этот период является наиболее неустойчивым в пищеварении. Дистальная локализация многих кишечных ферментов в молочный период определяет повышенную чувствительность молодняка к некомпенсируемому дефекту пищеварительно-транспортных комплексов. Воспалительные процессы в кишке телят сопровождаются 2—3-кратным повышением гидролитической активности содержимого дистальной части тонкой кишки по отношению к проксимальной при противоположной тенденции у здоровых животных. Сопряженность гидролиза и транспорта в процессе мембранного пищеварения зависит не только от активности адсорбированных ферментов, транслокации энзимов на наружную поверхность мембраны микроворсинок энтероцитов, но и от ряда других факторов. К наиболее значимым следует отнести застойные явления, гипоксию, недостаточное восстановление макроэнергетических комплексов, повышенную проницаемость сосудистых стенок при энтеритах, снижение, усиление или отсутствие перистальтики кишечника, блокаду ферментов токсинами разного происхождения, аутоиммунные поражения энтероцитов, паразитозы, дисбактериоз и др. Нарушение двигательной функции кишечника. Перистальтические движения кишечника под влиянием различных причин могут усиливаться (гиперкинез), замедляться (гипокинез) или прекращаться (акинез). Нарушения моторной функции кишечника могут касаться и их сегментирующих (ритмичная сегментация, маятникообразные движения) сокращений, направленных на перемешивание содержимого. Ускорение перистальтики возникает под влиянием повышения тонуса эфферентных парасимпатических нервных волокон, стимулирующих моторику выделением медиатора ацетилхолина, взаимодействующего с вегетативными ганглиями и холинреактивными структурами гладких мышц кишечной стенки. Эта патологическая эфферентная импульсация — ответная реакция на эмоциональный стресс (диарея у рысистых лошадей, выходящих на старт), раздражение рецепторного аппарата слизистой оболочки грубыми, непереваренными частицами корма, продуктами избыточного брожения, гниения при дисбактериозе. Нередко причины ускоренной перистальтики кишечника у животных разных видов — инфекции, поражающие преимущественно желудочно-кишечный тракт, такие, как колибактериоз, паратиф, вирусный энтерит телят, парвовирусный энтерит собак и др. На почве инфекции, инвазии, поедания недоброкачественных кормов, расстройств нервной и эндокринной регуляций возникают энтериты (воспаление слизистой оболочки тонкого кишечника), колиты (воспаление слизистой оболочки толстого кишечника), гастроэнтериты, энтероколиты. Воспалительные процессы сопровождаются повышением двигательной функции кишок, ускорением перемещения их содержимого от проксимальной части к дистальной, ухудшением переваривания и всасывания, поносом (diarrhoea). Диарея характерна болевым синдромом за счет спазма и тонических сокращений кишечника, частой дефекацией жидкими фекальными массами. Усиление перистальтики и освобождение организма от токсических продуктов, поступивших с кормом или эндогенного происхождения, имеет защитное значение. Однако продолжительные поносы приводят к обезвоживанию организма, гиповолемии, аутоинтоксикации, снижению продуктивности, истощению. Особенно опасна диарея для молодняка сельскохозяйственных животных. Обезвоживание, потеря пластических и энергетических источников существования, электролитов, аутоинтоксикация нередко сопровождаются гибелью телят, поросят, ягнят, щенков собак, пушных зверей. Замедление перистальтики наблюдают как результат преобладания симпатической иннервации, усиленного выброса адреналина и норадреналина или понижения тонуса кишечной стенки. Поэтому возникающие запоры кишечника (constipatio intestini) подразделяют на спастические и атонические. Спастические запоры обусловлены длительным сокращением мышц кишечника под влиянием эмоционального стресса, депрессивных состояний, висцеро-висцеральных патологических рефлексов. Атонические запоры возникают чаще. Их происхождение может быть алиментарного характера: в связи с уменьшением количества принимаемого корма, недостатка клетчатки как физиологического раздражителя кишечных механорецепторов. Запоры сопровождают гиперсекрецию желудочного сока, гипо- или ахолию, перитонит, снижение аппетита, сопутствующее многим заболеваниям. Моделировать запоры можно введением животным атропина, настойки опия, денервацией кишечника. Замедление перистальтики сопровождается застоем содержимого в тонком или толстом кишечнике, снижением секреции кишечного сока, ингибицией его ферментативной активности и мембранного пищеварения. Вследствие длительного застоя содержимое кишечника обезвоживается, превращается в уплотненные массы. Такой процесс, происходящий в тонком кишечнике, получил название химостаза, а в толстом — копростаза. Копростазы часто наблюдают у лошадей в слепой, большой и малой ободочной кишках. Заболевание возникает как следствие длительного скармливания концентратов при ограничении грубых кормов. Кишечная непроходимость. Непроходимость кишечника — илеус (от греч. eileo — запираю, скручиваю) наблюдают у продуктивных животных всех видов. Заболевание характеризуется прекращением дистально-проксимального перемещения содержимого кишечника, его брожением и гниением с обильным образованием токсических, в том числе газообразных, веществ, болевым синдромом, аутоинтоксикацией. Рассматривают три формы непроходимости кишечника у животных: динамическую, механическую, тромбоэмболическую. Динамическая непроходимость обусловлена функциональными расстройствами нервно-мышечного аппарата кишечной стенки. Возможно развитие спастической формы как результат длительного сокращения мышечных элементов стенки кишок, в частности у лошадей при ревматической форме энтералгии. Противоположная форма динамической непроходимости — паралитическая. Паралич кишечных мышц возможен при перитонитах, травмах брюшной полости, оперативных вмешательствах на этих органах. Механическая непроходимость у животных встречается наиболее часто. Она может быть результатом закупорки (обтурации) просвета кишечника безоарами (рис. 30), уплотненным содержимым (химо- и копростаз), кишечными камнями, особенно у лошадей, паразитами (аскаридоз свиней), отечной тканью при воспалениях разного генеза, опухолью, гематомой стенки кишки. Механическим препятствием могут быть ущемленная в грыжевом мешке петля кишки, инвагинация, перекручивание кишок вокруг брыжейки, особенно у свиней, образование связок и соединительнотканных тяжей. Возможны врожденные аномалии развития, ведущие к непроходимости кишечника (отсутствие анального отверстия). Тромбоэмболическая (гемостатическая) непроходимость кишечника встречается как результат тромбоза или эмболии ее сосудов. Происхождение эмболов различно. Это могут быть личинки паразитов, опухолевые клетки, тромбические массы. У лошадей нередкая причина тромбоэмболической непроходимости — личинки делафондий, которые повреждают брыжеечные артерии. От образующегося рыхлого тромба легко отрываются частицы, током крови они переносятся в нижележащие артерии, вызывают их эмболию с последующим некрозом соответствующего сегмента кишки. Перистальтика прекращается, возникает непроходимость. 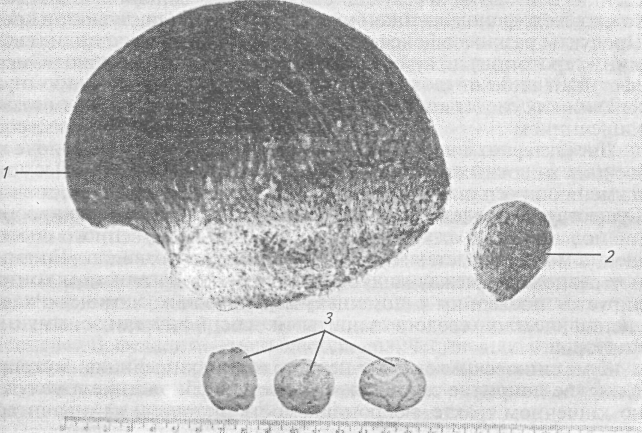 Рис. 30. Конкременты желудочно-кишечного тракта у животных: 1- распил пилоконкремента, извлеченного из желудка свиньи; 2- трихобензоар из сычуга овцы; 3- энтеролиты из кишечника лошади Патогенез кишечной непроходимости в начальной стадии развития обусловлен этиологическим фактором. Однако вслед за прекрашением перемещения содержимого кишок проявляются общие закономерности развития данного вида патологии. Содержимое кишечника выше места препятствия начинает подвергаться усиленному брожению и гниению. Образуется избыточное количество токсических продуктов, газов. Токсины раздражают рецепторные образования слизистой оболочки кишок, газы быстро ведут к перерастяжению кишечной стенки, раздражению бароре-цепторов. Патологическая импульсация перевозбуждает центральную нервную систему. Возникает ощущение резкой боли, проявляющееся у животных симптомокомплексом колик. Падает артериальное давление. Возможно развитие рвоты. При продолжающейся секреции кишечного сока всасывание резко снижается. Рвота ведет к потере воды, ионов калия, натрия, хлоридов, гидрокарбонатов. Обезвоживание сопровождается гиповолемией, гипотензией, аутоинтоксикацией. Потеря желудочного содержимого способствует развитию алкалоза, что усугубляет атонию. Непосредственно в очаге непроходимости прогрессирует ишемия в случае эмболии артерий или венозная гиперемия, обусловленная затруднением оттока крови и лимфы (тромбоз, заворот петли кишки). В том и другом случае гипоксия сопровождается повышением проницаемости сосудов пораженной кишечной стенки. В избытке образующиеся продукты гниения (индол, скатол, крезол, фенол, аммиак) из полости кишки поступают в кровь. Продукты развивающейся некротизации кишечной стенки (гиста-мин, серотонин) и аутолиза усугубляют интоксикацию. Смерть наступает либо от шока, вызванного интоксикацией, либо от асфиксии как следствия сдавливания легких переполненным газами кишечником. Дисбактериоз кишечника. В раннем постнатальном периоде кишечник животных заполняется микрофлорой. Ее состав, несмотря на меняющиеся условия внешней среды, относительно постоянен. Существует определенная закономерность расселения микроорганизмов в разных отделах кишечника и количественного соотношения между представителями микробов разных видов. Динамичное равновесие между микрофлорой и макроорганизмом контролируется последним с помощью механических, химических, неспецифических средств защиты и специфических иммунных факторов. К механическим относят перистальтику кишечника, мукопротеиновое покрытие эпителия, его быстрое обновление в желудочно-кишечном тракте, непроницаемость щеточной каймы энтероцитов. Химические факторы представлены хлористоводородной кислотой желудочного сока, пепсином, трипсином, желчными кислотами, кишечным соком. Местная защита кишечника включает в себя неспецифические факторы, такие, как лизоцим, комплемент, интерферон, лактоферрин, и специфические, обусловленные клеточными (Т-система) и гуморальными (В-система) факторами. В пищеварительном тракте присутствуют различные популяции иммунокомпетентных клеток. Очень важную роль играет секреторный иммуноглобулин A(IgA). Фактор колонизационной резистентности, способности сопротивляться колонизации кишечника условно-патогенными микроорганизмами представляет собой анаэробную флору, населяющую кишечник. Анаэробные бактерии, такие, как бифидобактерии и бактериоиды, контролируют состав условно-патогенных микроорганизмов (клебсиеллы, энтеробактер, протей, стафилококки и др.), которые, заселяя толстый отдел кишечника, могут являться основным источником эндогенной инфекции. К важнейшим для организма функциям нормальной (эубиотической) микрофлоры относят:
У 14-дневных телят общее число микроорганизмов в фекалиях было в 9,6 раза больше, чем у однодневных. Эти важнейшие функции микроорганизмов-симбионтов могут быть нарушены. Изменение нормальной флоры кишечника, ее качественных и количественных характеристик, мест обитания называют дисбактериозом. Дисбактериоз — ведущий синдром при многих формах патологии тонкого и толстого кишечника. Для дисбактериоза характерно увеличение содержания микроорганизмов в тонкой кишке с преобладанием эшерихий, лактобацилл, энтерококков, бактерий рода Klebsiella. В фекалиях уменьшается количество или отсутствуют совсем бифидобактерии, но существенно увеличивается количество стрептококков, стафилококков, протея, эшерихий, дрожжевых грибов, бактерий рода Klebsiella. Причинами дисбактериоза кишечника являются заболевания желудка (ана-, гипацидный гастрит), нарушение моторной функции кишечника (запоры, поносы, непроходимость), голодание (полное, неполное, частичное), лекарственные средства (антимикробные препараты, антибиотики), воздействие ионизирующей радиации, аллергия, воспалительные и инфекционные заболевания, повреждающие кишечник. Дисбиотическая микрофлора вызывает расстройство пищеварения, является источником всасывающихся токсических веществ, газообразных продуктов, вызывающих метеоризм. Метаболиты и токсины бактерий подавляют дезинтоксикационную функцию печени, повышают проницаемость кишечной стенки, ингибируют регенерацию эпителия, во многом определяют развитие диспептического синдрома. Дисбактериоз может какое-то время протекать бессимптомно, но при снижении общей резистентности, упадке защитных сил организма проявляются свойственные ему признаки. Выделяют следующие формы дисбактериоза:
По преобладанию того или иного вида микроорганизма рассматривают параколидисбактериоз, для которого характерно появление необычных, в том числе гемолизирующих, штаммов кишечной палочки; протейный, энтерококковый, стафилококковый, дрожжевой, ассоциированный, с участием нескольких условно-патогенных микроорганизмов, дисбактериозы. Дисбактериоз может быть первичным в кишечной патологии и вторичным. При первичном вначале активируется дисбиотическая микрофлора, а затем возникает воспаление слизистой оболочки кишечника. Вторичный дисбактериоз появляется как осложнение возникшего ранее заболевания (лучевая патология, аллергия) кишечника. Дисбактериоз сопровождается недостаточностью пищеварения, всасывания, интоксикацией, болевым синдромом. |
