учебник. Учебник ФЛ - Виноградов, Каткова 2016. Учебник для медицинских и фармацевтических учреждений среднего профессионального образования Под
 Скачать 5.41 Mb. Скачать 5.41 Mb.
|
ИммунодепрессантыПрепараты,угнетающиевызванныеантигеномкоопертивныереакцииим- мунных клеток, пролиферацию лимфоцитов, синтез антител; применяются для лечения тяжелых аутоиммунных заболеваний и подавления реакции отторжения трансплантата. Иммунодепрессанты (иммуносупрессоры) применяются в качестве средств патогенетической терапии тяжелых проявлений гипериммунных реакций, свя- занных с клеточным иммунитетом. Основная область их использова- * Вещества, после применения которых зафиксированы случаи смерти. ния — лечение ревматических заболеваний (коллагенозов): ревматоидного ар- трита, системной красной волчанки, узелкового периартериита, склеродермии; иммунных поражений ЦНС, почек и других аутоиммунных заболеваний; ряд пре- паратов применяется в хирургии для профилактики отторжения трансплантата при пересадке органов и тканей. В развитии реакций клеточного иммунитета основное значение принадлежит лимфоцитам (лф) (рис. 27). Благодаря большому количеству специальных рецеп- торов (порядка 108), лимфоциты очень точно распознают множество антигенов и обеспечивают специфический ответ иммунной системы. Важную роль в запуске кооперативного ответа иммунокомпетентных клеток играет особый медиатор — интерлейкин-1 (ИЛ-1), продуцируемый антигенпредставляющими клетками (в том числе моноцитами-макрофагами в процессе фагоцитоза и обработки анти- гена). ИЛ-1 активирует Т-помощников (хелперов), которые начинают вырабаты- вать специфические цитокины — лимфокины, главным образом интерлейкин-2 (ИЛ-2) — основной медиатор иммунной системы, участвующий во всех фазах им- мунного ответа, а также гамма-интерферон и др. Под влиянием ИЛ-2 происходит усиленная пролиферация исходных Т-лимфоцитов, образование специфических клонов этих клеток, в первую оче- редь Т-киллеров, обладающих высокой цитотоксичностью в отношении своих измененных и чужеродных клеток, а также Т-супрессоров, Т-помощников и др. ИЛ-2 способствует также пролиферации Влф, из которых образуются плазма- тические клетки, вырабатывающие антитела (иммуноглобулины) разных типов (M, G, A, D, Е). Последующее взаимодействие антигенов (циркулирующих в кро- 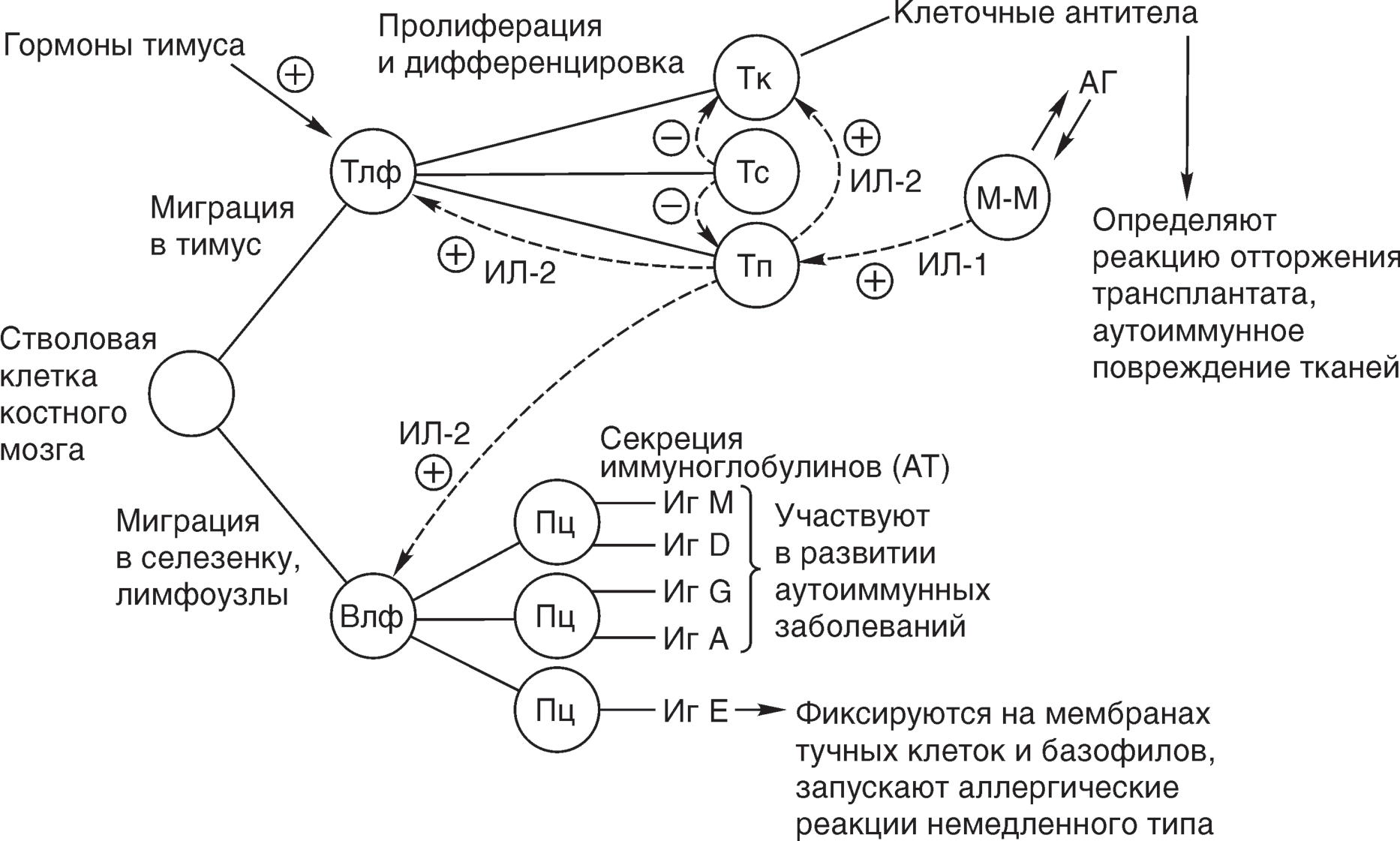 Рис.27.Схема формирования патологических иммунных реакций: М–М — моноцит—макрофаг; Тлф — тимусзависимые лимфоциты; Влф — тимуснезависимые лимфоци- ты; Тк — Т-лимфоциты-киллеры, или «убийцы»; Тс — Т-лимфоциты-супрессоры; Тп — Т-лимфоциты- помощники; Пц — плазмоциты («плазматические клетки»); Иг — иммуноглобулины (антитела); ИЛ — интерлейкины-1 и -2; АГ — антиген ви или тканевых) с иммуноглобулинами часто приводит к повреждению тканей разного характера (от обратимых функциональных изменений до хронического воспалительного процесса, лизиса и некроза) и возникновению аутоиммунных заболеваний. Действие иммунодепрессивных препаратов направлено на ключевые этапы клеточного иммунного ответа замедленного типа, поэтому они дают ощутимый терапевтический эффект. Умеренное иммунодепрессивное действие оказывают следующие пре- параты («малые иммунодепрессанты»): хлорохин (хингамин) и гидроксихлорохин (плаквенил); пеницилламин (купренил). Применявшиеся ранее в качестве иммунодепрес- сантов препараты золота в настоящее время не используются. Более сильным иммунодепрессивным эффектом («большие иммуноде- прессанты») обладают: цитостатики — азатиоприн(имуран),метотрексат,циклофосфамид; циклоспорин (сандиммун); глюкокортикоиды (преднизолони др.); моноклональные антитела — базиликсимаб, инфликсимаб и др. Иммунодепрессанты весьма токсичны и используются лишь при гипериммун- ных реакциях (различных аутоиммунных заболеваниях и др.) с тяжелым и сред- ней тяжести течением, когда возможности иной терапии исчерпаны, а риск про- грессирования болезни превосходит риск иммуносупрессии. Назначение имму- нодепрессантов производится только специалистом в соответствующей области медицины. «Малые иммунодепрессанты» — хлорохин и гидроксихлорохин (описаны как противомалярийные средства в соответствующем разделе) — препараты успешно применяются для лечения ревматоидного артрита, системной красной волчанки и других коллагенозов. Высокая эффективность препаратов при вялотекущих хро- нических воспалительных заболеваниях соединительной ткани аутоиммунной природы (коллагенозах) определяется их способностью подавлять клеточный и гуморальный иммунный ответ на разных этапах, а также воспалительный про- цесс преимущественно в фазе пролиферации. Хлорохин и гидроксихлорохин стабилизируют лизосомальные и клеточные мембраны, подавляют фагоцитарную функцию макрофагов, уменьшают секре- цию ИЛ-1 макрофагами и ИЛ-2 Т-лимфоцитами-помощниками, угнетают проли- ферацию Т-лимфоцитов, а также клеток соединительной ткани в ревматических очагах, нарушают образование коллагена. Пеницилламинспособен прямо взаимодействовать с ревматоидным фактором и разрушать его; кроме того, он нарушает созревание коллагена, замедляет про- лиферацию Т-лимфоцитов, образует комплексы с двухвалентными металлами (медь, железо, цинк, марганец и др.). Комплекс с медью нейтрализует активные радикалы кислорода, поддерживающие аутоиммунные процессы и воспаление. Многое в механизме иммунодепрессивного и противовоспалительного действия препаратов остается неясным. При ревматоидном артрите хлорохин и гидроксихлорохин несколько уступают по эффективности пеницилламину, но они менее токсичны и применяются при широком спектре ревматических заболеваний. Назначают их внутрь в таблетках. Терапевтический эффект развивается через 10—12 нед. ежедневного приема; ле- чение должно быть длительным (не менее 6 мес., обычно 1—2 года). Пеницилламин — одно из наиболее активных базисных средств терапии ревма- тоидного артрита. Наилучшие результаты отмечены у больных с высокой скоро- стью синтеза коллагена и повышенным уровнем специфических антител в плаз- ме. Назначается внутрь в капсулах по индивидуальным схемам; эффект достигает терапевтического пика спустя 9—15 мес. Пеницилламин относится к токсичным препаратам — может вызывать нарушение вкуса, тошноту, рвоту, понос, зуд, по- краснение кожи, повышение температуры, нарушение функции почек. «Большие иммунодепрессанты» применяются для лечения тяжелых, не поддающихся лечению другими препаратами форм ревматоидного артрита, си- стемной красной волчанки, других коллагенозов и аутоиммунных заболеваний; некоторые препараты используются для предупреждения реакции отторжения трансплантата после пересадки органов. Препараты из группы цитостатиков (азатиоприн, метотрексат, цикло- фосфамид)блокируют клеточное деление, в том числе Т- и В-лимфоцитов, тор- мозят синтез белков, включая антитела. Эти эффекты достигаются: в результате конкуренции с естественными пуриновыми основаниями ДНК и РНК (азатиоприн) и вытеснением их из биосинтеза; в результате антагонизма по отношению к фолиевой кислоте (метотрексат), принимающей участие в синтезе пуриновых и пиримидиновых нуклеотидов; «сшивками» спиралей ДНК в клетках (циклофосфамид) с нарушением про- цесса редупликации ДНК и клеточного деления. 2 Влияние препаратов этого ряда на разные этапы клеточного и гуморального иммунных ответов несколько различается. Лечебный эффект при лечении ревма- тических и других аутоиммунных заболеваний развивается довольно медленно и достигает пика спустя 1/ —2 года от начала терапии. Принципиальными недостаткамиэтихиммунодепрессантовявляются: общий цитотоксический эффект в отношении тканей с высоким темпом физиологической регенерации — они подавляют кроветворение и вызывают лей- копению, тромбоцитопению, анемию; нарушают регенерацию слизистой ЖКТ (изъязвление ЖКТ); выраженное подавление иммунитета — противовирусного, противогриб- кового, антибактериального и др. Довольно высока токсичность этих препаратов в отношении печени и почек. Циклофосфамид, кроме того, чаще других препаратов вызывает бесплодие, об- ратимое выпадение волос, тошноту и рвоту. Целесообразно сочетание таких иммунодепрессантов (со снижением дозировок) с НПВС (диклофенаком и др.), глюкокортикоидами, хлорохином. При этом удается добиться лучшей переносимости препаратов. Одновременно отмечается более силь- ное подавление местных иммуновоспалительных процессов в суставах, коже, почках. Азатиоприн — наиболее эффективный и менее токсичный иммунодепрессант, в большей степени подавляет Т-лимфоциты, чем В-лимфоциты, иногда применя- ется для подавления реакции отторжения трансплантата (тканевой несовмести- мости) при пересадке органов. К метотрексатуболее чувствительны В-лимфоциты, он сильнее нарушает образование антител, в малых дозах проявляет в большей степени противовос- палительный эффект, чем иммунодепрессивный. Метотрексат и циклофосфамид являются также активными противоопухолевыми средствами. Циклоспорин(сандиммун)считается иммунодепрессантом нового поколения, представляет собой антибиотик — циклический полипептид, состоящий из 11 ами- нокислот. Особенностью препарата является обратимое и избирательное угнете- ние клеточного иммунного ответа на ранних этапах. Он подавляет способность Т-лимфоцитов-помощников продуцировать ИЛ-2. В результате этого Т-клетки остаются в состоянии покоя, не образуются активные клоны Т-лимфоцитов, в первую очередь цитотоксических Т-киллеров, убивающих чужеродные в им- мунном отношении клетки пересаженных тканей. В отличие от цитостатиков, циклоспорин не подавляет кроветворение, пролиферацию клеток слизистой ЖКТ и других тканей. Применяется в основном для профилактики отторжения транс- плантата после пересадки костного мозга, почки, печени, сердца и других органов; возможно использование и при аутоиммунных заболеваниях. Препарат начинают вводить внутривенно капельно за 4—12 ч до операции трансплантации (при пересадке костного мозга исходную дозу вводят накануне операции). Продолжают внутривенные инъекции в течение 2 нед. Затем пере- ходят на пероральную поддерживающую терапию. Дозировки устанавливают индивидуально. Иногда комбинируют с глюкокортикоидами или другими имму- нодепрессантами. Циклоспорин обладает довольно высокой нефротоксичностью, может нарушать функцию печени. Глюкокортикоиды.Гормоны надпочечников и их синтетические аналоги (преднизолон,дексаметазон и др.) обладают выраженным и многосторонним иммунодепрессивным действием, которое может быть целью применения препа- ратов или крайне нежелательной и опасной побочной реакцией. Глюкокортикоиды подавляют функцию макрофагов, пролиферацию Т- (в большей степени) и В-лимфоцитов, тормозят их миграцию из мест формирова- ния (тимус, костный мозг) в кровь. Слабее других иммунодепрессантов угнетают кооперативный иммунный ответ и продукцию ИЛ-2. Снижают цитотоксичность Т-киллеров. В больших дозах подавляют синтез иммуноглобулинов плазматиче- скими клетками. Глюкокортикоиды обладают мощным и быстро развивающимся противовоспалительным действием, которое вносит существенный вклад в лечеб- ный эффект при аутоиммунных процессах. Применяют глюкокортикоиды в качестве иммунодепрессантов при ревмато- идных и других аутоиммунных заболеваниях, при пересадке органов и тканей для предупреждения отторжения трансплантата. В качестве средства, блокирующего реакцию отторжения при пересадке поч- ки, разработан и используется в трансплантологии препарат базиликсимаб, пред- ставляющий собой моноклональные антитела, которые избирательно взаимодей- ствуют с рецепторами ИЛ-2 на Т-лимфоцитах человека и инактивируют их, вслед- ствие этого тормозятся пролиферация Т-лимфоцитов, образование и активация Т-киллеров. Применяется базиликсимаб для предупреждения отторжения транс- плантата. Получение подобных препаратов достаточно сложно, и они слишком дороги для того, чтобы рассматривать их как средства широкого применения. Иммуностимулирующие средстваПрепараты, модулирующие клеточный и (или) гуморальный иммунитет и при- меняемые для лечения заболеваний, обусловленных недостаточностью иммунной системыилиеедисфункцией. Варианты дефицита и дисфункции иммунной системы многочисленны, и вы- явление природы и характера этих нарушений составляет одну из главных задач клинической иммунологии. Различные нарушения иммунитета являются показа- нием для лечения иммуностимулирующими средствами. В качестве иммуностимуляторов применяют: препараты гормонов тимуса (вилочковой железы) — тимуса эстракт (ти- малин, тактивин), альфа-глутамил-триптофан (тимоген); синтетические препараты — левамизол(декарис), бендазол(дибазол), изо- принозин, анаферон, глутоксим и др.; препараты бактериального происхождения — лизатов бактерий смесь (ри- бомунил, бронхо-мунал, имудон), ликопид; интерлейкины, интерфероны и индукторы синтеза интерферонов — гамма- интерферон, интерлейкин-1 (беталейкин), интерлейкин-2 (пролейкин, алдеслей- кин, ронколейкин). Препараты гормонов тимуса. Являясь центральным органом иммунной си- стемы, тимус вырабатывает несколько пептидных гормонов (порядка 8—10), ко- торые обеспечивают созревание лимфоцитов и регуляцию разных стадий иммун- ного ответа. Из тимуса получен ряд экстрактивных препаратов (тималин,так- тивини др.), содержащих комплексы тимических гормонов. Сейчас начато при- менение препаратов чистых гормонов тимуса — альфа-глутамил-триптофан (тимоген). При угнетении или дисфункции иммунной системы препараты тимуса восстанавливают нарушенную деятельность подобно стимулирующим гормонам тимуса. Активируются клеточный и Т-зависимый гуморальный иммунитет, фаго- цитоз, процессы регенерации тканей и кроветворения. Тималин и тактивин назначают при состояниях и заболеваниях, обусловлен- ных первичным или вторичным дефицитом иммунитета, в том числе при лечении остеомиелитов, хронического сепсиса, ожоговой болезни, трофических язв, про- лежней, лучевых поражений (некрозов) тканей, хронических вялотекущих вирус- ных, грибковых, микробных инфекций и т. п. Показаны они и для профилактики инфекционных осложнений в посттравматическом и послеоперационном перио- дах, в процессе проведения лучевой терапии и химиотерапии опухолей. Тималин вводят внутримышечно по 10—30 мг, курс лечения 5—20 дней. Тактивин более активный препарат, его вводят подкожно по 0,1—0,2 мг/сут или через день. Препараты тимуса не обладают антигенными свойствами, но у некоторых лю- дей могут давать аллергические реакции. Синтетические препараты свой иммуностимулирующий эффект реализуют, по-видимому, через мембранные рецепторы лимфоцитов, которые воспринимают различные влияния нейрогуморальной регуляции, в том числе гормоны тимуса. Левамизол (декарис) рассмотрен ранее как средство лечения аскаридоза (см. «Противоглистные средства»), однако основное значение для медицины имеет его иммуностимулирующее действие. Левамизол повышает чувствитель- ность иммунных клеток к гормонам тимуса, стимулирует систему клеточного и Т-зависимого гуморального иммунитета. Практически не влияет на нормальный иммунный ответ, но восстанавливает последний при его дефиците. Повышает фа- гоцитарную активность макрофагов, усиливает пролиферацию Т-лимфоцитов, выработку интерлейкинов и интерферонов. Назначается внутрь по 150 мг на при- ем (взрослым) после еды 1—2 раза в неделю; курс лечения от 2—3 нед. до 1 года. Препарат довольно токсичен, может вызывать желудочно-кишечные расстрой- ства, гриппоподобный синдром, бессонницу. Наиболее опасным осложнением яв- ляется агранулоцитоз. Бендазол(дибазол)широко применялся в прошлом в качестве спазмолити- ческого и антигипертензивного средства. Способность препарата стимулировать иммунные реакции была впервые показана Н. В. Лазаревым. Дибазол активирует неспецифическую резистентность организма, повышая фагоцитарную активность макрофагов, увеличивая синтез антител, интерферонов. Действие препарата раз- вивается медленно, поэтому его используют для профилактики, а не для лечения инфекционных заболеваний (гриппа и других ОРВИ в период эпидемий). Подобными свойствами обладает метапрот(см. «Психостимулирующие средства»). Его нормализующее влияние на иммунную систему обусловлено способностью активировать синтез белков и энергопродукцию в тканях, в том числе в клетках иммунной системы. Метапрот усиливает образование антител, Т-зависимые иммунные ответы, систему неспецифической иммунорезистентно- сти, особенно функцию макрофагов. В качестве иммуностимулятора использу- ется при лечении вирусных гепатитов, назначается пациентам, часто болеющим ОРВИ, рецидивирующей рожей и пиодермиями. Препараты бактериального происхождения относятся к числу неспе- цифических иммуностимуляторов. Лизатов бактерий смесь (рибомунил,имудон) стимулируют клеточный и гуморальный иммунитет, усиливают синтез интерфе- ронов, повышают неспецифическую резистентность организма. Увеличивают эф- фективность противомикробной терапии, в связи с чем используются при лечении инфекций у больных со сниженным иммунитетом (пневмонии, бронхиты, рини- ты, синуситы, остеомиелит, гнойно-некротические процессы и т. п.). Рибомунил назначают внутрь по 3 таблетки или в виде гранул, предварительно растворенных в воде (1 пакетик), 1 раз утром натощак курсом по схеме. Интерфероны (альфа-, бета-, гамма-) были рассмотрены как противовирус- ные средства. Из них интерферонгаммаотличается меньшим влиянием на тече- ние вирусной инфекции и значительной ролью в тонкой регуляции иммунных от- ветов. Он вырабатывается Т-лимфоцитами, стимулированными специфическими антигенами. Гамма-интерферон оказывает многогранное модулирующее влияние на клетки иммунной системы: повышает фагоцитарную активность макрофагов, усиливает действие Т-киллеров на инфицированные, поврежденные и опухоле- вые клетки; модулирует антителообразование; стимулирует выработку ряда бел- ков, обеспечивающих противовирусное состояние клеток, останавливающих син- тез ДНК и пролиферацию опухолевых и других клеток и т. д. Механизм действия интерферонов продолжает изучаться. Применяется интерферон гамма (ингарон)для лечения различных онкологи- ческих заболеваний, ревматоидного артрита, системной красной волчанки и дру- гих коллагенозов; при хронических вирусных (в том числе при гепатите В, С и D), грибковых и других инфекциях. Побочными эффектами являются кратковременное повышение температуры тела через 1—2 ч после внутривенного введения, кожные сыпи. В качестве иммуностимуляторов иногда используются индукторы интерфе- ронов (неовир,циклоферон,тилорони др. — см. «Противовирусныесредства»), усиливающие выработку эндогенных интерферонов (в основном альфа- и бета- типов) клетками организма. В стадии клинического изучения при врожденных и приобретенных иммуно- дефицитных состояниях, а также при лечении злокачественных опухолей нахо- дятся рекомбинантные интерлейкин-1 (беталейкин), интерлейкин-2 (алдеслей- кин,пролейкин)и ряд других медиаторов иммунной системы. Беталейкин уже сейчас с успехом применяется для поддержания механизмов иммунной защиты организма в хирургической практике, при химио- и радиотерапии опухолей. Показания к применению иммуностимулирующихсредств: хронические вялотекущие и рецидивирующие вирусные, грибковые и бак- териальные инфекции (тималин, левамизол, метапрот, интерфероны). Терапия на- правлена на усиление Т-зависимого гуморального иммунитета при его дефиците; злокачественные опухоли и опухолеподобные заболевания крови (тима- лин, левамизол, гамма- и иногда альфа-интерферон). Цель применения препара- тов — восстановить Т-киллерную систему иммунного «надзора». Разумеется, эти препараты не подменяют хирургических и иных методов лечения и предназна- чены для борьбы с метастазированием и профилактики рецидивов заболевания; ревматоидный артрит и другие коллагенозы (левамизол, тималин, гамма- интерферон). Применение иммуностимуляторов представляет собой новый подход к лече- нию этих заболеваний и является альтернативой назначения иммунодепрессан- тов (иногда их используют в чередующемся режиме). Иммуностимулирующим действием обладают некоторые препараты расти- тельного происхождения: из эхинацеи пурпурной (настойка эхинацеи, им- мунал), из корня солодки (сироп), из микроводоросли спируллины, а также расти- тельные адаптогены — препараты женьшеня, элеутерококка, золотого корня. Они активируют преимущественно клеточный иммунитет, стимулируют фагоцитарную функцию макрофагов, способствуют высвобождению интерферонов, повышают неспецифическую резистентность организма. Применяются для профилактики и лечения (в составе комбинированной терапии) простудных заболеваний, гриппа, инфекционно-воспалительных процессов в носоглотке и ротовой полости и т. п. Разработка иммуностимуляторов различного типа с прицельным действием на разные этапы физиологического иммунного ответа и неспецифическую рези- стентность организма — одно из важнейших и наиболее прогрессивных направле- ний фармакологии. Пока же набор средств, регулирующих иммунитет, и опыт их клинического применения ограниченны и тактика применения препаратов про- должает уточняться. |
