Важнейшие химические понятия и законы Химический элемент это определенный вид атомов с одинаковым зарядом ядра Атом
 Скачать 3.53 Mb. Скачать 3.53 Mb.
|
|
ВОПРОС 27 Понятие о растворах. Способы выражения концентрации растворов. Раствором называется твердая или жидкая гомогенная система, состоящая из двух или более компонентов, относительные количества которых могут изменяться в широких пределах. Концентрацией раствора называется содержание растворенного вещества в определенных массе или объеме раствора или растворителя. Чаще всего для выражения концентрации растворов используются следующие способы. М 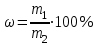 ассовая доля – число граммов растворенного вещества в 100 г раствора. ассовая доля – число граммов растворенного вещества в 100 г раствора.Молярная концентрация – число моль растворенного вещества на 1 литр раствора 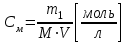 Эквивалентная (нормальная) концентрация – число моль эквивалентов растворенного вещества на 1 литр раствора. 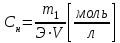 Титр раствора – число граммов растворенного вещества, содержащихся в 1 мл раствора. 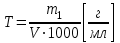 Молярная доля (хи) - отношение количества молей данного компонента к общему количеству молей всех компонентов. 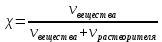 Все эти способы выражения концентрации связаны между собой следующим уравнением: 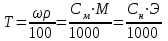 , где , гдеm1 – масса растворенного вещества, г, m2 – масса раствора, г. M – молярная масса, г/моль, V – объем раствора , л. Э – молярная масса эквивалентов, г/моль, ρ - плотность раствора, г/см3. 28. 29. осмос- процесс самопроизвольной односторонней диффузии растворителя к раствору через полупроницаемую перегородку. Перегонка-метод разделения жидких смесей на составные компания ,основанный на частичном испарении смеси с последующей конденсацией. Экстракция- метод разделения жидкой смеси на компоненты,основанной на добавлении растворителя с избирательной способностью.  30. 31. Сила электролита – условная характеристика, отражающая способность вещества диссоциировать на ионы. Сила электролита определяется по степени диссоциации. Электролиты принято разделять на две группы: сильные и слабые. У слабых электролитов степени диссоциации значительно меньше 100% (α < 3%). К ним относятся слабые неорганические кислоты (угольная, кремниевая, сернистая, азотистая и др.), большинство органических кислот, гидроксид аммония, гидроксиды d- и f- элементов, вода. Резкой границы между всеми перечисленными группами нет. Степень диссоциации (α) – это отношение числа, продиссоциировавших (распавшихся) молекул к общему числу молекул вещества, измеряется в долях единицы или в %: Степень диссоциации зависит от природы электролита, от температуры (при повышении температуры степень диссоциации в основном повышается), от концентрации раствора (чем меньше концентрация, тем больше степень диссоциации), от степени полярности молекул растворителя (чем больше полярность, тем выше степень диссоциации). Константа диссоциации – константа равновесия процесса электролитической диссоциации (т.е. выражение закона действующих масс для реакции диссоциации). Она представляет собой отношение произведения концентраций ионов к концентрации недиссоциировавших молекул. Например, для синильной кислоты, диссоциирующей по уравнению HCN → H+ + CN− выражение для Кд будет выглядеть так: Наряду со степенью диссоциации константа диссоциации может служить для оценки силы электролита: чем меньше значение Кд, тем хуже электролит в данных условиях распадается на ионы (т.е. тем он слабее). 32. Сила электролита – условная характеристика, отражающая способность вещества диссоциировать на ионы. Сила электролита определяется по степени диссоциации. Электролиты принято разделять на две группы: сильные и слабые. У сильных электролитов степени диссоциации больше 30%. К ним относятся подавляющее большинство солей щёлочи, сильные кислоты (серная, азотная, соляная, хлорная и др.). Иногда выделяют группу электролитов средней силы. Активность ионов (активная концентрация) (а) – формальная величина, введённая для количественной оценки содержания ионов, которая показывает, согласно какой концентрации ведут себя ионы в растворе: a = f ∙ Ci, [моль/л] где Ci – концентрация ионов, f < 1 – фактор (коэффициент) активности. Ионная сила раствора – величина, представляющая собой полусумму произведений концентраций всех ионов, присутствующих в растворе, на квадраты их зарядов: Она является мерой интенсивности электрического поля, создаваемого ионами в растворе. Например, ионная сила 0,1 М раствора серной кислоты рассчитывается следующим образом. Уравнение диссоциации: H2SO4 → 2H+ + SO42−. Так как электролит сильный, α = 1, тогда Сраспавш.мол-л = Собщ = См, и [H+] = 2См = 0.2 моль/л, [SO42−] = См = 0,1 моль/л. Определим ионную силу раствора: Правило ионной силы – ионы с одинаковым зарядом в растворах с одинаковой ионной силой имеют равные коэффициенты активности. Это правило вытекает из того, что фактор активности не зависит от природы веществ, а зависит только от концентрации раствора и заряда ионов. 33. Кислотно-основные свойства веществ с точки зрения теории электролитической диссоциации. Другие теории кислот и оснований. Содержание понятий «кислота» и «основание» в процессе развития химической науки существенно менялось, оставаясь одним из основных вопросов химии. В 1778 г. французским ученым Лавуазье была выдвинута «кислородная теория кислот», согласно которой общие свойства кислот обусловлены обязательным наличием в них атомов кислорода. Однако эта теория сразу же встретилась с затруднениями. В начале XIX века немецким ученым Юстусом Либихом была предложена «водородная теория кислот», согласно которой кислотой является водородное соединение, способное замещать атомы водорода на металл. Но данное определение не отражало наиболее существенного свойства кислот, благодаря которому эти вещества были выделены в особый класс соединений, – способности вступать в реакцию нейтрализации с основаниями. В конце XIX века немецким ученым Вильгельмом Оствальдом и шведским ученым Сванте Аррениусом на основании теории электролитической диссоциации были предложены новые определения кислот и оснований. По теории Аррениуса-Оствальда кислотой называется электронейтральное вещество, которое при растворении в воде диссоциирует с образованием ионов Н+, а основанием – электронейтральное вещество, которое диссоциирует с образованием ионов ОН–. Все общие свойства кислот – кислый вкус, действие на металлы, индикаторы и т.д. – являются свойствами ионов Н+. В свою очередь, все общие свойства оснований являются свойствами ионов ОН–. Реакция нейтрализации между кислотой и основанием, таким образом, обусловлена взаимодействием водородных и гидроксильных ионов, приводящих к образованию недиссоциированных молекул воды: Н+ + ОН– = Н2О Однако представления о кислотах и основаниях, согласно теории Аррениуса-Оствальда, также являются не всеобъемлющими и не удовлетворяют во многих случаях наблюдаемым экспериментальным фактам, особенно если они относятся к неводным растворам. Так, например, кислоты и основания могут взаимодействовать между собой и не будучи диссоциированы на ионы. В частности, газообразный хлороводород реагирует с твердой щелочью: HCl + NaOH = NaCl + H2O Тот же хлороводород при растворении в бензоле совершенно не распадается на ионы, однако изменяет окраску индикатора и взаимодействует с металлами, выделяя газообразный Н2. Существует много реакций образования солей, аналогичных реакции нейтрализации, протекающих как в водной, так и безводной среде, но без участия ионов Н+ и ионов ОН–: NH3(газ.) + HCl(газ.) = NH4Cl(тв.) Таким образом, теория кислот и оснований Аррениуса-Оствальда полностью применима лишь к водным растворам веществ. Процессы, протекающие без участия растворителя, а также в неводных жидких средах, требуют существенного дополнения и обобщения данной теории. Такой более общей теорией кислот и оснований явилась протолитическая теория, предложенная в 1923 г. независимо друг от друга датским ученым Бренстедом и английским ученым Лоури. Йоханнес Николаус Бренстед (1879 – 1947) – датский физикохимик. Томас Мартин Лоури (1875 – 1936) – английский химик. Независимо друг от друга практически одновременно сформулировали основные положения протолитической теории кислот и оснований. Согласно этой теории, кислотой называется всякая частица (молекула или ион), способная отдавать протон. Основанием является частица (молекула или ион), способная присоединять протон. Причем отдача иона водорода кислотой всегда происходит в присутствии основания, которое его должно присоединить. При диссоциации кислоты в растворе в роли основания выступают молекулы растворителя:
Образующаяся после отделения иона водорода частица А– называется сопряженным данной кислоте основанием, т.к. она способна снова присоединять к себе ион Н+. Соответственно, частица, полученная после присоединения к основанию иона Н+, называется сопряженной данному основанию кислотой, т.к. способна отдавать его обратно:
Кислота и основание в кислотно-основной паре взаимосвязаны друг с другом. Чем сильнее (слабее) кислота, тем слабее (сильнее) сопряженное с ней основание (табл. 13). Например, в водном растворе хлороводородная кислота HCl сильнее, чем уксусная кислота СН3СООН, поэтому ацетат ион СН3СОО– будет более сильным основанием, чем хлорид ион Cl–. Трактовка понятия «кислота» в протолитической теории Бренстеда-Лоури совпадает с теорией Аррениуса-Оствальда и лишь распространяет ее и на неводные растворы. В случае же трактовки понятия «основание» подход совершенно другой. Например, гидроксид натрия NaOH считается основанием не потому, что он диссоциирует с отщеплением гидроксид-иона ОН–, а потому что этот ион может присоединять к себе ион Н+ с образованием молекулы воды. И именно его следует считать основанием в данном случае. Причем основные свойства ион ОН– проявляет в присутствии кислоты, способной отдать ему Н+. При растворении основания в роли такой кислоты опять же выступают молекулы растворителя:
Согласно протолитической теории, кислоты и основания могут быть трех типов: нейтральные, анионные и катионные. В роли первых выступают нейтральные молекулы, способные отдавать или присоединять ион Н+, например: HCl, H2SO4, HNO3 (кислоты); NH3, CH3–O–CH3 (основания). Анионные основания и кислоты представляют собой отрицательно заряженные ионы, например: HSO4–, HPO42–, HS– (кислоты); OH–, Cl–, NO3– (основания). В роли катионных оснований и кислот выступают положительно заряженные ионы, например: NH4+, H3O+ (кислоты); H2N–NH3+, H2N–(CH2)2–NH3+ (основания). Многие частицы (как молекулы, так и ионы) обладают амфотерными свойствами, т.е. в зависимости от условий могут выступать как в роли кислоты, так и в роли основания, например: H2O, NH3, HSO4–, H2N–NH3+ и т.д. Данные соединения называются амфипротными или амфолитами. В некоторых случаях провести резкую грань между их кислотными и основными свойствами и определить, какие из этих свойств выражены сильнее, бывает затруднительно. Кислотные свойства соединения в растворе определяют по отношению к растворителю как к основанию. Количественно они оцениваются константой равновесия (К) реакции, заключающейся в переносе протона от кислоты к основанию (протолитическая реакция). Покажем это на примере диссоциации муравьиной кислоты в водном растворе:
Константа равновесия данной реакции равна 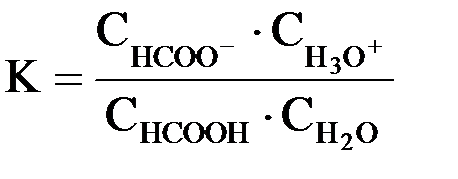 Эта константа отличается от обычного выражения константы диссоциации кислоты (Kдисс.), приводимого ранее, множителем 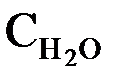 . При рассмотрении диссоциации разных кислот в одном и том же растворителе данный множитель остается одинаковым, поэтому его обычно включают в константу равновесия в виде произведения . При рассмотрении диссоциации разных кислот в одном и том же растворителе данный множитель остается одинаковым, поэтому его обычно включают в константу равновесия в виде произведения 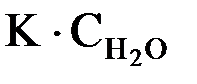 и обозначают Ka (константа кислотности): и обозначают Ka (константа кислотности):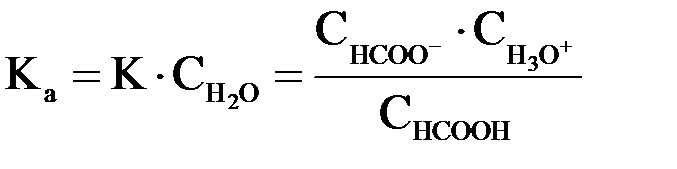 Чем больше величина Ka, тем сильнее кислота, т.е. тем она легче отдает ионы Н+ основанию (молекулам растворителя). Для оценки силы слабых кислот чаще используют не величину Ka, а ее десятичный логарифм, взятый с обратным знаком: –lg Ka = pKa Чем больше значение рKa, тем слабее кислота. |
