Патфиз ч.2. Патфиз ч. Гл. 11 Нарушения водного обмена Гл. 12 Нарушения ионного обмена
 Скачать 7.84 Mb. Скачать 7.84 Mb.
|
|
§ Повышение притока крови к сердцу. § Увеличение кровенаполнения, ударного выброса и, как следствие — перфузионного давления. ‡ Позднее (в связи с изменениями обмена веществ в органах и тканях) накапливаются БАВ, снижающие тонус стенок сосудов (как резистивных, так и ёмкостных). К этим веществам относятся аденозин, биогенные амины, гистамин, NO, Пг E, I2 ‡ Под действием экстремального фактора (особенно вызывающего плазмо или кровопотерю) происходит перераспределение кровотока. Проявления § Увеличение кровотока (или, по меньшей мере, отсутствие снижения) в артериях сердца и мозга. § Одновременное уменьшение кровотока в сосудах кожи, мышц, органов брюшной полости, почек (вследствие вазоконстрикции). Этот феномен получил название централизации кровотока. Причины § Неравномерное содержание адренорецепторов в разных сосудистых регионах. Наибольшее их число выявлено в стенках сосудов мышц, кожи, органов брюшной полости, почек и значительно меньшее — в сосудах сердца и головного мозга. § Образование в ткани миокарда и мозга большого количества сосудорасширяющих веществ — аденозина, простациклина, NO и др. Значение § Адаптивное. Кровоснабжение сердца и мозга в условиях феномена централизации кровотока способствует поддержанию жизнедеятельности организма в целом. Напротив, ишемия этих органов значительно усугубляет течение шока. § Патогенное. Гипоперфузия сосудов кожи, мышц, органов брюшной полости и почек ведёт к развитию в них ишемии, замедлению тока в микроциркуляторном русле (особенно в посткапиллярах и венулах), нарушению реабсорбции жидкости в венулах. Последнее обусловливает уменьшение ОЦК и сгущению крови. † Уменьшение ОЦК, изменение вязкости крови и активности факторов системы гемостаза выявляются уже на раннем этапе шоковых состояний. Проявления † Повышение вязкости крови. † Снижение её текучести. † Образование тромбов в сосудах микроциркуляции. † Повышение содержания и/или активности факторов свёртывающей системы крови. Последнее обусловлено, главным образом, повреждающим действием шокогенного агента, гиперкатехоламинемией, выходом из повреждённых клеток Ca2+ и другими факторами. В совокупности расстройства сердечной деятельности, тонуса сосудистых стенок, повышение проницаемости их и нарушения реабсорбции жидкости в сосудистое русло инициируют нарастающее нарушение центрального и регионарного кровообращения, а также микрогемоциркуляции при всех разновидностях шока. • Гипоксическое звено Гипоксическое звено патогенеза является одним из главных и закономерных компонентов патогенеза шока. Причины † Первоначально гипоксия обычно является следствием расстройств гемодинамики и носит циркуляторный характер. † По мере усугубления состояния гипоксия становится смешанной. Это является результатом прогрессирующих расстройств дыхания, изменений в системе крови и тканевого метаболизма. Последствия † Снижение эффективности биологического окисления потенцирует нарушение функций тканей и органов, а также — обмена веществ в них. † Гипоксия является одной из причин подавления активности факторов системы антиоксидантной защиты тканей. В связи с этим в них генерируется избыток реактивных форм кислорода, активируются реакции липопероксидации и накапливаются продукты этих реакций — перекиси, гидроперекиси, альдегиды и другие. • Токсемическое звено Токсемическое звено включается уже на ранней стадии шока. Причины † Действие экстремального фактора (при токсическом, токсикоинфекционном, ожоговом, анафилактическом и других видах шока). † Повреждение экстремальным фактором клеток и высвобождение из них большого количества невостребованных БАВ (кининов, биогенных аминов, аденин и аденозиннуклеотидов, ферментов), продуктов нормального и нарушенного метаболизма, ионов, денатурированных соединений. † Нарушение инактивации и/или экскреции токсичных соединений печенью, почками, другими органами и тканями. Последствия Нарастание интоксикации потенцирует гипоксию, нарушения гемодинамики, функций органов и тканей. • Метаболическое звено Причины † Чрезмерная активация нервных и гуморальных влияний на ткани и органы. † Расстройство гемодинамики в тканях и органах. † Гипоксия. † Токсемия. Последствия В целом изменения метаболизма характеризуются преобладанием процессов катаболизма: † Содержание белка в тканях, как правило, снижается. Одновременно в них увеличивается уровень продуктов его распада. Причина: значительная активация протеолитических ферментов под влиянием избытка катехоламинов, Ca2+, H+ и других ферментов. † Общее содержание белка в крови также уменьшается. Одна из ведущих причин: выход низкомолекулярных белковых фракций из сосудов в связи со значительным повышением проницаемости их стенок. † Уровень гликогена в тканях снижается. Причины: ‡ гликогенмобилизирующее действие избытка катехоламинов, глюкокортикоидов и других гормонов; ‡ торможение синтеза гликогена в клетках в связи с инсулиновой недостаточностью, ‡ следствием указанных процессов является гипергликемия. † Содержание остаточного (небелкового) азота в крови обычно повышается. Причины: ‡ активация процесса глюконеогенеза, ‡ нарушение функций печени, ‡ снижение экскреции мочевины почками. † Липидный обмен характеризуется: ‡ интенсификацией липолиза в тканях, ‡ увеличением содержания в них свободных жирных кислот, которые интенсивно окисляются, эстерифицируются, а также подвергаются липопероксидации; ‡ снижением уровня фосфолипидов в тканях, что свидетельствует об активации фосфолипаз; ‡ уменьшением содержания свободных жирных кислот в крови, поскольку они интенсивно включаются в тканевой метаболизм (при условии достаточного для этого уровня АТФ в клетках) и трансформируются в реакциях свободнорадикального окисления. † Содержание адениннуклеотидов (АТФ, АДФ, АМФ) и неорганического фосфата в тканях меняется по-разному. ‡ Уровень АТФ в них снижается в результате интенсивного гидролиза АТФ. ‡ Концентрация фосфатов падает в связи с их выходом в кровь. ‡ Содержание АДФ и АМФ в тканях возрастает, так как гидролиз АТФ повышен, а его ресинтез недостаточен в условиях дефицита кислорода. † Уровень ионов и жидкости в целом в тканях возрастает. Причины: повреждение цитолеммы, а также мембран митохондрий и саркоплазматической сети. Проявления: увеличение в тканях [K+], [Ca2+], [Na+], осмотического и онкотического давления и объёма жидкости. Усугубление описанного выше комплекса расстройств функций органов и тканей, обмена веществ и пластических процессов в них, а также нарастающее истощение адаптивных реакций создаёт условия для перехода стадии адаптации (компенсации) в стадию декомпенсации шока. СТАДИЯ ДЕКОМПЕНСАЦИИ Стадия декомпенсации (деадаптации, прогрессирующая, необратимая, торпидная) — результат действия как самого экстремального фактора, так и прогрессирующей недостаточности функций тканей, органов, их систем, а также истощения адаптивных возможностей организма. Основные звенья патогенеза шока на стадии декомпенсации приведены на рис. 20–8, а проявления шока на этой же стадии в табл. 20–4. 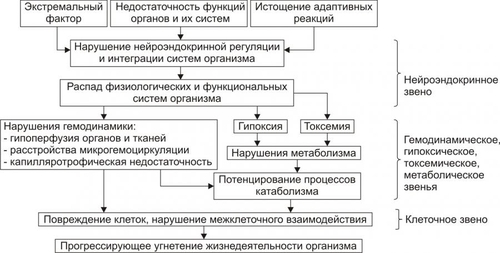 Рис. 20–8. Основные звенья патогенеза шока (стадия декомпенсации). В отличие от стадии компенсации, степень и масштаб расстройств значительно более выражены. Разнообразные патологические изменения развиваются одновременно и потенцируют друг друга. Наиболее часто наблюдается декомпенсация функций почек, лёгких, печени (синдромы «шоковых почек», «шоковых лёгких» и др). В этих условиях недостаточность функции органов достигает крайней степени. Это может стать причиной смерти пациента. • Нейроэндокринное звено † Сознание на стадии декомпенсации не утрачивается. Вместе с тем при тяжёлом течении шока отмечаются признаки заторможенности и спутанности сознания. Это проявляется тем, что пациент с задержкой и часто невпопад отвечает на вопросы, с трудом ориентируется в окружающей обстановке. † Интенсивность нервных влияний и уровень гормонов: ‡ либо снижаются, либо сохраняются на повышенном уровне; ‡ эффекты нервных и гормональных влияний прогрессирующе уменьшаются вплоть до отсутствия. Причины ‡ Существенное повреждение нервной и других тканей. ‡ Значительные физикохимические сдвиги в тканях (ацидоз, ионный дисбаланс, гипергидратация и др.). ‡ Снижение чувствительности (гипосенситизация) клеток к гормонам и нейромедиаторам. ‡ Падение выраженности условных и безусловных рефлексов (гипорефлексия). ‡ Уменьшение содержания в крови гормонов большинства желёз внутренней секреции. Совокупность указанных изменений приводит к дисбалансу как содержания нейромедиаторов и гормонов в плазме крови и межклеточной жидкости, так и их эффектов. Это является причиной распада функциональных и физических систем организма, что обусловливает дискоординацию и тенденцию к минимизации функций органов и тканей. • Гемодинамическое звено На стадии декомпенсации гемодинамическое звено патогенеза шока приобретает ключевое значение. Причины † Прогрессирующее нарушение функции сердца, развитие недостаточности его сократительной деятельности, а также аритмии. † Тотальное снижение тонуса резистивных и ёмкостных сосудов. Это устраняет адаптивный феномен централизации кровообращения. Систолическое АД при тяжёлом течении шока снижается до 60–40 мм рт.ст., что чревато прекращением процесса фильтрации в клубочках почек и развитием уремии. † Дальнейшее снижение ОЦК и повышение её вязкости в связи с выходом жидкой части крови в межклеточное пространство. Проявления † Тотальная гипоперфузия органов и тканей. † Существенное расстройство микроциркуляции. † Капилляро-трофическая недостаточность. Изменения в сосудах микроциркуляторного русла: † замедление скорости кровотока. † появления в одних регионах сосудистого русла большого количества так называемых плазматических капилляров (в которых отсутствуют форменные элементы крови), а в других — капилляров, заполненных агрегатами клеток крови или с признаками феномена сладжа и стаза. Изменения в системе гемостаза заключаются в развитии дисбаланса концентрации и/или активности факторов свёртывающей, противосвёртывающей и фибринолитической систем. Последствия Развитие на стадии декомпенсации шока: † ДВСсиндрома, † ишемии тканей, † дистрофических изменений в органах и тканях, † некроза тканей, † геморрагий в них. • Гипоксическое звено Причины † Системные расстройства гемодинамики. † Гиповентиляция лёгких. † Уменьшение ОЦК. † Нарушение функции почек. † Расстройства обмена веществ. Последствия † Развитие выраженной гипоксии смешанного типа. † Некомпенсированный ацидоз. В таких условиях усугубляются расстройства обмена веществ, накапливаются продукты нарушенного метаболизма и ещё более подавляются функции органов и тканей. • Токсемическое звено Токсемия характеризуется: † увеличением содержания в крови и других биологических жидкостях продуктов нарушенного метаболизма и физиологически активных веществ (например, молочной и пировиноградной кислот, жирных кислот, полипептидов, биогенных аминов); † накоплением в крови соединений: ‡ высвобождающихся из повреждённых и разрушенных клеток (ферментов, денатурированных белков, ионов, различных включений и др.); ‡ образующихся в организме в связи с недостаточностью функций печени и почек индолов, фенолов, скатолов, мочевины, мочевой кислоты и ряда др. Указанные вещества значительно усугубляют повреждение органов. • Метаболическое звено Метаболическое звено шока на стадии декомпенсации проявляется: † доминированием процессов катаболизма белков, липидов, углеводов, сложных их соединений (ЛП, гликопротеинов, фосфолипидов и др.); † минимизацией интенсивности обмена веществ и пластических процессов в клетках, † гипергидратацией клеток. † накоплением в биологических жидкостях недоокисленных веществ (молочной, пировиноградной кислот, КТ и др.); † увеличением в тканях уровня продуктов липопероксидации, • Клеточное звено Клеточное звено патогенеза шока на стадии декомпенсации характеризуется: † нарастающим подавлением активности ферментов и жизнедеятельности клеток, † повреждением и разрушением клеточных мембран, † нарушениями межклеточных взаимодействий. В целом, недостаточность функций органов и тканей, гипоксия, токсемия грубые расстройства обмена веществ обусловливают значительные отклонения от нормы жизненно важных параметров гомеостаза, проявляющихся: • артериальной гипотензией и коллапсом, • значительным снижением показателей рО2 и рН, • увеличением осмолярности плазмы крови, • нарастающим угнетением жизнедеятельности организма в целом. Таблица 20–4. Основные звенья патогенеза шока (стадия декомпенсации)
ОСОБЕННОСТИ ПАТОГЕНЕЗА НЕКОТОРЫХ ВИДОВ ШОКА Особенности различных видов шока определяются главным образом их причиной и характером реагирования на неё организма. С учётом этих двух факторов ниже приводится характеристика отдельных и клинически значимых вариантов шока. АНАФИЛАКТИЧЕСКИЙ ШОК См. статью «Шок анафилактический» в приложении «Справочник терминов» на компакт диске. ИНФЕКЦИОННО-ТОКСИЧЕСКИЙ ШОК См. статью «Шок инфекционно-токсический» в приложении «Справочник терминов» на компакт диске. КАРДИОГЕННЫЙ ШОК См. статью «Шок кардиогенный» в приложении «Справочник терминов» на компакт диске. ОЖОГОВЫЙ ШОК Причина ожогового шока: обширные ожоги кожи (как правило, более 25% от её общей поверхности) второй и/или третьей степени. У детей и людей пожилого возраста развитие шока наблюдается при ожоге уже около 10% поверхности кожи. Патогенез и проявления Основные звенья механизма развития ожогового и травматического шока сходны. Вместе с тем ожоговый шок имеет ряд особенностей (рис. 20–9). 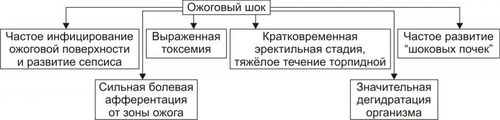 Рис. 20–9. Некоторые особенности ожогового шока. • Значительная болевая афферентация от обожжённой кожи и мягких тканей, являющаяся причиной генерализованной активации нервной и эндокринной систем. Это ведёт к развитию сильнейшего эмоционального, двигательного и речевого возбуждения, активации функций органов и тканей, а также обмена веществ в них. • Сравнительно кратковременная стадия компенсации. Часто она переходит в стадию декомпенсации ещё до оказания первой врачебной помощи. Краткосрочность первой стадии обусловлена перенапряжением и быстрым истощением адаптивных реакций организма, а также значительными расстройствами гемодинамики и интоксикацией. • Выраженная дегидратация организма в результате массивной потери плазмы крови. Последнее определяется значительным повышением проницаемости стенок сосудов, особенно в области ожога. • Повышенная вязкость крови, развитие феномена сладжа, тромбообразование и расстройства микрогемоциркуляции, развивающиеся в результате большой потери плазмы крови. • Выраженная интоксикация организма: † продуктами термической денатурации белка и протеолиза, † избытком БАВ, образующихся при повреждении тканей (кининов, биогенных аминов, олиго и полипептидов и др.), † токсинами микробов. • Частое поражение почек, обусловленное нарушением их кровоснабжения и гемолизом эритроцитов. • Аллергические реакции и болезни иммунной аутоагрессии. Наблюдается у пациентов, выведенных из шокового состояния и при развитии у них ожоговой болезни. Это является следствием денатурации белков крови и тканей, а также инфицирования организма. Иммунопатологические реакции значительно усугубляют тяжесть течения как ожогового шока, так и ожоговой болезни. |
