|
|
Орг. Химия. Орг. химия. Лаборат. практ. 2018. Мифи (дити нияу мифи) Органическая химия Лабораторный практикум для студентов специальности 18. 05. 02 Составитель С. В. Павутницкая Димитровград 2018 г
3.20.1 Моно- и дисахариды
Методика проведения опытов
Опыт 1. Качественная реакция на углеводы (реакция Молиша)
Опыт проводят одновременно с несколькими различными углеводами.
Помещают в пробирку 0,5—1 мл воды и вносят в нее очень немного исследуемого углевода (несколько крупинок сахара или крахмала). Затем добавляют 2 капли 10%-ного раствора α-нафтола в спирте.
После этого, наклонив пробирку, осторожно приливают по стенке (лучше из пипетки) 1 - 1,5 мл концентрированной серной кислоты. Тяжелый слой кислоты должен опуститься на дно пробирки, почти не смешиваясь с водным слоем. На границе слоев быстро образуется красно-фиолетовое кольцо; при взбалтывании смесь разогревается и окрашивается по всему объему, а при разбавлении ее водой выделяются окрашенные хлопья.
В отсутствие углеводов фиолетового кольца не образуется, хотя жидкость может позеленеть или пожелтеть.
Цветную реакцию с α-нафтолом (Молиш, 1886 г.) дают углеводы, причем кетозы, свободные или связанные в дисахаридах и полисахаридах, реагируют более интенсивно. Появление окраски обусловлено расщеплением молекулы углевода при действии концентрированной серной кислоты с образованием в числе прочих продуктов фурфурола или его производных, которые вступают в реакцию конденсации с α-нафтолом, образуя окрашенные соединения.
Окрашенный продукт, образующийся в описанных условиях из гексозы и α-нафтола, имеет следующее строение:
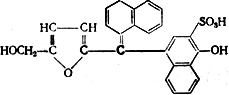
Описанная цветная реакция на углеводы очень чувствительна.
Опыт 2. Доказательство наличия в сахарах гидроксильных групп.
В пробирку помещают 5 капель 0,5%-ного раствора глюкозы и 1мл 2н NaOH. К полученной смеси добавляют 5 капель 0,2н раствора сульфата меди. Образующийся вначале осадок гидроксида меди должен немедленно раствориться и должен образоваться прозрачный раствор сахарата меди со слабой синей окраской.
В другую пробирку помещают 5 капель 1%-ного раствора сахарозы и 1мл 2н NaOH. Добавляют для разбавления 1мл воды и 5 капель 0,2 н. раствора сульфата меди. Сравнивают полученный результат с опытом в первой пробирке.
Обе пробирки с полученными растворами используют в опыте 3.
Опыт 3. Отношение сахаров к окислителям
К раствору в первой пробирке из опыта 2 добавляют воду так, чтобы высота слоя жидкости была около 4 см. нагревают пробирку над пламенем спиртовки, держа пробирку наклонно так, чтобы нагревалась только верхняя часть раствора. Нагрев прекращают с началом кипения.
С содержимым второй пробирки проводят аналогичную операцию и сравнивают полученные результаты.
В случае проявления восстановительных свойств должен выпасть желтый осадок СuОН, при более продолжительном нагревании теряющий воду с образованием оксида меди (I) красного цвета.
Опыт 4. Восстановление аммиачного раствора оксида серебра глюкозой (реакция «серебряного зеркала»)
Для получения зеркального налета необходима чистая поверхность стекла. В пробирку наливают 2 мл 2н раствора NaOH, нагревают пробирку и ополаскивают горячим раствором. Щелочь сливают в склянку с отходами щелочей и дважды ополаскивают пробирку водой.
В вымытую пробирку вносят 1 мл раствора глюкозы и 1 мл аммиачного раствора оксида серебра. Слегка подогревают пробирку, держа её над пламенем спиртовки только до начала побурения раствора. Далее реакция идет без нагревания, и металлическое серебро выделяется либо в виде черного осадка, либо, если стенки пробирки были чисты, в виде блестящего зеркального налета.
Пробирку после опыта не следует мыть, следует оставить ее в штативе.
Опыт 5. Гидролиз сахарозы
Помещают в пробирку 5 капель 1%-ного раствора сахарозы, добавляют 5 капель 2н НСl и 1 мл воды. Нагревают над пламенем спиртовки до кипения и кипятят в течение 1-2 мин. Пробирку следует держать как можно более наклонно и все время встряхивать, чтобы раствор не выбросило.
Разливают полученный раствор в две пробирки и определяют продукты гидролиза сахарозы.
А. В одну пробирку добавляют для нейтрализации кислоты 1мл 2н NaOH и 1 мл воды. Затем добавляют 5 капель 0,2н CuSO4 и нагревают верхнюю часть синего раствора до кипения.
Б. Во вторую пробирку вносят несколько крупинок резорцина и 10 капель концентрированной соляной кислоты. Нагревают до кипения. При этом должно появиться отчетливое красное окрашивание. Такая реакция характерна для кетогексоз.
Опыт 6. Образование сахара при окислении многоатомного спирта
Растворяют 3 - 4 капли глицерина в 3 мл воды и разливают раствор в две пробирки.
В первую пробирку добавляют разбавленный раствор щелочи и затем по 2 - 3 капли раствора сульфата меди. Образующийся голубой сгусток гидроокиси меди при взбалтывании растворяется, образуя раствор фиолетового или синего цвета. Нагревают раствор до кипения и отмечают, заметны ли в нем изменения.
Во вторую пробирку добавляют 8 - 10 мл свежеприготовленной насыщенной бромной воды и нагревают на кипящей водяной бане до обесцвечивания раствора. Если через 10 - 15 мин окраска раствора не исчезла, то кипятят его 1 - 2 мин. на пламени горелки. Охладив бесцветную жидкость, отливают 2 - 3 мл ее в пробирку и повторяют описанную выше реакцию со щелочью и сульфатом меди с последующим нагреванием до кипения.
Бромная вода является сильным окислителем и энергично превращает многоатомный спирт преимущественно в альдегидоспирт — альдозу:
Вr2 + Н2О → НВr + НОВr
СН2ОН(СНОН)nСН2ОН + НОВг → СН2ОН(СНОН)nС=O + НВr + Н2O
\Н
Одновременно образуется и кетоноспирт — кетоза; при большом избытке бромной воды альдоза частично окисляется далее до оксикислоты.
Глицерин при окислении бромной водой дает смесь триоз — глицерозу (глицериновый альдегид СН2(ОН)СН(ОН)СНО и диоксиацетон СН2(ОН)СОСН2ОН).
Техника безопасности
При нагревании жидкостей отверстие пробирки необходимо направлять в сторону от себя и окружающих во избежание выброса веществ из пробирки.
Работы с бромом проводить в вытяжном шкафу.
3.20.2 Полисахариды
Наиболее важными полисахаридами являются природные полисахариды -крахмал и целлюлоза (клетчатка).
В состав крахмала входят остатки α,D-глюкозы, в состав целлюлозы - β,D-глюкозы. Общим их свойством, используемым на практике, является способность полисахаридов гидролизоваться с образованием в качестве конечных продуктов глюкозы.
Обычный растительный крахмал содержит два полисахарида — амилозу и амилопектин, молекулы которых построены из остатков дисахарида мальтозы. Амилопектин имеет молекулярную массу свыше 1 000 000, а амилоза — не выше 200 000. В холодной воде крахмал практически нерастворим, в горячей же воде образует коллоидный раствор — клейстер.
При действии йода амилоза окрашивается в чисто-синий цвет, а амилопектин - в сине-фиолетовый. Причиной появления окраски следует считать образование молекулярных соединений йода с амилозой и амилопектином. Образовавшееся соединение включения («клатрат») имеет общий состав С6Н10О5 ·I2. Реакция с иодом позволяет обнаружить уже 0,01 - 0,05 мг крахмала в 1 мл раствора. Бром дает с крахмалом лишь слабо-желтое окрашивание.
При нагревании до 200 - 2500С большие молекулы крахмала (амилоза и амилопектин) распадаются на молекулы меньшего размера, образуя смесь декстринов. Эти продукты распада крахмала в отличие от самого крахмала довольно хорошо растворимы в воде, содержат значительно большее число свободных глюкозидных гидроксилов и обнаруживают восстановительные свойства.
Гидролиз крахмала значительно ускоряется в присутствии кислот. В результате последовательно углубляющегося гидролиза крахмала сначала образуются декстрины, затем дисахарид мальтоза С12Н22О11 и, как конечный продукт гидролиза, моносахарид D-глюкоза.
Целлюлоза относится к природным полисахаридам. Ее молекула представляет собой цепь, состоящую из остатков β-D-глюкозы. Целлюлоза нерастворима в органических растворителях, воде, водных растворах щелочей и разбавленных кислотах. Растворима в реактиве Швейцера (медно-аммиачный растворе), водном растворе хлорида цинка и с гидролизом в концентрированных минеральных кислотах (H2SO4, HCl, H3PO4).
В концентрированных растворах щелочи (выше 10%) целлюлоза набухает с образованием щелочной целлюлозы. Считается, что при этом имеет место как образование молекулярного соединения целлюлозы со щелочью - [С6Н7О2(ОН)3.NаОН]n, так и образование алкоголята целлюлозы [С6Н7О2(ОН)2ОNа]n.
При этом целлюлоза сильно набухает, ее волокна утолщаются и укорачиваются. После промывки щелочной целлюлозы водой получают гидратцеллюлозу, отличающуюся от природной целлюлозы более рыхлой структурой и физико-химическими свойствами. Гидратцеллюлоза более гигроскопична, обладает повышенной набухаемостью, более подвержена гидролизу и интенсивнее окрашивается. Такая обработка называется мерсеризацией.
Глюкозидные связи молекул целлюлозы очень неустойчивы к минеральным кислотам и легко гидролизуются. Полный гидролиз заканчивается образованием β-D-глюкопиранозы. Промежуточным продуктом гидролиза присвоено название гидроцеллюлозы. Из подобных смесей выделены целлодекстрины со степенью полимеризации от 7 до 60 и олигосахариды, имеющие степень полимеризации от 2 до 6.
Параллельно идет постепенный гидролиз целлюлозы, вследствие чего и происходит растворение целлюлозы. Кислота концентрации
70% при кратковременном действии на холоду растворяет лишь поверхность волокон целлюлозы, которые склеиваются продуктами частичного гидролиза, так называемым амилоидом в прочную массу. Обработанную таким образом бумагу называют растительным пергаментом.
Методика проведения опытов
Опыт 1. Реакции крахмала.
Около 1 г сухого крахмала взбалтывают с 5 - 6 мл воды, дают смеси отстояться 1 - 2 мин, сливают воду и повторяют промывание крахмала еще 2 - 3 раза новыми порциями воды. Добавив последнюю порцию воды и хорошо взболтав смесь, выливают суспензию крахмала в 50 мл воды, нагретой до кипения в стакане или колбе. Образуется почти прозрачный, слегка опалесцирующий крахмальный клейстер.
Охлаждают раствор и проводят с ним следующие реакции.
А. К 1—2 мл раствора крахмала добавляют каплю раствора йода. Полученную темно-синюю жидкость нагревают. Окраска исчезает, но при охлаждении снова появляется.
Б. Другую пробу раствора крахмала (1—2 мл) смешивают с 1 мл спирта и добавляют йод. Появляется лишь слабое буроватое окрашивание.
В. К 1—2 мл крахмального клейстера добавляют несколько капель разбавленного раствора щелочи и нагревают смесь до кипения; жидкость не обнаруживает изменений или лишь слегка желтеет.
Г. К 1—2 мл клейстера добавляют несколько капель щелочи и 1—2 капли раствора сульфата меди и нагревают смесь на кипящей водяной бане 2—2 мин. Раствор остается почти бесцветным; голубые хлопья нерастворившейся гидроокиси меди при нагревании чернеют, красного или желтого осадка не образу-ется.
Опыт 2. Гидролиз крахмала
А. Гидролиз крахмала при нагревании. Около 1 г сухого крахмала очень осторожно, при постоянном встряхивании нагревают в сухой пробирке на пламени горелки до начала пожелтения порошка. Дают пробирке остыть. К образовавшемуся декстрину добавляют 10 - 12 мл холодной воды, смесь сильно встряхивают 1 - 2 мин и фильтруют через бумажный фильтр.
Прозрачный фильтрат делят на 4 части и проводят с ним реакции, как в предыдущем опыте: с йодом, со спиртом, со щелочью при нагревании и с солью двухвалентной меди в щелочном растворе при нагревании. Во всех случаях наблюдается различие между отношением крахмала и декстрина к этим реактивам.
Б. Гидролиз крахмала кислотами. В стаканчик или в колбочку помещают 15 - 20 мл крахмального клейстера, добавляют 1 мл разбавленной серной кислоты. Смесь кипятят 5 - 10 мин, при этом через каждые 1 - 2 мин отливают в отдельную пробирку немного (1 - 2 мл) горячей жидкости, быстро охлаждают пробу в воде, добавляют каплю раствора йода и ставят пробирку в штатив. В последовательно отобранных пробах наблюдается постепенное изменение окраски при реакции с йодом.
После того как окраска пробы при действии йода совершенно перестанет появляться, кипятят смесь еще 5 - 6 мин, затем охлаждают ее и понемногу при сильном взбалтывании добавляют 2 г карбоната кальция. После прекращения вспенивания горячую смесь фильтруют через складчатый фильтр, собирая 10 - 20 мл прозрачного фильтрата. Полученный раствор испытывают реактивами на моносахариды (опыт 1Г) и сравнивают наблюдаемые изменения с результатами опыта 1 с исходным крахмалом.
Выпаривая 10 - 15 мл этого фильтрата в фарфоровой чашечке, получают несколько капель густого, желтоватого, сладкого на вкус сиропа — патоки.
Опыт 3. Кислотный гидролиз целлюлозы
В пробирку помещают маленький кусочек фильтровальной бумаги (1x1 см), добавляют 6 капель концентрированной серной кислоты и размешивают стеклянной палочкой до полного растворения целлюлозы. Для ускорения растворения пробирку можно слегка подогреть на водяной бане (осторожно). Затем добавляют 20 капель воды и нагревают пробирку на водяной бане в течение 10 мин.
После этих операций проводят пробу на присутствие глюкозы. Для этого вносят в пробирку 20 капель 2н NaOH (для нейтрализации кислоты и создания щелочной среды). Добавляют 2 капли 0,2н CuSO4.
Опыт 4. Получение эфиров целлюлозы
А. Получение азотнокислых эфиров (нитратов) целлюлозы. В широкую пробирку наливают 2 мл концентрированной азотной кислоты (плотностью 1,52) и осторожно при взбалтывании добавляют 4 мл концентрированной серной кислоты (плотностью 1,94). Слегка охладив разогревшуюся смесь, погружают в нее при помощи стеклянной палочки небольшой комок ваты. Осторожно помешивая палочкой, содержимое пробирки нагревают в водяной бане при 60-700.
Через 5 мин вынимают вату палочкой и хорошо промывают в сосуде с водой (сменяя воду несколько раз) или под водопроводным краном. При промывке расщипывают вату пальцами. Промытую вату хорошо отжимают в фильтровальной бумаге и сушат в сушильном шкафу.
Высушенный образец с помощью пинцета вносят в пламя спиртовки. Если реакция прошла достаточно полно, полученный нитрат сгорает мгновенно.
Б. Получение триацетата целлюлозы. Смешивают в пробирке 3 мл уксусного ангидрида, 3 мл ледяной (концентрированной) уксусной кислоты и 1 каплю концентрированной серной кислоты.
0,2 г ваты или фильтровальной бумаги замачивают в течение 3-5 мин в воде, хорошо отжимают фильтровальной бумагой, расщипывают и стеклянной палочкой проталкивают на дно пробирки. Пробирку помещают в водяную баню с температурой 50 - 600С и перемешивают ее содержимое до полного растворения целлюлозы. Однородную жидкость выливают тонкой струей в стакан с 150 - 200 мл холодной воды. Триацетат целлюлозы должен выпасть в виде хлопьев. При необходимости хлопья можно отфильтровать с отсасыванием через кружок фильтровальной бумаги или материи, отжать и высушить в сушильном шкафу.
Для доказательства получения триацетата проверяют растворимость продукта при легком нагревании в ацетоне или хлороформе.
Опыт 5. Взаимодействие целлюлозы со щелочью
Две пробирки заполняют наполовину одну водой, другую – 30%-ным раствором NaOH. Из фильтровальной бумаги вырезают две одинаковые полоски длиной 15 см и шириной 1,5-2 см. Полоски складывают вдвое вдоль так, чтобы каждая могла свободно войти в пробирку. Опускают полоски в подготовленные пробирки на 5 - 7 мин. Вынув полоску из воды, отжимают ее в фильтровальной бумаге и оставляют сохнуть.
Затем вынимают полоску из раствора щелочи, стряхивают капли, опускают полоску последовательно в воду, пробирку с разбавленной соляной кислотой, снова в воду и отжимают. После сушки в сушильном шкафу сравнивают длину полосок, плотность и характер поверхности.
Опыт 6. Превращение целлюлозы в амилоид
В пробирку наливают 4 мл 70%-ной серной кислоты и погружают в неё узкую полоску фильтровальной бумаги. Через 10-15 секунд бумагу вынимают и тщательно отмывают от кислоты в проточной воде под краном, а затем в воде, к которой добавлено несколько капель раствора аммиака.
Отмечают различие плотности и прочности мокрой бумаги в обработанной и необработанной кислотой частях полоски. После сушки бумаги различие свойств этих участков полоски должно становиться еще более резким.
На границу двух участков бумаги помещают каплю раствора йода и наблюдают различие их окраски. Йод образует с молекулами полисахаридов комплекс с синей окраской. Интенсивность окраски изменяется в зависимости от молекулярной массы полимера.
Техника безопасности
В работе используются растворы щелочи, уксусный ангидрид и концентрированные кислоты, способные вызвать химические ожоги.
Соблюдать правила работы с кислотами и щелочами.
С уксусным ангидридом и концентрированными кислотами работать только в вытяжном шкафу.
4 Рекомендуемая литература
Практикум по органической химии. Под ред. О.Ф. Гинзбурга, А.А. Петрова.- М.: Высш. шк., 1989. 318 с.
Некрасов В.В. Руководство к малому практикуму по органической химии./ В.В.Некрасов. – М.: Химия, 1975. – 328 с.
Рево А.Я. Малый практикум по органической химии / А.Я.Рево, В.В.Зеленкова. – М.: Высшая школа, 1980. – 175 с.
Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. Изд. 5-е. СПб: Иван Федоров, 2002. 624 с.
Березин Б.Д., Березин Д.Б. Курс современной органической химии. Изд. 2-е. М.: Высшая школа, 2003. 768 с.
Швехгеймер М.-Г.А., Кобраков К.И. Органическая химия. – М.: Высш.шк., 1994. – 543 с.
Справочник химика. Под редакцией Никольского Б.П. - Л.: Химия, 1968. Том 1 – 7.
Гороновский И.Т., Назаренко Ю.П., Некряч Е.Ф. Краткий справочник по химии. 5-е изд., испр. и доп. - К.: Наукова думка, 1987. - 833 с.
Учебное издание
ОРГАНИЧЕСКАЯ ХИМИЯ
Лабораторный практикум
для студентов специальности 18.05.02 дневной формы обучения.
ПАВУТНИЦКАЯ Светлана Владимировна
В авторской редакции
Изготовление оригинал макета Волковой Л.Н.
Подписано в печать 20.01. 2018.
Формат 60х90/16. Бумага писчая. Усл. печ. л. 5,0. Уч.-изд. л. 5,8
Тираж 15 экз. Заказ № 1.
ДИТИ НИЯУ МИФИ
Редакционно – издательский отдел
433511. Димитровград, ул. Куйбышева, 294
|
|
|
 Скачать 1.26 Mb.
Скачать 1.26 Mb.
