РУКОВОДСТВО ПО ОБЩЕЙ ХИРУРГИИ. Руководство по общей хирургии Учебное пособие. М. Оао Издательство Медицина
 Скачать 9.28 Mb. Скачать 9.28 Mb.
|
|
Электрокардиография. Наиболее характерными ЭКГ-признаками острого инфаркта миокарда являются элевация (3 мм и более) или депрессия сегмента STс остроконечными положительными зубцами Т, их инверсия, патологический широкий (более 0,03 с) зубец Q. Двухмерная эхокардиография (эхоКГ) позволяет выявить нарушения локальной сократимости желудочков, оценить их систолическую функцию, состояние клапанов. При допплеровском исследовании определяют особенности нарушенной внутрисердечной гемодинамики. При эхоКГ-исследовании выявляются зоны гипокинезии миокарда правого желудочка, снижение общей сократимости и дилатация его полости, трикуспидальная недостаточность, нормальная или сниженная систолическая функция левого желудочка. При сцинтиграфии миокарда с технецием-99т-пирофосфатом наблюдается накопление изотопа в соответствующих сегментах. 348 При инвазивном мониторинге давления отмечается повышенное диастоли-ческое давление в правом предсердии и правом желудочке и нормальное в легочной артерии. Варианты клинического течения острого инфаркта миокарда:
Лечение. Основные принципы лечения инфаркта миокарда:
А Как правило, при лечении болевого синдрома первоначально используют нитроглицерин сублингвально или внутривенно капельно (с начальной скоростью 10—20 мкг/мин и последующим ее постепенным увеличением через каждые 5 мин под контролем АД). При неинтенсивной боли или при непереносимости нитроглицерина можно использовать нитросорбит (при разжевывании антиангинальный эффект наблюдается через 3—5 мин). Назначают также для приема внутрь нитраты пролонгированного действия. Начало действия препаратов депо-нитроглицерина (сустак, нитронг, нитро-мак) может проявляться через 15—30 мин. Для достижения быстрого эффекта внутривенно вводят обзидан (5 мг за 5 мин), а затем переходят на пе-роральный прием препаратов. Если на фоне лечения нитроглицерином не удается купировать боль или достигнут неполный эффект, применяют наркотические анальгетики. А Фентанил обладает мощным обезболивающим (в 100 раз превосходит эффект морфина) и кратковременным действием. При внутривенном введении аналгезия наступает через 1—3 мин и продолжается при однократном введении не более 30 мин. Вводят внутривенно в дозе 1—2 мл 0,005 % 349 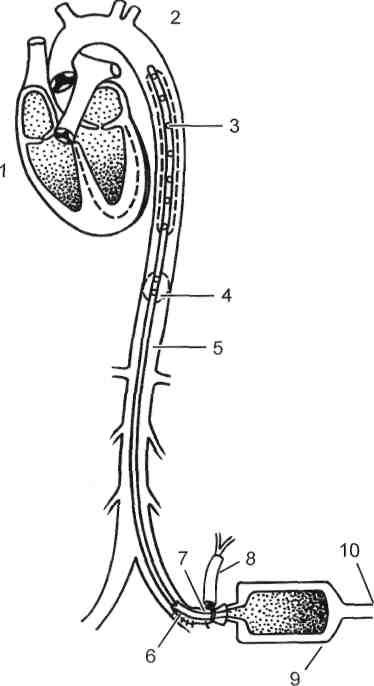 Рис. 16.2. Внутриаортальная баллонная контрапульсация. 1 — сердце; 2 — грудная аорта; 3 — баллон контрапульсатора; 4 — блокирующая просвет манжета; 5 — катетер контрапульсатора; 6 — брюшная аорта; 7 — сосудистый протез; 8 — обтяжка; 9 — контрапульсатор; 10 — пневматический источник питания контрапульсатора (схема по А. Л. Костюченко и соавт., 2000). раствора. Нередко его применяют вместе с дроперидолом (нейролепта-налгезия). Дозу дроперидола подбирают в зависимости от исходного АД: при систолическом АД не ниже 100—120 мм рт.ст. вводят 2,5 мг (1мл); 120—140 мм рт.ст. — 5 мг; 140—160 мм рт.ст.— 7,5 мг; более 160 мм рт.ст. — 10 мг. Промедол обладает относительно слабым обезболивающим действием, умеренно угнетает дыхание, несколько повышает симпатическую активность. Препарат применяют внутривенно в дозе 20 мг (1 мл 2 % раствора). Действие начинается через 3—5 мин и продолжается около 2 ч. Морфин — мощный анальгетик. Назначают по 10 мг (1,0 мл 1 % раствора) в сочетании с атропином (0,5 мл 0,1 % раствора). Внутривенно вводят медленно, дробно. Побочное действие: угнетение дыхания, брадикардия, тошнота, рвота. Морфин нельзя применять у пожилых, ослабленных больных с признаками угнетения дыхания, при гипотонии. Бупренорфин (норфин) — мощный анальгетик центрального действия (не вызывает привыкания). Вводят препарат внутривенно медленно в дозе 1—2 мл (0,3—0,6 мг). После внутривенного введения эффект достигает максимума в течение 15 мин. Продолжительность действия 6—8 ч. Побочное действие: сонливость, тошнота, рвота, угнетение дыхания. Дипидолор по активности сходен с морфином. Продолжительность действия 6 ч. Препарат вводят внутримышечно по 15 мг (2 мл 0,75 % раствора). Побочное действие: тошнота, рвота, снижение АД. Ограничение (уменьшение, предупреждение распространения) зоны ишемического повреждения является одной из главных задач лечения инфаркта миокарда в первые часы (сутки). Для этого необходимы прежде всего ранняя тромболитическая терапия и, во-вторых, эффективные действия, направленные на снижение потребности миокарда в кислороде. А Внутриаортальную контрапульсацию (артерио-артериальное нагнетание крови, синхронизированное с работой сердца больного) применяют при осложненном течении инфаркта (шок, разрыв межжелудочковой перегородки, острая митральная недостаточность при отрыве сосочковой мышцы), а также при тяжелой нестабильной стенокардии перед операцией (внутрикоронарная ангиопластика, аортокоронарное шунтирование). Наи- 350 более простым методом контрапульсации является внутриаортальная баллонная контрапульсация, или баллонирование {рис. 16.2). А Восстановление коронарного кровотока достигают с помощью внут-рикоронарного или системного тромболизиса — наиболее эффективного способа уменьшения размера инфаркта. Однако спустя 4—6 ч от начала поражения миокарда эффективность тромболитической терапии снижается, поэтому следует возможно раньше назначать нитраты и р-адреноблокаторы (пропранолол, метопролол, атенолол, тимолол). Нитраты увеличивают коронарный и коллатеральный кровоток, уменьшают потребность миокарда в кислороде за счет уменьшения пред- и постнагрузки и напряжения стенки левого желудочка; р-адреноблокаторы уменьшают потребность миокарда в кислороде, ЧСС и напряжение стенки левого желудочка. Поврежденный миокард может восстановиться, если тромболитическую терапию проводят в первые 1—3 ч после окклюзии. Однако практически трудно определить начало и скорость образования тромба, в связи с чем ее рекомендуют в первые 12 ч от начала длительного приступа интенсивной загрудинной боли. С этой целью внутривенно вводят стрептокиназу, тканевый активатор плазминогена (ТАЛ) или анизоилированный плазминоген-стрептокиназ-ный активированный комплекс (АПСАК). Применяют также стрептодеказу и проурокиназу. Сразу после или во время проведения тромболитической терапии с целью профилактики повторного тромбоза традиционно назначают гепарин и аспирин. Первую дозу гепарина (5000 ЕД) вводят внутривенно струйно, затем в виде инфузии в суточной дозе 32 000 или 24 000 ЕД (1 тыс. ед/ч). При подкожном введении гепарина используют дозу 5000 ЕД (от 2500 до 10 000 ЕД) через каждые 4 ч. Гепаринотера-пию продолжают 7—10 сут. Аспирин назначают для постоянного приема в дозе 325 мг/сут с первого дня поступления больного. Таким образом, активная (антиангинальная, тромболитическая и антиаритмическая) терапия в первые часы инфаркта миокарда, а также «агрессивная» тактика лечения в последующие дни (физическая реабилитация с первых дней болезни, внутрикоронарная баллонная ангиопластика в раннем постинфарктном периоде) улучшают прогноз как в острой фазе, так и в отдаленном периоде болезни. Оперативное лечение. Основная цель операции при инфаркте миокарда — устранение ишемизированной периинфарктной зоны, повышение сократительной функции миокарда, предотвращение увеличения зоны некроза миокарда, создание благоприятных условий для рубцевания этой зоны. Принцип операции основан на адекватном восстановлении кровотока в коронарной артерии путем создания аортокоронарного шунта (АКШ) в обход места резкого стеноза или окклюзии коронарной артерии (рис. 16.3). 16.2.2.2. Кардиогенный отек легких Кардиогенный отек легких является наиболее драматичным проявлением острой левожелудочковой недостаточности. Этому предшествует острое развитие или увеличение венозной легочной гипертензии на фоне повышения конечного диастолического давления левого желудочка и(или) левого предсердия. Повышение давления в легочных капиллярах сопровождается увеличением их проницаемости, снижением коллоидно-осмотического давления и пропотеванием плазмы в интерстициальное пространство и альвеолы. 351 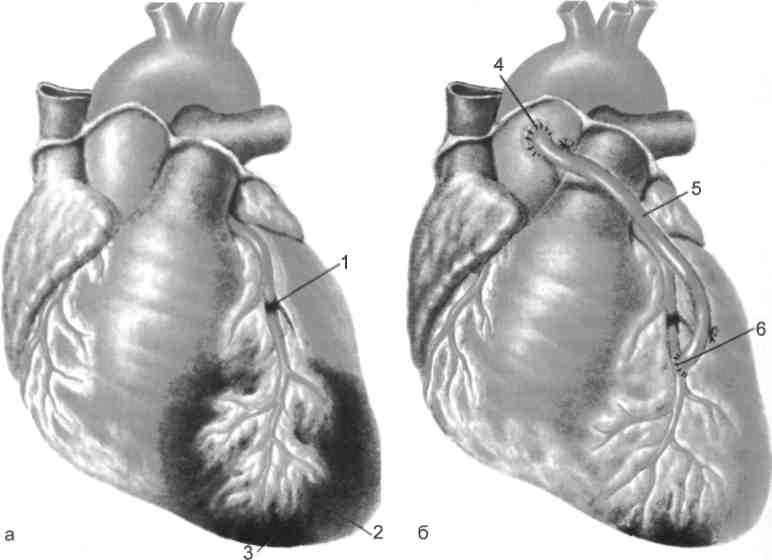 Рис. 16.3. Операция аортокоронарного шунтирования при инфаркте миокарда. а — до операции; б — после операции (видно значительное уменьшение зоны ишемии): 1 — локализация тромба коронарной артерии; 2 — зона периинфарктной ишемии; 3 — зона некроза; 4 — анастомоз трансплантата с аортой; 5 — трансплантат; 6 — анастомоз трансплантата с коронарной артерией. Клиническая картина. Кардиогенный отек легких имеет характерную клиническую картину. Внезапно развивается инспираторная одышка, вплоть до удушья. У больного появляются сильное возбуждение, одышка, кашель с отделением пенистой розовой мокроты (альвеолярный отек легких), что вызывает у него ощущение, близкое к утоплению. Пациент пытается сесть, иногда может вставать, жадно «хватает» воздух, мечется. Чтобы обеспечить возможность участия в акте дыхания дополнительной мускулатуры, опирается руками на края кровати. Дыхание становится шумным, сопровождается клокочущими хрипами на вдохе и вьщохе, слышными на значительном расстоянии. Появляется профузный пот, кожные покровы становятся холодными, землисто-серыми с цианотичным оттенком. Набухают шейные вены (повышается ЦВД), увеличивается печень. При аускуль-тации выслушивается шумное дыхание с массой разнокалиберных влажных и (часто) сухих хрипов (интерстициальный отек легких), которые вначале определяются в базальных отделах легких, но по мере ухудшения состояния распространяются к верхушкам. За исключением случаев сочетания с кар-диогенным шоком, при отеке легких повышается АД. Выявляются тахикардия, ритм галопа, глухость тонов, акцент II тона над легочной артерией. Диагностика. При рентгенологическом исследовании грудной клетки в случае интерстициального отека легких определяются нечеткость легочного 352 рисунка и понижение прозрачности прикорневых отделов. При альвеолярном отеке преобладают изменения в прикорневых отделах в виде «крыльев бабочки». Указанные изменения могут сохраняться на протяжении 24—48 ч после купирования отека легких. Стабильность рентгенологической картины отека легких прогностически неблагоприятна и всегда указывает на возможность его рецидива. На ЭКГ выявляются признаки основного заболевания — инфаркта миокарда, аневризмы левого желудочка или рубцовых изменений, пароксиз-мальной тахикардии, а также перегрузки левого желудочка и(или) левого предсердия. При эхоКГ отмечаются признаки органического поражения сердца в связи с основным заболеванием, увеличение и гипокинезия левых отделов сердца, снижение функции выброса левого желудочка, увеличение правого желудочка при тотальной сердечной недостаточности. Лечение при кардиогенном отеке легких направлено на улучшение окси-генации артериальной крови; снижение пред- и постнагрузки на левый желудочек и инотропную поддержку миокарда. С этой целью назначают:
А Наркотические анальгетики:
А Ганглиоблокаторы (с целью быстрого снижения АД и депонирования крови):
А Вазодилататоры (для снижения АД, ОПСС и венозного возврата, что приводит к увеличению фракции выброса и уменьшению конечного диастолического объема): нитроглицерин, нитропруссид натрия, изосор-битдинитрат. А Диуретики (с целью уменьшения ОЦК и дегидратации легких): фуро-семид (лазикс, фрузикс). 353 А Сердечные гликозиды: строфантин, коргликон. Инотропные препараты (с целью увеличения сердечного выброса и снижения давления в легочных сосудах): добутамин, допамин. А Инотропно-вазодилатирующее средство (инодилататоры): амринон и др. При рецидиве отека легких проводят ультрафильтрацию крови. Метод позволяет одномоментно эвакуировать значительный объем избыточной жидкости, что особенно ценно при нарушениях вьщелительной функции почек. Прогрессирующее несмотря на ингаляцию 100 % 02, нарастание гипер-капнии является показанием для интубации трахеи и начала ИВЛ. Вспомогательная или искусственная вентиляция увеличивает средний объем легких, что приводит к открытию большего количества неаэрированных альвеол и улучшает газообмен. Если отек легких является осложнением острого инфаркта миокарда (в особенности в сочетании с низким сердечным выбросом), применяют внут-риартериальную контрапульсацию. 16.2.3. Острая печеночная недостаточность Острая печеночная недостаточность — патологическое состояние, характеризующееся «срывом» компенсаторных возможностей печени и возникновением новой клинической ситуации — несоответствием между потребностью в синтезе необходимых компонентов внутренней среды (белков, факторов свертывания, гормонов) и возможностями такого синтеза печенью. Причины, вызывающие острую печеночную недостаточность: острый вирусный гепатит, лекарственные гепатиты, связанные с применением противотуберкулезных средств (изониазид, рифампицин) и антигрибковых препаратов, парацетамола, пиразинамида, отравления грибами или афлатокси-ном, интраоперационные циркуляторные расстройства, приводящие к гипоксии печени, на фоне которой может проявиться неблагоприятное действие ряда ингаляционных анестетиков (фторотан), ишемический некроз печени. В основе развития и других вариантов острой печеночной недостаточности чаще всего лежат системная гипотензия и селективное нарушение кровотока в органе. Расстройство печеночного кровотока и детерминированные им нарушения детоксикационной функции печени напрямую зависят от тяжести острой кровопотери. Присоединение эндогенной интоксикации, хирургической инфекции повышает вероятность развития острой печеночной недостаточности. В прогностическом отношении неблагоприятными факторами развития острой печеночной недостаточности считают возраст старше 60 лет, концентрацию билирубина крови выше 300—340 мкмоль/л и продолжительность желтухи более 1 -го месяца. Этиология и патогенез. Развитие острой печеночной недостаточности начинается с повреждения гепатоцитов. Различают два функциональных состояния поврежденной печени. Гепатопривный синдром проявляется в изменении функциональных показателей, характеризующих состояние этой печени. В развитии патоцеллюлярной несостоятельности ведущую роль играет снижение кислородного обеспечения паренхимы печени, в результате чего в значительной степени нарушаются биоэнергетические процессы и в гепатоцитах возникают изменения, свойственные некробиозу. Это приво- 354 дит к уменьшению массы функционально активной печеночной паренхимы до критической. |
