Системы крови
 Скачать 7.82 Mb. Скачать 7.82 Mb.
|
Стадии развития острых лейкозовРазличают две основные стадии их развития. Первая стадия – первый острый период, продолжающейся от начальных клинических признаков заболевания до ярко выраженных клинических проявлений, то есть до разгара болезни, включая начало лечения и получение положительного терапевтического эффекта. Вторая стадия – стадия ремиссии острого лейкоза, проявляющаяся ослаблением клинико-гематологических патологических сдвигов под влиянием соответствующей противолейкозной терапии, именуемой терапией индукции. Ремиссия может быть полной и неполной. Согласно ВОЗ, полной клинико-гематологической ремиссией считается состояние больного, характеризующееся полной нормализацией в течение не менее 1 месяца клинической симптоматики, анализов крови и костного мозга (наличием в миелограмме не более 5 % бластных клеток и не более 30 % лимфоцитов) и постепенной нормализацией имеющейся анемии и тромбоцитопении. 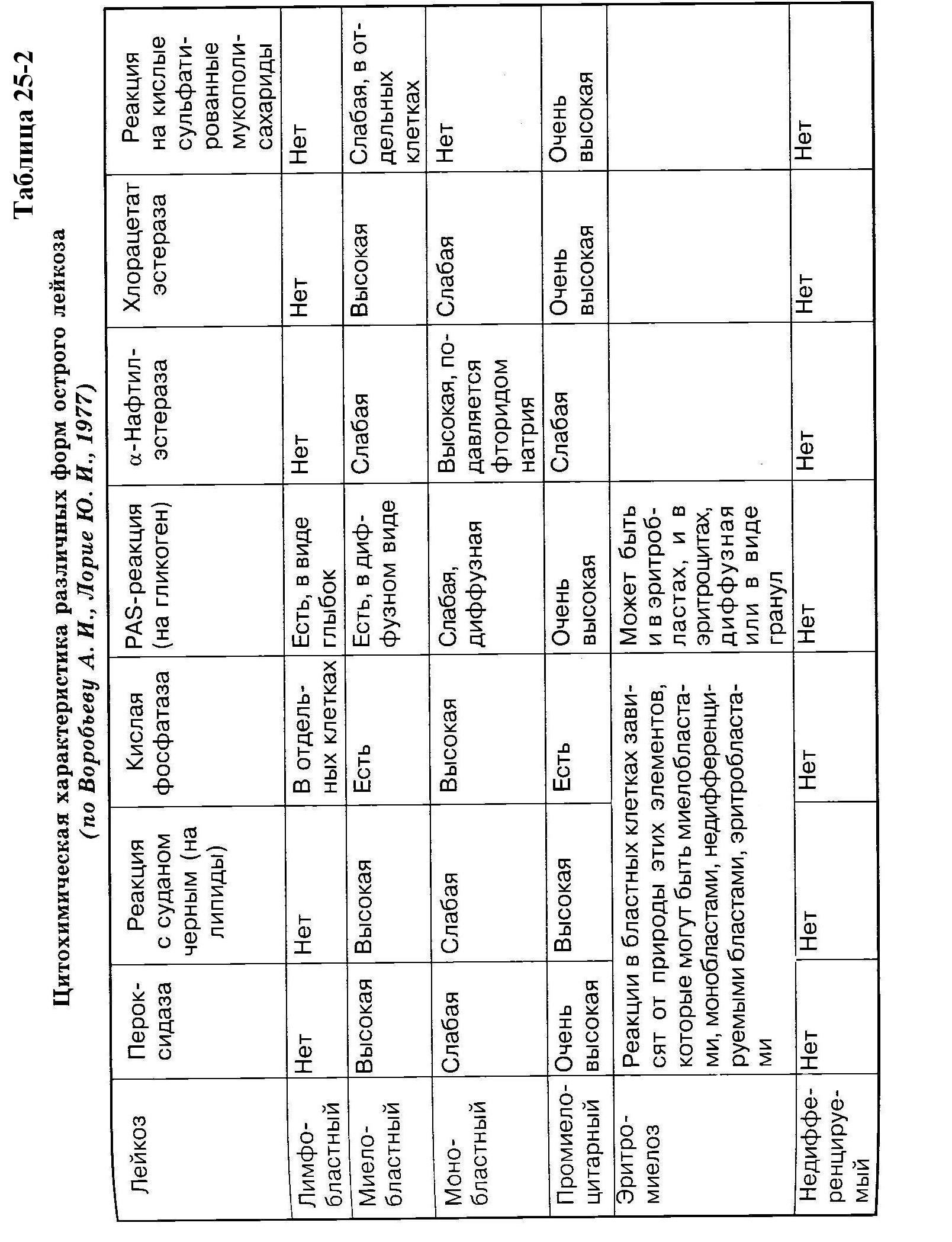 Таблица 25-3 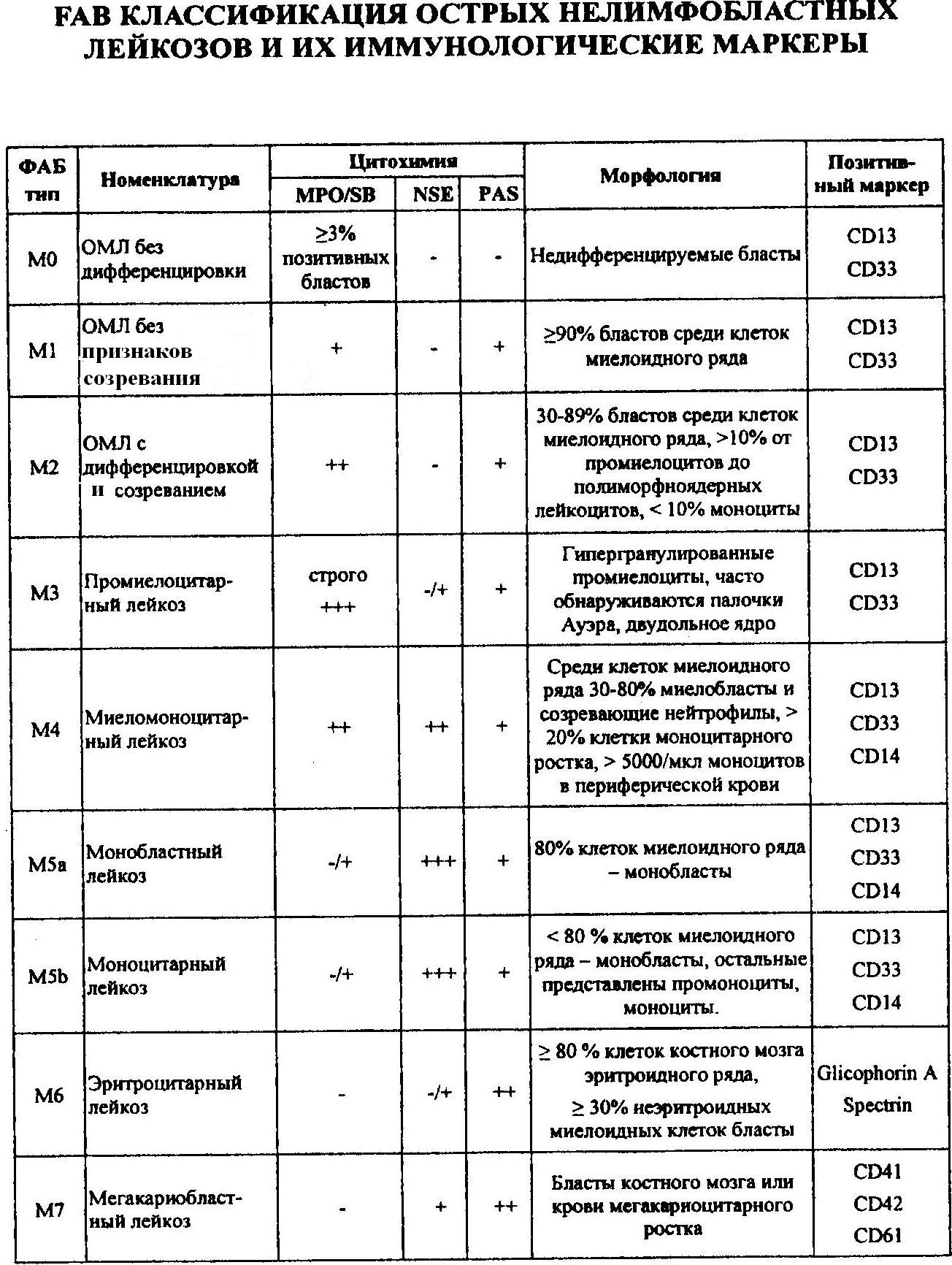 Морфологическая анаплазия клеток крови при острых лейкозах Она, главным образом, заключается в:
Увеличение ядра бластных клеток более чем на 1/3 считается признаком злокачественного течения лейкоза. Принципы лечения острых лейкозов Для выбора эффективных методов и средств лечения, необходимо своевременно и точно определить вид лейкоза (тип бластной клетки), а также стадию и тяжесть заболевания. Интенсивная комплексная терапия лейкоза должна производиться на всех этапах развития заболевания, в том числе обязательно в специализированных онкогематологических отделениях, клиниках, центрах, имеющих боксы (изоляторы), реанимационное оборудование, аппараты для лучевой терапии, средства для переливания крови и пункции костного мозга, а также операционные для пересадки костного мозга. Назначение апробированных стандартных схем и средств лечения необходимо проводить с учетом особенностей течения заболевания, наследственности и конституции организма. Лечение острых лейкозов должно включать:
При эффективном, своевременно начатом, квалифицированном, комплексном и комбинированном лечении в специализированных онкогематологических лечебных учреждениях удается получить полную ремиссию в течении 5 лет у детей с острым лимфобластным лейкозом до 80-95 % случаев и у больных разного возраста с острым миелобластным лейкозом в течении 1-2 лет в 35-70 % случаев. Выздоровевшим считают того больного, у которого отсутствует рецидив заболевания в течение 5 лет после завершения полного курса лечения. У большинства же больных, к сожалению, наступают рецидивы лейкозов. Последние могут быть ранними, возникающими уже в период проведения лечения, и поздними, проявляющимися после периода проведения лечения. 25.2.3. ХРОНИЧЕСКИЕ ЛЕЙКОЗЫ. ХАРАКТЕРИСТИКА. ПРИНЦИПЫ ЛЕЧЕНИЯ Хронические лейкозы – это длительно дифференцирующиеся опухоли белого, красного и мегакариоцитарного ростков системы крови, то есть длительно остающиеся на стадии моноклоновой доброкачественной опухоли, основу которой составляют клоны опухолевых морфологически зрелых и созревающих клеток крови (гранулоцитов, моноцито, эритро- и мегакариоцитов). Эти лейкозы развиваются преимущественно в зрелом, пожилом и старческом возрасте. Классификация хронических лейкозов определяется по: - виду усиленно функционирующего ростка кроветворной ткани (миелолейкоз, лимфолейкоз, моноцитолейкоз, эритромиелолейкоз, эритремия или истинная полицитемия, рассмотренная ранее в разделе патологии системы красной крови ); - количеству лейкоцитов в периферической крови (чаще развивается сублейкемический и алейкемический виды лейкозов); - степени дифференцируемости клеток крови (чаще обнаруживаются морфологически дифференцируемые клетки). - длительности течения (продолжительность заболевания может сильно варьировать и составлять более 2, 5, 10, 15 и даже 20 лет); - выраженности опухолевой прогрессии (признаки опухолевой прогрессии, в отличие от острых лейкозов, выражены незначительно). ХРОНИЧЕСКИЙ МИЕЛОЛЕЙКОЗ Является наиболее распространенным видом лейкоза у взрослых (встречаются в 25 % случаев). У детей развивается в 5 % случаев; мужчины болеют несколько чаще, чем женщины и при этом отмечаются два пика заболеваемости: в 15-20 лет и в 60-70 лет. Для него характерно расширение миелоидного ростка кроветворения и существенное увеличение числа опухолевых клеток всех стадий гранулоцитопоэза (от сегментоядерных до миелобластов). Чаще отмечается лейкемический, а также сублейкемический вариант течения хронического миелолейкоза. Данный вид лейкоза отличается резким (почти 10-кратным) увеличением продолжительности жизни гранулоцитов и снижением их функциональной активности. Диагностическим показателем хронического миелолейкоза с одной стороны, является появление в миелоидных клетках аномальной ( с укорочен- ным или отсутствующим длинным плечом) филадельфийской (Ph,) хромосомы, с другой, - повышение активности тирозинкиназы. В этиологии хронических миелолейкозов, наряду с действием различных мутагенов, важное место занимает хромосомные абберации, выявляемые, в среднем, в 87% случаев хронического миелолейкоза и в 26% случаев эритриемии. В патогенезе развития данного лейкоза ведущее место занимают: - расширение пула гранулоцитарных предшественников в результате изменения их чувствительности к регуляторным ФАВ и микроокружению; - усиленная пролиферация молодых клеток белой крови как в костном мозге, так и в экстрамедуллярных структурах (селезенке, печени и других органах); - снижение активности щелочной фосфатазы в гранулоцитах крови и др. В патогенезе хронического миелолейкоза важное значение отводят интра- и экстармедуллярной миелоидной пролиферации опухолевых клеток, со временем срчетающейся с развитием медуллярного склероза и фиброза. Развернутая стадия хронического миелолейкоза формируется постепенно и продолжается в течение нескольких (обычно 3-5) лет. В разгар заболевания характерны незначительные общая слабость, ухудшение общего состояния, снижение работоспособности, тяжесть и неприятные ощущения в брюшной полости, бледность кожи, гипохромная анемия, увеличение селезенки, печени; выраженный нейтрофильный лейкоцитоз с умеренным ядерным сдвигом влево и наличие всех форм гранулоцитов; появление филадельфийской хромосомы в гранулоцитах крови и костного мозга. В костном мозге отмечается постепенное замещение жировой ткани миелоидной тканью и значительное увеличение соотношения лейкоциты /эритроциты. Картина периферической крови представлена на схеме 25-1. В терминальную стадию данного вида лейкоза резко нарастают более молодые бластные клетки (миелобласты и недифференцируемые бласты), резко увеличиваются в размерах селезенка и печень, прогрессирует развитие анемии, тромбоцитопении, геморрагического синдрома, гранулоцитопении, лихорадки, инфицирования организма и возникновение прогрессирующей, резко выраженной общей слабости и возникновение болей в костях. Работоспособность снижается и исчезает. В эту стадию больные обычно живут не более 0,5-1 года. Финалом заболевания является бластный криз. Лечение хронического миелолейкоза Определяется стадией и клинической картиной заболевания. Лечение вначале проводится амбулаторно, потом периодически стационарно. Целесообразно длительное время, с перерывами назначать фитоадаптогены. Сначала использовать слабые цитостатики (гидроксимочевину, бусульфан и др.), присоединяя - интерферон и облучение селезенки, позже – более сильные цитостатики (винкристин, миелосан, имифос, рубомицина гидрохлорид, преднизолон и другие глюкокортикоиды и, наконец, миелобромол), а также блокатор мутантной тирозинкиназы (р210) – Гливека. Их основное назначение – подавить или элиминировать клон опухолевых клеток. Периодически, особенно, при эритриемии, проводятся кровопускания. Особое место в лечении заболевания, особенно в его 1 стадию, у лиц моложе 50 лет, занимает эффективная трансплантация костного мозга или стволовых клеток, приводящая до 70 % случаев к выздоровлению. Положительные действия оказывает и эффектиная, сопуствующая симптоматическая терапия, а также здоровый образ жизни. Больной постоянно должен под наблюдением врача, в том числе гематолога, и периодически сдавать кровь на анализы. Беременность прерывается. Санаторно-курортное лечение противопоказано. ХРОНИЧЕСКИЙ ЛИМФОЛЕЙКОЗ Является самым распространенным видом хронического лейкоза (лимфопролиферативного заболевнаия). Этим видом лейкоза страдают примерно 25 % людей, больных всеми видами лейкозов, особенно лица пожилого возраста. Пик заболеваемости приходится на 61-70 лет. Мужчины болеют в 2,2 раза чаще, чем женщины. У пожилых заболевание протекает более доброкачественно, у молодых – более злокачественно. У детей не встречается. Заболевание характеризуется постепенно прогрессирующим увеличением числа лимфоцитов, достигающего до 90 % всех клеток крови. Чаще отмечается лейкемический вариант его течения. Лимфоидные клетки при данном виде лейкоза развиваются из предшественников В-лимфоцитов, первично поражающих костный мозг, а в 5% случаев – из Т-лимфоцитов. Различают 2 основных варианта заболевания: 1)В-лимфолейкоз, при котором дифференцировка В-лимфоцитов не зависит от Т-лимфоцитов, 2) В-лимфолейкоз, определяемый В-клетками памяти. В патогенезе хронического лимфолейкоза важное место отводят хромосомной абберации (трисомии) по 12 хромосоме, а также нарушениям структуры 6, 11, 13, и 14 хромосом. Бластные лимфоидные клетки обычно дифференцируются до уровня, способного к рециркуляции, иногда (не более 3 % случаев) они трансфор- мируются в злокачественную опухоль. Различают следующие клинические формы хронического лимфолейкоза: доброкачественную, прогрессирующую, опухолевую, селезеночную, абдоминальную, костномозговую, пролимфоцитарную, лимфоплазмацитарную. В начале развития заболевания жалобы отсутствуют. Позже больные жалуются на общую слабость, повышенную потливость, увеличение периферических узлов. При доброкачественной форме заболевание развивается медленно, обычно не прогрессирует, отмечается выраженной (до 50·109/л) лейкоцитоз. Выделяют следующие стадии классического хронического лимфолейкоза: 0, 1, 2, 3 и 4. Стадия 0 – стадия лимфоцитоза (отмечается сублейкемический и лейкемический лимфоцитарный лейкоцитоз, средняя продолжительность жизни больного составляет 10-12 лет). Стадии 1 и 2, характеризующиеся присоединением клинических проявлений (1 – лимфоаденопатия, увеличенные и мягкие лимфоузлы в верхней половине тела, уменьшение лейкоцитоза; 2 – спленомегалия с невысоким лейкоцитозом). Продолжительность жизни больного ограничивается до 4-7 лет. Стадии 3 и 4, характеризующиеся возникновением аутоиммунной патологии (3 – аутоиммунная гемолитическая анемия, 4 – аутоиммунная тромбоцитопения). Продолжительность жизни больного в эти стадии снижается до 1,5 лет. Наряду с этими ведущими проявлениями данного заболевания отмечаются прогрессирующие анемия, геморрагический синдром, появление антител к эритроцитам, развитие гипогаммаглобулинемии, снижение клеточного и гуморального иммунитета, возникновение и усиление инфекционных и аллергических осложнений. Характерными гематологическими признаками хронического лимфолейкоза, имеющими диагностическое значение, являются: разной степени абсолютный лимфоцитоз (главным образом, за счет малых лимфоцитов с круглым ядром и узкой полоской цитоплазмы); клетки (тени) Боткина-Гумпрехта, нормоцитарная нормохромная прогрессирующая анемия; ретикулоцитоз; тромбоцитопения; снижение в плазме крови различных Ig; трисомия по 12 хромосоме; делеция 6, 11, 13 и 14 хромосом. Картина периферической крови представлена на схеме 25-1. Лечение хронического лимфолейкоза Определяется стадией, тяжестью и клинической формой данной болезни. Ведущее место в лечении хронического лимфолейкоза отводится:
В 0-й стадии заболевания и при доброкачественном его течении активной терапии не проводится. Режим и диета – обычные. Исключаются общие инсоляция, перегревание, переохлаждение. В 1-ой и 2-ой стадиях болезни назначаются лейкоран (сначала ежедневно, затем 1-2 раза в неделю, позже – 1 раз в 10 дней), циклофосфан (по схеме), глюкокортикоидные препараты – преднезалон и др. (по жизненным показаниям) и рентгенотерапия. В 3-ей и 4-ой стадиях хронического лимфолейкоза лечение осуществляют а специализированных стационарах по программам острого лимфобластного лейкоза. Ослабляют проявления аутоиммунной гкмолитичской анемии и аутоиммунной тромбоцитопении. Проводят противомикробную и антиаллергическую терапию. Следует отметить, что в результате длительного использования цитостатиков в лечении хронического лимфолейкоза, как и в лечении других форм хронических лейкозов, возможно развитие следующих осложнений:
Реабилитационная терапия сводится к проведению поддерживающей, дезинтоксикационной и симптоматической терапии при обязательном адекватном, лабораторном контроле за картиной крови. При этом обязательно исключение электро-, грязе- и бянелечения, а также инъекций витаминов и биостимуляторов. Глава 26. ТИПОВЫЕ ФОРМЫ И МЕХАНИЗМЫ НАРУШЕНИЙ ГЕМОСТАЗА Гемостаз (от греч. haima – кровь, stasis - остановка) - остановка кровотечения или кровоизлияния при повреждении кровеносных сосудов. Механизмы, обеспечивающие гемостаз, реализуются не только при повреждении всей стенки сосудов, но и при любом повреждении интимы сосудистой стенки, вызванном физическими (например, катетеризация), гемодинамическими, химическими факторами, воспалением, действием иммунных комплексов, нарушением метаболизма (атеросклероз, коллагеновые болезни) и т.д. Гемостаз достигается, главным образом, благодаря образованию пристеночного или закупоривающего (интрамурального) тромба в результате взаимодействия компонентов плазмы, тромбоцитов и сосудистой стенки. Различают два механизма гемостаза:
Преобладание того или иного механизма зависит, главным образом, от калибра поврежденного сосуда и скорости кровотока. Однако эффективный гемостаз возможен только при нормальном функционировании обоих механизмов. Функциональная неполноценность системы гемостаза может привести к локальной или генерализованной кровоточивости из сосудов соответственно с низким или высоким кровяным наполнением. Избыточность системы гемостаза может привести к образованию микро - и макротромбов, закупоривающих не только дефекты в стенках поврежденных сосудов, но и просветы последних. Расстройства гемостаза, с одной стороны, включают нарушения способности плазмы крови находиться в полужидком состоянии, а форменные ее элементы – в суспензионном (взвешенном) состоянии, то есть, нарушения беспрепятственно циркулировать в сосудистом (особенно микроциркуляторном) русле. С другой стороны, они сопровождаются расстройствами и предупреждения, и остановки кровотечения или кровоизлияния в условиях повреждения стенки сосудов различными патогенными факторами. Расстройства гемостаза возникают в результате нарушений метаболизма, структуры, функций и механизмов регуляции трех взаимосвязанных систем: 1) сосудистой (чаще всего интимы); 2) клеток крови (главным образом, тромбоцитов); 3) плазмы крови (факторы свертывающей, антисвертывающей и фибринолитической систем). |
