Пат физиология. Учебные пособия для студентов высших учебных заведений
 Скачать 7.09 Mb. Скачать 7.09 Mb.
|
|
Глава 14 . ПАТОЛОГИЧЕСКАЯ ФИЗИОЛОГИЯ СИСТЕМЫ КРОВИ Функции крови разнообразны. Циркулируя по замкнутой системе сосудов, она обеспечивает клетки органов и тканей необходимыми для питания веществами и выведение продуктов метаболизма. Через кровь координируется, регулируется деятельность функциональных систем, поддерживается гомеостаз, характерный для каждого вида животного, определенный ходом эволюционного развития. Постоянство состава и свойств крови может быть нарушенным, что ведет к патологическим изменениям в организме. С другой стороны, расстройства, возникающие в деятельности клеток, органов, тканей, находят свое отражение в системе крови. Поэтому у животных рассматривают первичные и вторичные патологические изменения крови. Первичные могут быть обусловлены патологией органов гемопоэза, органов, в которых зарождаются и созревают клетки крови, патологией системы гемодиереза, обеспечивающей разрушение этих клеток, и нарушениями самой циркулирующей и депонированной, так называемой периферической крови. Изменения крови вторичного генеза возникают в тех случаях, когда патологические процессы поражают другие органы и ткани. Такое деление несколько условно, не всегда можно отличить первичные патологии от вторичных. Тем не менее по состоянию крови ветеринарные врачи нередко устанавливают диагноз, этиологические факторы и генез многих заболеваний животных. 14.1. НАРУШЕНИЯ ОБЩЕГО ОБЪЕМА КРОВИ Отношение массы крови к массе тела у разных представителей животного мира неодинаково. У взрослых животных общее содержание крови колеблется в пределах 5—15% массы тела. Наибольшее количество крови у северных оленей (до 15 %), наименьшее — У откормочных свиней сальных пород (4,6 %). Кровь, содержащуюся в организме, подразделяют на циркулирующую и депонированную в капиллярах селезенки, печени, легких, кожи, других органов (40—45 %). Особенно много, до нескольких килограммов, крови депонируется в селезенке лошади, находящейся в покое. физиологических условиях (бег) или при патологии (лихорадка) резервные эритроциты элиминируют в кровь и обеспечивают потребность усиленно функционирующих органов. Цельная кровь состоит из форменных элементов и жидкой части — плазмы. Форменные элементы в среднем составляют 35— 48 %, плазма — 65—52 %. Каждый вид животных имеет свои показатели, но они колеблются в пределах приведенных чисел. Отношение объема форменных элементов к объему плазмы носит название гематокрита. Различные патологические процессы сопровождаются изменениями общей массы циркулирующей крови и соотношения между форменными элементами крови и плазмы. Рассматривают три типовые формы таких нарушений: нормоволемия, гиперволемия, гиповолемия. Нормоволемия (от лат. norma — образец, франц. volime — объем). Общий объем крови в организме не изменен, но нарушено обычное соотношение форменных элементов и плазмы. Поэтому выделяют нормоволемию олигоцитемическую и полицитемическую. Олигоцитемическая нормоволемия. Характеризуется уменьшением количества форменных элементов крови. Показатель гематокрита падает ниже 35 %. Причинами олигоцитемической нормоволемии у животных нередко служат гемоспоридиозы, вызывающие гемолиз, подавление гемопоэза. Снижение числа эритроцитов в крови приводит к гипоксемии и последующей гипоксии. Снижение числа лейкоцитов тормозит сопротивляемость организма инфекциям, инвазиям. Тромбоцитарная недостаточность проявляется сниженной способностью крови к свертыванию. Полицитемическая нормоволемия. Характерна увеличением числа клеток крови при ее нормальном объеме. Показатель гематокрита более 45 %. Хронические гипоксические состояния — наиболее частые причины полицитемической нормоволемии. Сгущение крови, повышение вязкости нарушают ее циркуляцию в сети капилляров. Замедление кровотока снижает интенсивность транскапиллярного обмена, способствует тромбообразованию и появлению инфаркта. Гиперволемия (от греч. hyper — над, сверх нормы, франц. volime — объем). Общий объем крови, свойственный каждому виду животных, увеличен. По соотношению форменных элементов и плазмы крови рассматривают три формы гиперволемии: нормоцитемическую, полицитемическую, олигоцитемическую. Нормоцитемическая гиперволемия. Увеличение общей массы крови не сопровождается изменением соотношения форменных элементов крови и плазмы. Показатель гематокрита остается в обычных для животных данного вида пределах. Такая гиперволемия встречается довольно редко, она возможна за счет переливания крови, непродолжительна. Полицитемическая гиперволемия. Увеличение общей массы крови происходит за счет форменных элементов. Показатель гематокрита выше нормы, например, у собак выше 45,5 %, у свиней выше 41,5 %. Основной причиной одновременного увеличения массы крови и форменных элементов считают хроническое кислородное голодание. Красный костный мозг усиленно выбрасывает в кровь эритроциты, находится в гиперрегенераторном состоянии. Полицитемию наблюдают при пороках сердца, недостатке кислорода в окружающей среде, хронической недостаточности кровообращения, недостаточности биологического окисления, эмфиземе легких. Эта форма гиперволемии представляет собой компенсаторную реакцию организма, обусловленную гиперрегенераторным состоянием клеток красного костного мозга. Снижение атмосферного давления в условиях высокогорных пастбищ сопровождается развитием у животных полицитемической гиперволемии. Олигоцитемическая гиперволемия. Характеризуется увеличением массы крови за счет ее жидкой части, поэтому подобное состояние носит еще название гидремии, гемодилюции. Показатель гематокрита меньше нижних значений физиологических колебаний. Такая волемия бывает у животных за счет введенных в рацион жидких кормов — отходов пивоваренного и сахарного производств. Олигоцитемическая гиперволемия может быть также результатом затруднения образования и выведения мочи при заболеваниях почек, усиленного выброса антидиуретического гормона задней долей гипофиза. Гиповолемия (от греч. hypo — ниже, франц. volime — объем). Представляет собой снижение общей массы крови в организме с нарушениями соотношения форменных элементов крови и плазмы. Рассматривают три ее формы: простую, олигоцитемическую и полицитемическую. Простая гиповолемия. Возникает при равностепенном понижении объема клеток крови и плазмы. Гематокрит не изменен. Наиболее частые причины — острая кровопотеря, состояние коллапса, вызванного системной вазодилатацией, и торпидная фаза шока. Нормоцитемическая гиповолемия проявляется признаками, свойственными основному страданию, симптоматикой компенсаторных реакций. Олигоцитемическая гиповолемия. Представляет собой уменьшение объема крови преимущественно за счет форменных элементов. Показатель гематокрита понижен, т. е. менее 35 % у лошадей, ниже 38 % у кур. У сельскохозяйственных животных такая гиповолемия часто сопровождает кровепаразитарные болезни: пироплазмоз, бабезиоз, нуталлиоз. Кровепаразиты, внедряясь в эритроциты, на определенной стадии развития разрушают их, вызывая гемолиз. Снижение объема крови возможно и за счет подавления гемопоэза. Проявляется недостаточностью кровоснабжения органов и тканей, в случае непринятия лечебных мер гиповолемия может стать причиной гибели больного животного. Полицитемическая гиповолемия. Развивается в результате преимущественной потери плазмы крови. Гематокритный показатель существенно превышает исходный, нормальный уровень. У свиней он становится выше 43 %, у обезьян — более 46 %. Важнейший признак дегидратации, сопровождающий диарею разного, чаще инфекционного, происхождения, гипертермию, лихорадочную реакцию, дефицит питьевой воды, сахарный и несахарный диабет, ожоговую болезнь. Полицитемическая гиповолемия — важнейший патогенетический фактор в генезе основного заболевания. Потеря организмом воды сопровождается расстройством циркуляции крови, особенно в микроциркуляторном русле. Эксикоз (обезвоживание) весьма опасен для молодняка животных. Возникающая аутоинтоксикация способствует гибели больных. 14.2. НАРУШЕНИЯ КОЛИЧЕСТВЕННОГО И КАЧЕСТВЕННОГО СОСТАВОВ ЭРИТРОЦИТОВ Жизнедеятельность организма зависит прежде всего от обеспеченности кислородом органов и тканей. Усваивают и транспортируют кислород от легких к клеткам специализированные элементы крови — эритроциты. Они же приносят двуокись углерода от клеток к легким, выполняют некоторые другие функции. Эритроциты составляют в среднем 30 (овцы) — 45 % (собаки) массы крови. Число эритроцитов колеблется у животных разных видов. Наименьшее их количество содержит кровь кур — 2—3 млн/мкл (х 1012/л; Т/л), наибольшее — кровь коз— 12—18 млн/мкл. Кровь большинства домашних животных содержит эритроциты в пределах 6,5—9,5 млн/мкл. У женских особей их несколько меньше, чем у мужских. Патологические изменения форменных элементов красной крови касаются их количественного состава и качества. Эритроцитов в крови может быть больше или меньше, что определяется соотношением образования клеток в органах эритропоэза и разрушением, потерей при кровотечениях, перераспределением, депонированием. Качественные изменения эритроцитов возникают за счет нарушения их созревания в красном костном мозге, наследуемых аномалий строения, расстройств обмена веществ. Эритроцитоз (от лат. erythrocytus — эритроцит, греч. osis — патологическое увеличение) — увеличение содержания эритроцитов в единице объема крови. Он может быть абсолютным и относительным, первичным (врожденным) и вторичным (приобретенным). Первичный (врожденный) эритроцитоз встречается редко. Это самостоятельное, генетически обусловленное заболевание, являющееся нозологической единицей. У человека наиболее часто встречается так называемая болезнь Вакеза, названная по имени автора, описавшего ее еще в 1862 г. В отношении животных ветеринарная медицина располагает сообщениями лишь о случаях первичного эритроцитоза у крупного рогатого скота и собак. Так, в стаде джерсеев, полученном с применением инбридинга, были выявлены телята с повышенным содержанием эритроцитов — от 15,8 до 25,5 млн/мкл, гемоглобина от 192 до 292 г/л и значением гематокрита от 60 до 80 %. Наследование признака шло по аутосомно-рецессивному типу, с высокой степенью летальности. Описаны единичные случаи заболевания первичным эритроцитозом взрослых кобелей кокер-спаниелей. Первичный эритроцитоз обусловлен чаще гиперплазией элементов красного костного мозга неопластической природы. Поэтому эритроцитоз сопровождается лейкоцитозом и тромбоцитозом. Абсолютный эритроцитоз вторичного происхождения (приобретенный) представляет собой один из симптомов, встречающихся нередко при различных патологических процессах, болезнях. Устранение причин, излечение болезни приводят к восстановлению числа эритроцитов. Наиболее часто вторичный эритроцитоз у домашних животных обусловлен недостаточностью дыхания. Сужение трахеи и бронхов, пневмо- и гидроторакс, хронические заболевания легких, недостаточная вентиляция животноводческих помещений, особенно птичников, разреженный воздух в горных условиях содержания животных затрудняют поступление достаточного количества кислорода в ткани. Пороки сердца, эмфизема легких также сопровождаются кислородной задолженностью. Эритроцитоз можно легко вызвать экспериментально, поместив животное в барокамеру со сниженным атмосферным давлением. Кислородное голодание тканей (гипоксия) является мощным инициатором синтеза эритропоэтинов, активно стимулирующих функцию эритроцитарного ростка красного костного мозга, что определяет повышенный выброс эритроцитов в кровь, увеличение содержания гемоглобина. Эритроцитоз в этих случаях носит адаптивный характер, способствует нормализации кислородного обеспечения тканей, предупреждает гипоксию и ее последствия. Излишнее количество эритропоэтина поступает в кровь при ишемизации почки, селезенки, печени или появлении новообразований в этих органах. Эритроцитоз, не являясь в этих случаях уже адаптивной реакцией, может сопровождаться негативными для животного организма явлениями. Увеличение объема циркулирующей крови, повышение ее вязкости, нарушения микроциркуляции приводят к расстройствам сердечной деятельности, гипертензии, повышенному тромбообразованию, а в последующем к кровоточивости. Относительный эритроцитоз вторичного происхождения выявляют у домашних животных при всех состояниях, вызванных чрезмерной потерей жидкости. Сгущение крови за счет снижения содержания плазмы наблюдают при усиленной мышечной нагрузке, обильном отделении пота, диареях разного происхождения, гипертермии, лихорадке, полиурии, перераспределении клеток. Содержание эритроцитов и гемоглобина в единице объема крови увеличивается за счет снижения объема плазмы. Другой причиной относительного эритроцитоза может быть выброс в ток крови эритроцитов из депонирующих органов. Например, у лошадей в отличие от животных других видов во время лихорадки, индуцированной пирогеналом, существенно возрастает число циркулирующих клеток красной крови. Так, если в исходном состоянии их количество равнялось (6,8 ± 0,2)1012/л, гемоглобина было 115 ± 2 г/л, гематокрит составлял 35,3 ± 0,7 %, то во время лихорадки эти показатели были уже следующими: количество эритроцитов — (8,5 ± 0,2)1012/л, гемоглобина —141+4 г/л, гематокрит —43,4 ± 0,9 %. По восстановлении температуры тела до исходной величины число эритроцитов приближалось к норме. Эритроцитоз сочетался с равностепенным возрастанием количества гемоглобина и показателей гематокрита. Объяснить данный феномен можно только тем, что у лошадей во время лихорадочной реакции эритроциты были элиминированы из селезенки, которая в условиях покоя у животных этого вида может содержать до 4 кг форменных элементов крови. Эритропения (от лат. erythrocytos — эритроцит, греч.реniа — бледность) — снижение числа эритроцитов в единице объема крови относительно их нормального содержания, свойственного животным каждого вида. Эритропения — не самостоятельное заболевание, она отражает процессы, происходящие в органах кроветворения и циркулирующей крови. Уменьшение количества эритроцитов всегда сопровождается гипогемоглобинемией. Анемия (от греч. an — отрицание, haima — кровь) — состояние организма, характеризующееся уменьшением содержания гемоглобина в единице объема крови и наличием патологически измененных форм эритроцитов. Анемия не представляет собой отдельную нозологическую единицу, а является симптомом того или иного патологического процесса, состояния или болезни. Почти всегда она сопровождается эритропенией. Эритропения становится результатом убыли эритроцитов (кровопотеря), ингибиции эритропоэза (лучевая патология), гемолиза (кровепаразиты) или сочетания этих факторов. При некоторых же патологических ситуациях число эритроцитов не изменяется. Так, недостаток железа в рационе животных приводит к анемии, характеризующейся снижением содержания гемоглобина в каждом отдельном эритроците, число которых, однако, остается неизменным. Анемии дифференцируют по вызвавшим их причинам на первичные и вторичные. Первичные анемии обусловлены врожденными аномалиями эритропоэза, вторичные являются следствием неблагоприятных воздействий среды в постнатальном онтогенезе. По патогенетическому принципу анемии подразделяют на гемолитические, постгеморрагические и связанные с разрушениями эритропоэза (дизэритропоэтические). Последние, в свою очередь, подразделяются на регенераторные, арегенераторные и апластические. По цветовому показателю выделяют нормохромную, гипохромную и гиперхромную анемии. Анемия может протекать остро, развиваясь в течение 2— 3 нед, и хронически, продолжаясь месяцы и годы. Для анемических состояний клиническая симптоматика у животных разных видов имеет много общего. Анемичные животные отличаются сниженной продуктивностью и работоспособностью, вялой реакцией на окружающие раздражители, ослабленными рефлексами. Важным признаком анемии являются бледность слизистых оболочек, иногда желтушность, кровоизлияния. Дыхание учащенное, поверхностное. Тахикардия сочетается со слабым, плохого наполнения пульсом. Сравнительно небольшая нагрузка вызывает неадекватную реакцию со стороны сердечно-сосудистой системы и органов дыхания. Аппетит чаще всего подавлен, упитанность низкая. Особенно чувствителен к анемии разного происхождения молодняк животных. Он отстает в росте, животные вялые, апатичные. Сопутствующая анемии гипоксия снижает иммунологическую реактивность и неспецифическую резистентность. Животные становятся более чувствительными к негативным факторам среды, особенно инфекционной и инвазионной природы. Основным критерием в оценке анемических состояний является гематологическое обследование. В крови больных всегда снижено содержание гемоглобина до 50 % и более. В большинстве случаев параллельно падает число эритроцитов в единице объема крови, но при отдельных формах анемии (железодефицитная) их число колеблется в пределах нормы (рис. 18). Для анемий различного происхождения характерно наличие патологических форм эритроцитов:
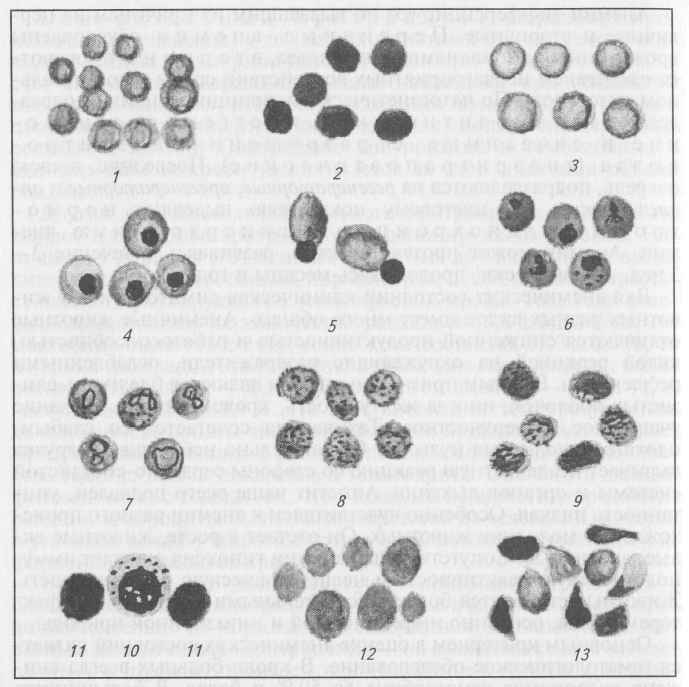 Рис. 18. Нормальные и патологические формы эритроцитов: 1 — нормоциты; 2 — гиперхромные эритроциты; 3— гипохромные эритроциты; 4— нормобла-сты; 5 — выталкивание ядра; 6— тельца Жолли; 7— кольца Кебота; 8— базальная пунктация; 9— полихроматофильные эритроциты; 10— мегалобласт; 11 — мегалоциты; 12— анизоцитоз; 13 — пойкилоцитоз
Развитие анемии зависит от многих факторов, поэтому наибольшее значение в ветеринарной медицине придают их систематизации по патогенетическим признакам. Постгеморрагическая анемия — состояние, связанное со значительной кровопотерей. Кровопотери являются следствием травматического повреждения стенки кровеносного сосуда. Нарушение ее целостности возможно в результате внешнего воздействия или патологических процессов, происходящих непосредственно в стенке сосуда либо в окружающих его тканях. Кровопотеря может быть результатом излияния крови во внешнюю среду через сосуды поврежденной кожи, слизистых оболочек желудочно-кишечного тракта, дыхательного аппарата, мочеполовых путей. Такое кровотечение называют наружным. Выход крови через травмированные сосуды в полости приводит к внутренним кровотечениям. Скопление крови в брюшной полости носит название гемоперитонеума, в плевральной — гемоторакса, в полости перикарда — гемоперикардиума. Внутренние кровотечения опасны тем, что свертывание крови происходит намного медленнее, чем при наружном кровотечении, поэтому повреждение, даже мелких брыжеечных сосудов может завершиться летальным исходом. Кроме того, затруднена диагностика внутренних кровотечений, что мешает принятию своевременных лечебных мер. Опасность постгеморрагической анемии зависит также от количества и скорости истечения крови. Острая постгеморрагическая анемия развивается быстро в результате повреждения крупных кровеносных сосудов. Анемию средней тяжести наблюдают при потере 30 % эритроцитов, потеря же 50—60 % крови сопровождается очень тяжелым состоянием животного, несовместимым с жизнью. Чувствительность к потере крови у разных животных неодинакова. Она зависит от видовых и индивидуальных особенностей организма, исходного состояния. Установлено, что наиболее чувствительны к кровопотере свиньи, собаки; наиболее устойчивы лошади, крупный рогатый скот. Основным, ведущим патогенетическим фактором в развитии острой постгеморрагической анемии является снижение общего объема циркулирующей крови. Развивается гипотензия, сопровождающаяся коллапсом. Падение уровня артериального давления сочетается с эритропенией и кислородным голоданием тканей (гипоксией), к которому наиболее чувствителен головной мозг. По мере падения уровня артериального давления и развития гипоксии вовлекаются срочные механизмы компенсации. В обычных условиях гомеостаз контролируют баро- и хеморецепторы, заложенные в сосудистых рефлексогенных зонах (дуга аорты, каротидный синус, устье полых вен). Гипотензия, измененный газовый состав крови, воспринимаются рецепторными образованиями. Информация от рецепторов передается сердечно-сосудистым центрам продолговатого мозга и тесно взаимодействующему с ними дыхательному центру. По центробежным нервам импульсы достигают органов-эффекторов. Стимулируется сердечная деятельность, выбрасывается депонированная кровь, сужаются сосуды, развивается компенсаторная одышка. В тяжелых случаях кровопотерь, нередко сопровождающих патологически протекающие роды у коров, одышка сопровождается необычным дыханием — широко открыт рот, свешен язык, дыхательные движения частые, поверхностные. Наряду с рефлекторными компенсаторными реакциями развивающаяся гиповолемия стимулирует поступление в ток крови межклеточной жидкости, пополняющей ее объем. Гипоксемия и последующая гипоксия повышают образование гемопоэтинов, в том числе эритропоэтина, усиливающего эритропоэз в красном костном мозге. Интенсивное поступление в ток крови эритроцитов постепенно восстанавливает их содержание, нормализует функциональную активность системы красной крови. Процесс восстановления продолжается 2—3 нед. Хроническая постгеморрагическая анемия — состояние, обусловленное сравнительно небольшими, но длительными кровотечениями. Причинами таких кровопотерь чаще всего бывают язвенные поражения желудка и кишечника у пушных зверей, свиней, собак; попадание инородных тел в преджелудки жвачных и прободение ими стенок рубца, сетки, книжки; развитие новообразований во внутренних органах животных и поражение ими тканей полового аппарата лошадей, собак; паразитоценозы лошадей, крупного рогатого скота. Кроме того, хроническая постгеморрагическая анемия может быть следствием острой кровопотери в условиях дефицита железа или функциональной недостаточности красного костного мозга, когда становится проблематичным быстрое восстановление функционально полноценных клеточных элементов системы красной крови. Основным патогенетическим фактором, определяющим негативные для организма последствия хронической постгеморрагической анемии, является дефицит железа, который приводит к постепенному развитию гипоксии со всеми вытекающими неблагоприятными для организма последствиями. Гемолитическая анемия возникает как следствие гемолиза эритроцитов различными агентами биологического, химического, физического происхождения. Разрушение эритроцитов, как правило, происходит в просвете кровеносных сосудов, но может быть и результатом усиленного эритроцитолиза в тканях, особенно селезенки. Гемолитические агенты биологического происхождения имеют наибольшее значение в генезе рассматриваемой анемии. Прежде всего это большая группа возбудителей кровепаразитарных заболеваний животных — пироплазмоза лошадей, рогатого скота, свиней, собак; бабезиоза рогатого скота, оленей, свиней; нуталлиоза лошадей; анаплазмоза рогатого скота; трипаносомоза лошадей, крупного рогатого скота, верблюдов. Эти заболевания домашних животных объединены тем, что паразитирующие простейшие, попадая различными путями в организм, поселяются и размножаются внутри эритроцитов, разрушают их. Прогрессивно нарастает число гемолизированных клеток. Так, пироплазмоз крупного рогатого скота сопровождается падением числа эритроцитов в тяжелых случаях до 1 млн/мкл, а содержания гемоглобина — до 15— 20 г/л; нуталлиоз лошадей характерен возможным снижением количества эритроцитов до 3 млн/мкл, гемоглобина — до 31 г/л (рис. 19). 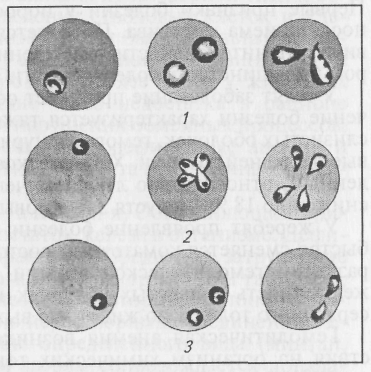 Рис. 19. Гемоспоридиозы, сопровождающиеся гемолитической анемией: 1- пироплазмоз овец; 2- нутталиоз лошадей; 3- бабезиоз крупного рогатого скота Продукты жизнедеятельности паразитов, циркулируя в крови, поражают жизненно важные органы (сердце, почки, печень, селезенка), приводят к нарушению их структуры и функции. Красный костный мозг не в состоянии пополнять дефицит эритроцитов. Развитие анемии сопровождается появлением в крови незрелых форм эритроцитов. Обнаруживаются анизоцитоз, пойкилоцитоз, базофильная зернистость. В крови появляются нормобласты, ретикулоциты. Изменяются количественный и качественный составы клеток белой крови. Наряду с другими характерным клиническим признаком для всех болезней является гемоглобинурия, т. е. окрашивание мочи в бурый цвет («кровавая моча») за счет гемоглобина, освобождаемого гемолизированными эритроцитами. Своевременное лечение больных гемоспоридиозами животных приводит к выздоровлению, хотя анемическое состояние и желтушность слизистых оболочек некоторое время еще сохраняются. Самоисцеление редко, чаще заболевшее животное, не получившее врачебной помощи, погибает. Гемолитическая анемия биологического происхождения может быть обусловлена и ядами, попадающими в организм при укусах жалящими насекомыми (пчелы, осы, гнус), змеями. Особенно чувствительны к змеиному яду лошади. Нередки случаи смерти этих животных от гемолиза, обусловленного укусами ядовитых змей. Разрушить мембрану эритроцитов способны также экзо- и эндотоксины бактерий (гемолитический стрептококк), вирусы (инфекционная анемия лошадей), переливание несовместимой крови, аутоантитела. Расстройствам функций иммунной системы, способствующим образованию аутоантител или стимуляции Т-киллерных клеток, направленных на уничтожение собственных эритроцитов, придают большое значение в современной гуманной медицине. Аутоантитела как причина гемолитической анемии у животных только начинают привлекать интерес исследователей. Так, описана гемолитическая анемия с желтушным окрашиванием тканей у жеребят, мулят, ослят, вызванная гемолизинами, полученными с молоком от сенсибилизированных матерей. Гемолизирующие антитела возникали в организме матерей после перенесенного переливания крови, вакцинации прививочным материалом, содержащим эритроцитарные антигены, трансплацентарной изоиммунизации матери эритроцитарными антигенами плода. У молодняка крупного рогатого скота острая гемолитическая анемия проявлялась после вакцинации матерей препаратами, содержащими эритроцитарный антиген. Аналогичные поражения описаны и у свиней. Гемолитическую болезнь новорожденных (желтуха новорожденных) наблюдают у поросят, телят, жеребят в случае несовместимости крови плода с кровью матери, оплодотворенной гомозиготным производителем в отношении эритроцитарных антигенов. Первые признаки болезни у поросят появляются спустя сутки после приема молозива. Появляется желтушность, ее тяжесть зависит от интенсивности разрушения эритроцитов. Течение острое, большинство заболевших погибает спустя 6—36ч. У телят заболевание протекает остро и хронически. Острое течение болезни характеризуется тяжелой анемией, желтушностью слизистых оболочек, гемоглобинурией, летальным исходом в первые пять дней желтухи. Хроническое заболевание отличается медленным, относительно легким течением. Гематокрит изначально снижен до 18 %, а спустя 3 нед повышается до 30 %. У жеребят проявление болезни вариабельно. Острое течение быстро сменяется коматозным состоянием. При более медленном развитии гемолитической анемии отмечаются гемоглобинурия, желтушность слизистых оболочек и склеры, одышка, усиление сердечного толчка, но животные выживают. Гемолитическая анемия возникает и как следствие воздействия на организм химических токсигенов. К гемолитическим ядам относят соединения фосфора, мышьяка, меди, свинца, нитробензол, бертолетову соль, фенилгидразин, гербициды, инсектициды, другие соединения. Так, экспериментальная гемолитическая анемия у кур, вызванная введением фенилгидразина, сопровождалась использованием костномозгового резерва эритроцитов, активной пролиферацией эритро- и гранулоцитопоэтических клеток. Нормализация гемопоэза в костном мозге наступала уже спустя 7 дней после прекращения действия вредящего фактора. Наибольшее количество макрофагов, участвующих в утилизации разрушающихся эритроцитов, выявлена в печени, селезенке, легких, костном мозге. Признаков экстрамедуллярного кроветворения не обнаружено. Гемолиз эритроцитов наблюдают при действии на животных физических факторов, таких, как высокая температура, вызывающая ожоговую болезнь, низкая температура (обморожения), повреждения ионизирующей радиацией. Наследственные аномалии, сопровождающиеся гемолитической анемией, изучены недостаточно. Они описаны при паралитической гемоглобинемии у лошадей, послеродовой и хронической гемоглобинуриях у крупного рогатого скота. Дизэритропоэтическая анемия возникает как результат преимущественного подавления эритропоэза в красном костном мозге. Апластические или гипопластические дизэритропоэтические анемии могут быть результатом прямого повреждающего действия вредоносного фактора на клетки красного костного мозга и результатом дефицита в организме компонентов (микроэлементы, витамины), необходимых для нормального эритропоэза. Прямое повреждение стволовым клеткам красного мозга наносит ионизирующая радиация. В зависимости от дозы облучения: наступает либо гипоплазия, либо аплазия кроветворной ткани, сопровождающаяся анемией. Поражение стволовых клеток и клеток—предшественников миелопоэза может быть результатом действия химических (цитостатики, антибиотики, аминазин и др.) и биологических (вирусы) факторов. Наиболее часто у животных наблюдают анемии, возникающие из-за недостатка в рационе микроэлементов, витаминов или нарушения обменных процессов. В первую очередь к ним относят железодефицитные анемии и анемии, развивающиеся вследствие дефицита кобаламина и фолиевой кислоты. Железодефицитная анемия. Объединяющий признак этой группы анемий — недостаток железа в организме. Дефицит железа вызывают многие факторы. Среди них затруднение всасывания железа в желудочно-кишечном тракте при гастритах, энтеритах, ахилии, язвенной болезни. Некоторые компоненты рациона способствуют образованию нерастворимых соединений железа. Скармливание сырой рыбы определенного вида (минтай, пикша, путассу, сайра) пушным зверям сопровождается попаданием в организм триметиламиноксида, при участии которого образуются нерастворимые соединения железа, не усваиваемые животными. Варка рыбы предупреждает развитие анемии, особенно часто регистрируемой в подобных случаях у норок. Одной из причин развития дефицитной по железу анемии является его повышенное расходование при хронических кровопотерях, вызванных заболеваниями (язвенная болезнь желудка пушных зверей, свиней; хроническая гематурия крупного рогатого скота), повышенной лактацией, интенсивной мышечной работой. Основной же причиной железодефицитной анемии у домашних животных является алиментарная недостаточность. Неполноценное кормление взрослых животных, дефицит железа в молозиве и молоке снижают его содержание в клетках красного костного мозга, эритроцитах, плазме крови. Анемию у новорожденных телят, ягнят, жеребят, поросят, щенков пушных зверей наблюдают тогда, когда в организме лактирующих матерей недостаточен уровень железа. Содержание гемоглобина у больных телят может колебаться от 80 до 40 г/л, тогда как у здоровых оно в пределах 100—115 г/л. Безвыгульное содержание свиноматок лишает их возможности пополнять запасы железа путем поедания глины, других богатых микроэлементами веществ. В подобных условиях поросята-сосуны могут получать с молоком лишь около 1 мг железа в сутки при потребности 7—10 мг, количество гемоглобина у них снижается до 25%, а падение гемоглобина до 2—4 % ведет к летальному исходу. Не регистрируют железодефицитную анемию там, где свиньям предоставлен выгульно-пастбищный режим. Недостаточное поступление железа в организм новорожденных ягнят с молоком матерей на фоне интенсивного роста определяет развитие выраженной анемии уже к 2—3-недельному возрасту, когда происходит удвоение массы тела. Изначальный скрытый дефицит железа сменяется анемией микроцитарного, гипохромного характера со снижением числа эритроцитов, гемоглобина в единице объема крови, уменьшением гематокритной величины, увеличением СОЭ, появлением анизоцитов, пойкилоцитов, базофильной зернистости и полихроматофильных эритроцитов. Весьма чувствительны к недостатку железа щенки пушных зверей клеточного содержания. В крови анемичных норок содержание железа может упасть до 50 мг/100 мл. Гибель щенков от железодефицитной анемии может достигать 20—30 % и более. Железодефицитная анемия зарегистрирована и у птиц. Установлено, что у кур (300—360-дневный возраст) в период максимальной яйценоскости развивается синдром умеренной гипохромной анемии. С изначальных величин 108 ±1,1 г/л количество гемоглобина падает до 77—79 г/л. Суточные цыплята, полученные из яиц больного анемией родительского стада, также имеют явные признаки малокровия (гемоглобина 70 ± 0,6 г/л). Внешне это проявляется белопухостью, бледно-гребешковостью, низкими массой и сохранностью. С целью предупреждения и лечения анемических состояний больным животным назначают легкоусвояемые комбинированные препараты железа, кобальта, цинка и марганца, вводимые в рацион или путем парентеральных инъекций. Витамин В12 (фолиево)-дефицитные анемии развиваются как следствие недостатка в организме антианемического фактора, обеспечивающего нормальный эритропоэз. Антианемический фактор состоит из двух компонентов — внешнего и внутреннего. Внешний (фактор Касла) представляет собой витамин В12 (цианкобаламин). Дефицитная по этому витамину анемия развивается в результате его недостаточного поступления в организм с кормом, нарушенного усвоения или усиленного расходования. Поступая в достаточном количестве, витамин В12 образует комплекс с внутренним антианемическим фактором, синтезируемым париетальными клетками желудка. Это гликопротеин с молекулярной массой 50 000—60 000 Да. Комплексное соединение через слизистую оболочку подвздошной кишки поступает в кровь и депонируется преимущественно в печени. Из печени витамин В]2 поступает в красный костный мозг, в котором он используется для синтеза нуклеиновых кислот эритрокариоцитов. Одна из коферментных форм витамина В12 — метилкобаламин участвует в образовании тетрагидрофолиевой кислоты, необходимой для синтеза тримединфосфата. Он включается в дезоксирибонуклеиновую кислоту (ДНК) предшественников эритроцитов - эритрокариоцитов. Любая из причин недостаточности тримединфосфата ведет к нарушению процессов эритропоэза. В кровь выбрасываются мегалобласты и мегалоциты как результат патологического, мегалобластического кроветворения. Значительная часть клеток (до 50 %) разрушается в красном костном мозге. У этих клеток укорочена продолжительность жизни, поэтому, несмотря на избыточное насыщение каждого эритроцита гемоглобином, их общее число снижено, развивается мегалобластическая гиперхромная анемия. Цветовой показатель становится больше 1 (1,4-1,8). В мазках крови наряду с признаками патологической регенерации (мегалоцитоз, мегалобластоз) обнаруживаются дегенеративно измененные эритроциты. Выявляется гиперхромия, пойкилоцитоз, макроцитоз, базофильная пунктация, появляются включения типа колец Кебота, телец Жолли. Снижено число ретикулоцитов, свидетельствующее о подавлении эритробластического кроветворения. Наблюдаются тромбоцитопения и лейкопения. Дефицит витаминов В12, В6 в организме и развивающаяся анемия у домашних животных часто возникают от алиментарной недостаточности. Особенно чувствительны к гиповитаминозу животные с однокамерным желудком. У жвачных микрофлора преджелудков синтезирует водорастворимые витамины, в их числе В12 и В6. Образование цианкобаламина может быть заторможено отсутствием в рационе достаточного количества кобальта, подавлением активности микрофлоры, нерациональным кормлением, чрезмерным применением антибиотиков. Так, недостаток кобальта в рационе коров приводит к гиперхромной анемии, характеризующейся падением числа эритроцитов с 5,7 ±0,07 до 4,7 ±0,04 Т/л, повышением среднего содержания гемоглобина в одном эритроците с 20,0 ± 0,4 до 24,1 ± 0,6 пг, снижением уровня кобаламина в крови. Усвоение витамина B12 становится затрудненным или невозможным из-за уменьшения либо полного прекращения выработки внутреннего антианемического фактора, что может быть обусловлено наследственным дефектом, аутоиммунной патологией, хроническими или острыми патологическими процессами в желудке (опухоли, воспаление, язвенные поражения). У телят с тяжелым течением гастроэнтероколита зарегистрированы уменьшение содержания гемоглобина в крови, возрастание цветового показателя и средней концентрации гемоглобина в одном эритроците, падение уровня железа со 170 до 98—108 мкг/100 мл крови. Причиной анемии может быть и некомпенсированная повышенная потребность в цианкобаламине у беременных животных при смене эмбрионального типа кроветворения у плода на эритробластический. Депонирование витамина В12 становится затрудненным при прогрессирующем, диффузном поражении печени (гепатит, гепатоз, цирроз). Развитию В12 -дефицитной анемии способствуют дисбактериоз и глистная инвазия, так как паразитирующие организмы вступают в конкурентные отношения с хозяином. Так, при неоаскаридозе у телят установлено снижение содержания гемоглобина и эритроцитов по сравнению с таковым у здоровых. |
