Пат физиология. Учебные пособия для студентов высших учебных заведений
 Скачать 7.09 Mb. Скачать 7.09 Mb.
|
|
14.3. НАРУШЕНИЯ КОЛИЧЕСТВЕННОГО И КАЧЕСТВЕННОГО СОСТАВОВ ЛЕЙКОЦИТОВ Кровь основных видов сельскохозяйственных животных — лошадей, свиней, крупного и мелкого рогатого скота содержит в среднем от 7 до 12 тыс/мкл (х 109/л; Г/л) лейкоцитов; у птиц эта величина колеблется в пределах 20—40 тыс/мкл, у рыб — 25— 50 тыс/мкл. Здоровые животные каждого вида сохраняют относительное постоянство этих показателей. Патологические реакции, состояния и болезни значительно изменяют количественную и качественную характеристики системы белой крови. Функциональное назначение отдельных элементов системы предопределяет их число, распределение в лейкограмме, биологические свойства, характерные для конкретных нозологических единиц. Вместе с тем существуют типовые формы патологии системы лейкоцитов. К ним прежде всего относят изменения общего числа клеток в единице объема периферической крови в сторону повышения — лейкоцитоз или понижения — лейкопения. Они могут быть первичного происхождения, обусловленные генетическими дефектами лейкопоэза, или вторичными как ответная реакция организма на различного рода повреждения. Ликвидация основного страдания влечет за собой нормализацию общего числа лейкоцитов, их процентного соотношения, функциональной активности. Лейкоцитоз (лейкоцит + греч. osis — ненормальное увеличение) — увеличение количества лейкоцитов в единице объема крови. По происхождению лейкоцитоз подразделяют на физиологический и патологический. Физиологический лейкоцитоз наблюдают после приема корма моногастричными животными — пищеварительный лейкоцитоз (у жвачных не отмечен); при интенсивной мышечной работе, особенно у беговых и скаковых лошадей, — миогенный лейкоцитоз; у плотоядных животных и молодняка большинства млекопитающих — в раннем постнатальном периоде развития (2—3 нед). Кровь поросят же первых недель жизни отличается сравнительно низким числом лейкоцитов. Патологический лейкоцитоз является следствием влияния на организм животных разнообразных факторов экзогенного и эндогенного происхождения. Он может быть вызван химическими соединениями (угарным газом, нитробензолом), некоторыми лекарственными средствами (камфора, фенацетин, соли ртути, эфирные масла, йодистый калий, сыворотки), физическим воздействием (длительным влиянием малых доз ионизирующей радиации). Главенствующими же причинами являются биологические. Лейкоцитоз сопровождает многие инвазионные, инфекционные, гнойно-воспалительные, асептические процессы у животных. Продукты жизнедеятельности микробов, паразитирующих организмов и их эндотоксины стимулируют лейкопоэз и усиленный выброс лейкоцитов в общий ток крови. Причинным фактором, получившим распространение среди животных разных видов, все больше становится опухолевая активация лейкопоэза при лейкозах крупного и мелкого рогатого скота, кур. Лейкоцитоз считают абсолютным, если он обязан усилению лейкопоэза за счет активации этиологическим фактором гуморальных стимуляторов — лейкопоэтинов, либо снижению уровня ингибиторов пролиферации клеток лейкопоэтических тканей. Он будет относительным, если стал результатом гипогидратации животных (анемия, гипертермия, водное голодание) или перераспределения лейкоцитов в русле крови при эмоциональных стрессах, шоке, коллапсе. Патологический лейкоцитоз не имеет самостоятельного диагностического значения, являясь вместе с тем важным патогномоничным признаком. Он, как правило, сопровождается преимущественным повышением числа отдельных форм лейкоцитов, изменениями в лейкограмме. Выделяют лейкоцитоз нейтрофильный (нейтрофилия), эозинофильный (эозинофилия), базофильный (базофилия), лимфоцитарный (лимфоцитоз) и моноцитарный (моноцитоз). Нейтрофилия (нейтрофилез) характеризуется увеличением числа зрелых сегментоядерных клеток, палочкоядерных и юных миелоцитов. Наиболее часто сопровождает острые инфекционные заболевания (мыт, инфекционный энцефаломиелит лошадей, ящур, рожа свиней) и гнойные воспаления (раны, абсцессы, флегмоны). Нейтрофилия со значительным сдвигом ядра влево, вплоть до появления миелоцитов, свидетельствует о тяжелой септической инфекции. Отсюда качество нейтрофильного сдвига может служить критерием тяжести заболевания и иметь прогностическое значение. О той или иной форме сдвига судят по виду нейтрофильных клеток. Регенеративный сдвиг характерен появлением в мазках крови повышенного числа палочкоядерных и юных нейтрофилов. Дегенеративный сдвиг проявляется появлением миелоцитов, т. е. резким перемещением ядра влево, и наличием дегенеративных изменений структуры клеток. Помимо ядерного сдвига влево возможен ядерный сдвиг вправо, о чем судят по преобладанию среди нейтрофильных лейкоцитов палочкоядерных и зрелых форм клеток с 5—6 сегментами. Сдвиг ядра нейтрофилов вправо свидетельствует о благоприятном течении заболевания. Эозинофилия (эозинофильный лейкоцитоз) у сельскохозяйственных животных встречается, как правило, при глистных инвазиях, обусловленных взрослыми паразитами или их личиночными формами. Фасциолез, трихомоноз, аскаридоз, стронгилоидоз, диктиокаулез сопровождаются резко выраженной формой эозинофилии. Повышение числа эозинофилов констатируют при различных аллергических состояниях (поллинозе, крапивнице, клеверной болезни), при применении антибиотиков (пенициллинотерапия, стрептомицинотерапия). С выраженной эозинофилией протекают некоторые кожные заболевания животных (экзема, грибные дерматиты). Рожа свиней характерна тем, что содержание эозинофилов в лейкограмме с исходных 1—4 % повышается до 45 %. Базофилию (базофильный лейкоцитоз) — увеличение содержания базофилов в крови — наблюдают у животных при аллергических состояниях, вызванных инъекцией чужеродного белка, при чуме и роже свиней, хроническом и остром миелозе. Из-за малого количества клеток (0,5—1,0 %) и трудности учета диагностического и прогностического значения базофилия не имеет. Лимфоцитоз — повышение уровня лимфоцитов в крови — может быть абсолютным или относительным. Относительным лимфоцитоз называют тогда, когда количество этих клеток в единице объема крови (мкл) не отличается от нормального, а возрастание их числа в лейкограмме происходит за счет снижения других элементов белой крови. Абсолютный лимфоцитоз присущ хроническим инфекциям, таким, как туберкулез, бруцеллез, инфекционная анемия лошадей, и инвазионным заболеваниям (пироплазмоз, бабезиеллез, нуталлиоз). Появление обильного количества лимфоцитов (до 100 тыс/мкл) и их подавляющее большинство в лейкограмме (80—100 %) служат указанием на неблагоприятный прогноз. Моноцитоз — увеличение числа моноцитов крови — один из показателей активизации иммунного процесса при вакцинопрофилактике болезней животных. Характерен для многих вирусных, бактериальных и протозойных заболеваний. Прогностическое позитивное значение имеет абсолютный моноцитоз, когда повышается число клеток этого рода в единице объема крови. Моноциты, циркулирующие в крови и фиксированные в тканях, выступают в роли макрофагов, презентуя антигены Т-клеткам, инициируя иммунный ответ. Лейкопения характерна уменьшением общего количества лейкоцитов в крови (ниже 4—8 тыс/мкл) соответственно видовым особенностям животных. Лейкопения может сочетаться с равностепенным уменьшением всех составляющих лейкограмму клеток или с преимущественным уменьшением отдельных ее форм. Она связана с нарушением функции гемопоэза, элиминацией лейкоцитов, их распределением. Рассматривают лейкопению органического происхождения как результат гипо- или аплазии гранулоцитарного ростка костного мозга и функциональную. Органическая лейкопения возникает в результате новообразований, действия ионизирующей радиации, иммунных антител, тропных ядов (соединения ртути) на костный мозг. Функциональная лейкопения появляется в тех случаях, когда клеточный состав костного мозга полноценен, но функционально угнетен. Лейкопения может служить показателем подавления кроветворения, быть одним из критериев пониженной реактивности, иммунной сопротивляемости организма. Лейкопению регистрируют при алиментарном истощении, большинстве вирусных инфекций (инфекционная анемия и инфлюэнца лошадей, чума крупного рогатого скота, чума свиней). Ряд лекарственных препаратов прямо или опосредованно действует на кровь и кроветворные органы (новарсенол, сульфаниламиды). Одной из причин лейкопении является аллергия, когда антиген с антителом формируют цитотоксический для лейкоцитов комплекс. Относительное снижение элементов белой крови возможно за счет перераспределения в сосудистом русле. Меняется соотношение между циркулирующим и пристеночным пулом лейкоцитов, что наблюдают, например, при анафилактическом шоке, воспалительных процессах, в первой стадии лихорадочной реакции. Лейкопении с преимущественным снижением отдельных форм лейкоцитов подразделяют на:
Показатели лейкограмм, по которым судят о преимущественном нарастании или снижении отдельных форм лейкоцитов, не могут быть статичными, неизмененными. Множество факторов экзогенного и эндогенного происхождения способны существенно изменить картину белой крови. Так, при паренхиматозных маститах у коров изначальная лейкопения спустя 1—2 дня сменяется лейкоцитозом. В первую стадию лихорадки, индуцированной бактериальными пирогенами, у лошадей, коров, овец, свиней наблюдалась лейкопения с преимущественной нейтропенией и эозинопенией. Последующее развитие лихорадочной реакции сопровождалось значительным лейкоцитозом, нейтрофилией, лимфоцитозом, эозинофилией. 14.4. ГЕМОБЛАСТОЗЫ Гемобластозы (от греч. haima — кровь, blastos — зародыш, osis — болезнь) — группа заболеваний кроветворной ткани, относящихся к злокачественным новообразованиям. Гемобластозы сельскохозяйственных животных распространены повсеместно, особенно в странах с высокоразвитым животноводством. Подвержены этим заболеваниям животные всех видов: крупный и мелкий рогатый скот, лошади, свиньи, куры, кошки, собаки, кролики, крысы, мыши и др. Особая опасность гемобластозов складывается из экономического ущерба, наносимого неизлечимостью болезней этой группы, охватом большого контингента животных и того, что преимущественно поражаются такие продуктивные животные, как коровы и куры — источники наиболее ценных продуктов питания (мясо, молоко, яйца). Вероятность попадания продуктов питания от больных животных человеку велика, ибо ге-мобластозам, как и другим новообразованиям, свойствен длительный период скрытого развития. 14.4.1. ОБЩАЯ ЭТИОЛОГИЯ Гемобластозы относятся к заболеваниям животных опухолевой природы, поэтому причиной их возникновения являются канцерогенные агенты физического, химического и биологического происхождения. Физические факторы. Лейкоз и гематосаркомы возникают в результате воздействия на организм животных и энизирующих излучений. Болезнетворный эффект может проявляться после многократного облучения малыми дозами или в результате одно- или двукратного массированного воздействия. Последствия в виде бластоматозного роста кроветворной ткани могут быть результатом внешнего облучения (космические лучи, рентгеновское излучение) или попадания радиоактивных изотопов (40К, 90Sr, 89Sr, 137Cs, 14C) в избыточных количествах внутрь организма. Подтверждением роли ионизирующего излучения как опасного лейкозогенного фактора служат статистические данные по заболеваемости лейкозом лиц, перенесших атомную бомбардировку японских городов Хиросимы и Нагасаки. В этих городах число заболевших лейкозом было в 11—18 раз больше, чем в других городах Японии. Химические факторы. Лейкемогенными, как и канцерогенными свойствами обладают различные химические соединения — ароматические углеводороды, бензолы, азотистые и поливиниловые соединения, анилиновые красители, синтетические гормоны, перекиси жиров, образующиеся при их перегревании или длительном хранении. Доказательствами лейкозогенного действия указанных веществ служат клинические наблюдения и экспериментальные данные. Типичный лейкоз у кур и мышей развивается при введении им чистого канцерогенного вещества — 1, 2, 5, 6-ди-бензантрацена. Аналогичные данные получены при введении животным 9,10-диметил-1,2-бензантрацена. Спустя 4—4,5 мес у подопытных развивался лейкоз. Смазывание кожи мышей высоко-лейкозных линий 0,5%-ным бензольным раствором диметилбензантрацена приводило к развитию лимфолейкоза у 85 % подопытных животных в среднем через 108 дней. Еще результативнее применение в аналогичных опытах метилхолантрена— лейкоз развивался у 99 % мышей всего через 88 дней. Обнаружены и эндогенные бластомогенные вещества. К наиболее типичным из них относят метилхолантрен, образуемый в организме из холевой и дезоксихолевой кислот. Биологические факторы. Особую значимость в заболевании животных гемобластозами придают вирусам. Еще в 1909 г. Эллерман и Банг осуществили перезаражение эритро- и миелолейкозом здоровых кур от больных как с помощью клеточных субстратов, так и бесклеточных фильтратов. В 50-х годах Л. Гросс успешно провел эксперименты по индукции новорожденным и взрослым мышам лейкоза путем инъекций бесклеточного фильтрата лейкозной ткани от больных мышей высоколейкозной линии. С положительным результатом проведены опыты по перепрививке лейкоза мышей крысам и хомячкам. Получены многочисленные данные о вирусной этиологии гемобластозов у млекопитающих разных видов (крупный рогатый скот, овцы, собаки, кошки, крысы, мыши) и птиц (куры, индейки, гуси, утки). Выделенные от больных лейкозом кошек, морских свинок, мышей, хомяков, обезьян, свиней, норок вирусы оказались РНК-содержащими и отнесены к семейству ретровирусов, подсемейству онковирусов типа С-1. В 60-х годах при изучении материала от больного лейкозом крупного рогатого скота были выделены возбудители этого заболевания — вирусы лейкоза крупного рогатого скота (ВЛКРС). Этот вирус также оказался РНК-содержащим, был отнесен к семейству ретровирусов, подсемейству онковирусов типа С-2. Описана морфология ВЛКРС. Его вирионы в зрелом виде состоят из электронноплотного, нейтрально расположенного нуклеотида диаметром от 73 до 120нм. Внешняя оболочка вируса имеет двуконтурную лабильную мембрану, отчего диаметр вириона может варьировать от 73 до 120 нм. Контактируя с соответствующими рецепторами мембран клеток гемопоэза, лейкозогенный вирус попадает внутрь. Затем с помощью ревертазы (обратной транскриптазы) на геномной РНК синтезируется ДНК вируса, интегрирующая в ДНК клетки. В последующем в клетке образуются различные виды вирусных РНК и белков, определяющих лейкозный процесс. ВЛКРС в экспериментальных условиях удается вызвать лейкоз у овец и коз. Один из способов заражения овец — манипуляция одной и той же инъекционной иглой, контаминированной кровью от больной лейкозом коровы. Продолжительность латентного периода от двух месяцев до одного года, после чего у подопытных животных развивались характерные признаки лимфолейкоза. Диагноз подтверждался серологическими, патологоанатомическими и гистологическими исследованиями. Очевидна правомерность вывода о том, что нарушение правил асептики и антисептики во время ветеринарно-зоотехнических обработок крупного и мелкого рогатого скота может быть одним из путей распространения лейкоза. 14.4.2. ОБЩИЙ ПАТОГЕНЕЗ Принято считать, что в механизме развития гемобластозов невозможно учитывать только внешний, в том числе вирусный, фактор. Особое значение имеют состояние самого организма, наличие наследственно-генетического фактора. Так, выявлены определенные особенности в распространении онкорновирусной инфекции и лейкоза среди крупного рогатого скота разных пород. ВЛКРС-инфекция широко распространена, например, среди животных красной степной, черно-пестрой, красной эстонской, бурой латвийской пород. Отмечают генетическую связь пород, менее устойчивых к лейкозу, с англерским (красным немецким) и остфризским скотом. Анализ заболеваемости показал, что кроме породной принадлежности в возникновении и развитии гемобластозов имеют значение продуктивность, особенно кур-несушек, корма и кормление, характер почвы, климат, пастбища и другие факторы. Таким образом, было установлено, что онкорновирусная инфекция является обязательным, но не единственным условием возникновения и развития лейкозного процесса. Реализация влияния бластомогенных факторов на организм возможна в условиях снижения противоопухолевой резистентности организма, ингибирования активности антимутационных механизмов, складывающихся из блокады активирующихся онкогенов, их обнаружения и элиминации ферментными системами. Превратить нормальные клетки гемопоэза в бластные способны мутации онкогенов, когда их продукт (онкобелок) появляется в избыточном количестве или приобретает измененную структуру. Неэффективный иммунный контроль позволяет мутантным клеткам с измененной генетической программой формировать опухолевый атипизм. Имеются многочисленные доказательства того, что опухолевой трансформации подвергается одна гемопоэтическая клетка, дающая начало клону гемобластных клеток. Изменение генетической программы клетки по одному или нескольким свойствам наследуется дочерними клетками. Нарастающая опухолевая прогрессия создает неравнозначные условия для всех дочерних клеток. Часть из них лучше приспосабливается к меняющимся условиям, они интенсивнее размножаются, передавая новые свойства своим потомкам. Лейкозы и гематосаркомы превращаются из моноклоновых в поликлоновые, причем преобладают менее дифференцированные и более злокачественные клеточные элементы. В процессе опухолевой прогрессии формируется атипизм гемобластозов. Появляются существенные отличия в обменных процессах, энергетике, росте, структуре и функции бластоматозных клеток от нормально функционирующих. Трансформированный костный мозг начинает интенсивно продуцировать лейкозные клетки разной степени зрелости. По мере усиления пролиферативных процессов, нарастания массы опухолевой ткани в кровь начинает выбрасываться все большее количество лейкоцитов, их бластных, незрелых форм. Повышается содержание молодых форм гранулоцитарных клеток — базофилов, эозинофилов и особенно нейтрофилов, лимфобластов, пролимфоцитов. Функциональная активность этих клеток извращена или полностью выпадает со всеми вытекающими отсюда последствиями. 14.5. ЛЕЙКОЗ Лейкоз (от греч. leukos — белый, osis — болезнь) — системное заболевание органов кроветворения бластоматозного происхождения. Характеризуется прогрессивной клеточной гиперплазией кроветворной и лимфоидной тканей, метапластическим разрастанием патологически измененных элементов в паренхиматозных органах. Лейкозом болеют почти все домашние животные, в том числе птицы. Впервые заболевание было описано в 1845 г. известным немецким патологом Р. Вирховым и названо лейкемией (белокровием). Вскоре эта болезнь выявлена у лошадей (Лейзеринг, 1858), коров, свиней, собак, кошек (Седам, Гродский, 1879), овец и коз (Авероус, 1896), у кур (Капарини, 1896). Термин «лейкемия» с 20-х годов был заменен термином «лейкоз», поскольку не всегда бластоматозный, гиперпластический процесс сопровождается лейкемией, могут быть лейкопенические и алейкемические формы заболевания. Лейкоз выявлен у 29 видов доместицированных и диких животных, в том числе у птиц, рыб. Наиболее часто лейкозом поражены крупный рогатый скот, овцы и куры. В связи с преимущественной локализацией лейкозного процесса у крупного рогатого скота выделяют лейкозы лимфоидный (рис. 20), миелоидный (рис. 21), недифференцируемый, а также злокачественный гистиоцитоз. 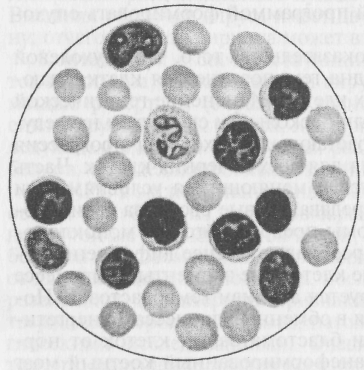 Рис. 20. Лимфоидный лейкоз. Насыщение крови лимфоцитами 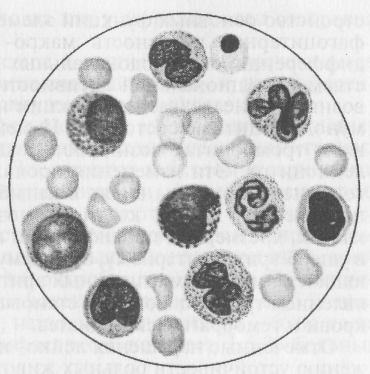 Рис. 21. Миелоидный лейкоз. Насыщение крови гранулоцитами в разных стадиях созревания В зависимости от общего количества лейкоцитов в единице объема крови принято различать следующие разновидности лейкоза:
Выделяют пять стадий (периодов) течения лейкозного процесса у крупного рогатого скота:
Одной их характерных черт лейкозного процесса, определяющего в определенной степени его течение и исход, является расстройство основных функций элементов белой крови. Снижается фагоцитарная активности макро- и микрофагов. Нарушение дифференцировки родоначальных клеток приводит к расстройствам функциональной активности Т- и В-систем иммунитета, возникают неадекватные реакции на антигены, развиваются им-мунодефицитные состояния. Изменения в системе красной крови и тромбоцитах возникают позднее наблюдаемых в системе лейкоцитов. Эти изменения проявляются анемией и тромбоцитопенией. Причины видят в ингибиции пролиферации эритропоэтических клеток костного мозга метаболитами лейкозных клеток, чрезмерной пролиферации клеток лейкоцитарного ростка в ущерб эритроцитарному, аутоиммунных процессах, сопровождающихся цитолизом атипичных эритроцитов и тромбоцитов. Проявлением тромбоцитопении становятся снижение свертываемости крови и геморрагический диатез. Отмеченные нарушений лейко- и эритропоэза приводят к снижению устойчивости больных животных к патогенной и условно-патогенной микрофлоре с септическими осложнениями, что в конечном итоге приводит к терминальной стадии лейкоза. Лейкоз овец. Наиболее часто отмечают лимфоидную форму лейкоза у спонтанно заболевших животных. Эта хроническая инфекционная болезнь чаще появляется у овец 5—6-летнего возраста, без специфических клинических проявлений. Характерно наличие алейкемической и сублейкемической стадий заболевания. Лейкограмма больных овец характеризуется нейтропенией и лимфоцитозом, когда количество лимфоцитов достигает 70—80%, тогда как у здоровых оно составляет в среднем 45 %. В крови появляются бластные формы, клетки лимфоидного ряда большого диаметра, пролимфоциты. Появление в крови лимфоцитов диаметром 13—16 мкм, чего не наблюдают у здоровых животных, — неблагоприятный признак исхода болезни. У больных спонтанный лейкозом выявлено снижение количества эритроцитов в крови с 7,6 до 6,2 Г/л и гемоглобина со 121 до 87 Г/л. Качественные изменения элементов красной крови проявляются анизоцитозом, пойкилоцитозом, олигохромемией, наличием других патологических форм эритроцитов. В красном костном мозге обнаруживаются очаги лимфоидно-клеточной пролиферации с вытеснением миелоидной ткани и уменьшением в лейкограммах клеток эритроидного ряда. Гистологически лимфоузлы брюшной полости представляют собой однородную массу пролиферата липидных клеток, часть из которых находится в состоянии митоза. Лимфоидные пролифераты инфильтрируют окружающую лимфоузел соединительную ткань. Узелковые скопления клеток лимфоидного типа обнаруживают в почках. Диффузный лимфоидно-клеточный пролиферат поражает сердце, что приводит к дистрофии и атрофии его мышечных элементов. Масса сычуга за счет разрастания лимфоидной ткани достигает 4 кг, тогда как у здоровых овец она равна 320-380 г. Кроме лимфолейкоза описаны и другие редко встречающиеся формы гемобластозов овец: миелоидный, слабо- и недифференцированный лейкоз, лимфогранулематоз, лимфосаркома. Лейкоз птиц. Группа инфекционных заболеваний, вызываемых РНК-содержащими онкорнавирусами шести антигенных подгрупп — А, В, С, D, Е, F. Поражаются лейкозом и саркомами домашние и дикие птицы: куры, индейки, фазаны, гуси, утки, чайки, лебеди и др. Наиболее часто болеют куры. Описана генетическая предрасположенность к лейкозу кур, как и относительная устойчивость отдельных пород. Выделяют лимфоидный, миелоидный, эритробластический (эритробластоз) лейкоз. По литературным данным, на долю лимфолейкоза приходится 88,5 % павшей от гемобластозов птицы, на долю миелолейкоза — 6, на долю эритробластоза — 4 и от лимфосарком погибает 1,5% больных птиц. Лимфоидный лейкоз, наиболее часто встречающийся у кур, протекает преимущественно алейкемически, но в некоторых случаях число лейкоцитов может достигать 60—70 Г/л с возрастанием числа псевдоэозинофилов и лимфоцитов разной степени зрелости. В патологический процесс вовлекаются внутренние органы, в которых возникают диффузные или очаговые разросты лимфоидной ткани. В 80—85 % случаев поражается печень, в 70 — почки, в 60—65 — селезенка, в 40—45 — яичники, в 25—30 % — желудочно-кишечный тракт, другие органы. Красный костный мозг при лимфолейкозе чаще остается интактным, изменения в нем непостоянны, возможно усиление гранулопоэза. Выявляется анемическое состояние, эритропения сочетается с низким уровнем гемоглобина. Клинически болезнь проявляется сонливостью, вялостью птицы, бледностью гребешка и сережек. Болезнь протекает хронически. Миелолейкоз — сравнительно редкое заболевание птиц. Характерен преимущественной инфильтрацией внутренних органов клетками миелоидного ряда. Миелобласты, миелоциты, псевдоэозинофилы образуются в избыточном количестве в почках, селезенке и в резко увеличенной (до 450 г) печени. Костный мозг может оставаться интактным, или в нем наблюдают миелоидные превращения. Протекает в алейкемической или лейкемической форме. Лейкемия характеризуется гранулоцитозом — базофилией, эозинофилией и псевдоэозинофилией, достигающей 60 % (при норме 27 %). Общее число лейкоцитов может достигать 120— 150 Г/л при выраженной лимфопении. Эритробластоз кур — остро протекающее инфекционное заболевание, в котором выделяют несколько периодов:
Основным, ведущим звеном патогенеза эритробластоза является поражение костного мозга. Клетки эритроидного ряда теряют способность накапливать гемоглобин, развивается дизэритропоэтическая анемия. Путем экспериментального заражения цыплят было выявлено, что к концу заболевания число эритроцитов снижается до 1,014 Т/л, т. е. более чем в 2 раза (норма 2,45 Т/л). Эритропения сочетается с падением количества гемоглобина (65 г/л вместо 104 г/л), появлением в крови проэритробластов, эритробластов, аномальных эритронормоцитов. Развитие анемии у больной эритробластозом птицы объясняют недостаточным количеством эритропоэтина, приводящего к задержке дифференцировки и выбрасывания эритроцитов в сосуды, неэффективностью эритропоэза, когда клон атипичных клеток подвергается гемолизу и фагоцитозу. В крови больных птиц выявляется тромбоцитопения. Число тромбоцитов падает до 1,5 Г/л вместо 75 Г/л по средней норме. Скорость свертывания крови замедляется до 8,5 мин, тогда как у здоровых она равна 3,5 мин. Развивается острый геморрагический синдром с кровоизлияниями во многих тканях и органах. Нарушена не только тромбо- и эритропоэтическая, но и лейкопоэтическая функция костного мозга. Свидетельство тому — наблюдаемые у больных кур гранулоцитопения, снижение или полное исчезновение в крови лимфо- и моноцитов. В миелограмме зараженных вирусом кур уже на 3-й день находят снижение числа базофильных и эозинофильных миелоцитов, а в последующем они вовсе исчезают. Выявляются лимфоцито- и моноцитопения. 14.6. НАРУШЕНИЯ СИСТЕМЫ ГЕМОСТАЗА Гемостаз (от греч. haima — кровь, stasis — остановка) — понятие, включающее в себя остановку кровотечения путем свертывания белков крови, адгезии и агрегации ее клеточных элементов, образование тромба. Это сложный саморегулирующийся физиологический механизм, в который входят множество компонентов свертывающей, противосвертывающей систем, системы фибронолиза и состояние стенки сосудов. В естественных условиях у здорового организма пограничная с эндотелием выстилающая фибриновая пленка уплотняет капиллярную стенку, снижает ее проницаемость, обеспечивает гемодинамику. Ферментные системы определяют равновесие между образованием пленки фибрина на поверхности эндотелия и ее растворением. Система гемостаза обеспечивает коагуляцию белка, образование сгустка фибрина и в условиях патологии — при повреждении сосудов, воспалениях различной этиологии, заживлении ран. Она сформировалась в процессе эволюции как важнейший защитный механизм, способствующий выживанию. Расстройства системы гемостаза получили название коагулопатий. К ним относят повышение и понижение свертываемости крови. Повышение свертываемости крови — гиперкоагуляция— возникает как следствие активации свертывающей системы крови или снижения функции антисвертывающего механизма. Усиленное поступление в кровь прокоагулятов вызывается повреждениями стенок сосудов при механической травме, ожогах, воспалительных процессах разной этиологии, массивном гемолизе, сепсисе, шоке. Повреждение стенки сосуда инифициирует каскад ферментативных реакций, определяемых факторами свертывания крови. Они содержатся в плазме крови, тромбоцитах, эритроцитах, лимфоцитах. Освобождаемая поврежденными тканевыми клеточными элементами и тромбоцитами тромбокиназа (тромбопластин FIII) в присутствии кальция (FIV) и АК-глобулина (FV) превращает протромбин (FII) в протеолитический фермент тромбин, который, в свою очередь, переводит растворенный в крови фибриноген (FI) в нерастворимый белок — фибрин, образующий рыхлый сгусток. Он подвергается ретракции, сжимается и уплотняется. В последующем под влиянием фибриногена фибрин расщепляется и рассасывается. Фибронолиз усиливается гепарином, ингибируется антиплазминами, бета- и липопротеидами. Повышенная свертываемость крови возможна и за счет низкой активности антикоагулянтов и фибринолитических механизмов. Развивающийся тромботический синдром является следствием снижения уровня основного антикоагулянта — свободного гепарина крови. Угнетение фибринолиза как причина гиперкоагуляции возможно при частом эмоциональном стрессе, токсикозах, росте новообразований. Тромбоз сосудов как следствие гиперкоагуляции может быть локальным, предотвращающим потерю крови при их ранении, сопровождать воспалительные процессы и быть генерализованным. Прижизненное внутрисосудистое свертывание крови возможно как следствие шока разного генеза, опухолевой болезни, массивного гемолиза, сепсиса, атеросклеротических изменений стенок сосудов, их травмирования личиночными формами гельминтов. Тромбообразование в сосудах чревато тяжелыми для организма, животных последствиями, которые зависят от скорости образования тромба, возможности развития коллатералей, диаметра и типа тромбированных сосудов (вены, артерии, сосуды микроциркуляторного русла), важности для жизнедеятельности организма органа, сосуды которого тромбированы. Быстрая активация системы свертывания крови сопровождается образованием рыхлых тромбических масс, частицы которых способны легко отрываться и вызывать тромбоэмболию. Так, тромбоэмболические колики со смертельным исходом возникают у лошадей как следствие поражения интимы брыжеечных артерий личинками гельминтов. Снижение свертываемости крови — гипокоагуляция, сопровождающаяся геморрагическим синдромом, у больных животных проявляется спонтанно и выражается повышенной кровоточивостью или обильной кровопотерей при незначительной травме сосудов. В ветеринарной медицине встречается гораздо чаще, чем тромбоз. Геморрагический диатез сопровождает многие различные по этиологии и патогенезу заболевания животных, отличительным признаком которых является временная или постоянная, врожденная или приобретенная склонность организма к кровотечениям. Они могут возникать самопроизвольно или под влиянием незначительных повреждений сосудистой стенки. Кровоточивость может быть основным симптомом болезни (гемофилия) или как сопутствующее явление наблюдаться при заболеваниях печени, почек, системы крови, инфекционных болезнях, химических интоксикациях, лучевых поражениях, авитаминозах, аллергических состояниях. Развитие геморрагического диатеза определяется двумя факторами — изменением состояния сосудистых стенок и самой крови. Изменение стенки сосудов приводит к повышенной проницаемости капилляров и их более легкой ранимости. Этиологическими факторами, приводящими к сосудистым изменениям, являются:
Изменения свойств самой крови, приводящие к геморрагическим диатезам, сводятся к нарушениям отдельных фаз гемостатического процесса. К наиболее значимым расстройствам гемостаза, связанным с состоянием самой крови, следует отнести тромбоци-топению, К-гиповитаминозный диатез, гемофилию. В кровотоке тромбоциты занимают краевое положение, прилегая к эндотелию сосудов. Они «заклинивают» межклеточные щели, образуют своеобразную подстилку, обеспечивающую естественную проницаемость капилляров для жидкостей и газов и непроницаемость по отношению к форменным элементам крови. Отсутствие или недостаток кровяных пластинок приводит к «оголению» эндотелия и спонтанному диапедезу тромбоцитов через мембрану капилляров. Роль тромбоцитов в гемостазе определяется их способностью к адгезии (прилипанию), агрегации (скапливанию) и агглютинации (патологическому склеиванию в присутствии антител). Начальная реакция тромбоцитов на повреждение сосудистой стенки — распад АТФ с образованием аденозиндифосфорной кислоты, что приводит к адгезии кровяных пластинок к поврежденному эндотелию и их агрегации. Образуется провизорный тромб из пластинок, предотвращающий развитие более обширного кровоизлияния. Он становится опорным центром для последующего выпадения фибрина. Ретракция, уплотнение кровяного сгустка — также следствие активности кровяных пластинок. Снижение числа тромбоцитов в результате нарушения функции источника их образования — мегакариоцитов или усиленного распада лишает стенку сосуда защиты в виде цементирующего слоя из кровяных пластинок, делает затрудненным или невозможным реализацию тромбического процесса. Возникают условия для развития геморрагии. Тромбоцитопению наблюдают у крупного рогатого скота, лошадей, свиней и собак. Больные животные теряют аппетит, а кожа — эластичность. На ее непигментированных участках обнаруживают множественные точечные и пятнистые кровоизлияния. Слизистые оболочки бледные, с кровоизлияниями, особо выраженными на деснах. В фекалиях и рвотных массах собак выявляют примесь крови. Хроническая потеря крови, связанная с тромбоцитопенией, приводит к постгеморрагической анемии, падению числа эритроцитов до 1— 3 Т/л и появлению патологических форм элементов красной крови. Количество тромбоцитов уменьшено до 11—17 Г/л. Их снижение до 5 Г/л может привести к смертельной кровопотере. У поросят наиболее часто встречается изоиммунная тромбоци-топатическая пурпура — заболевание, возникающее в первые две недели после рождения. Противотромбоцитарные антитела поступают приплоду с молозивом. Весь помет от свиноматок поражается в тех случаях, когда хряк был гомозиготен в отношении специального антигена тромбоцитов. При осмотре больных поросят в разных местах, но главным образом на животе, ушах, конечностях обнаруживают петехии и экхимозы. 14.7. ГЕМОФИЛИЯ Гемофилия (от греч. haima — кровь, philia — склонность) — наследственная болезнь, проявляющаяся склонностью к трудно останавливаемым кровотечениям из-за сниженной способности крови к свертыванию. Полагают, что одной из основных причин гемофилии у сельскохозяйственных животных является близкородственное разведение. Наследование этого заболевания происходит по рецессивному признаку, сцепленному с полом. Рассматривают гемофилию: А и В мужских особей и С и D у животных обоих полов. Гемофилия А объясняется недостатком, антигемофильного глобулина (FVIII), гемофилия В — недостатком фактора Кристмана (FIX), гемофилия С — недостатком плазменного предшественника тромбопластина (FXI) и гемофилия D — недостатком фактора Хагемана (FXII). Суть патогенеза гемофилии в том, что нарушена первая фаза свертывания крови — отсутствует активный плазменный тромбопластин, поэтому невозможен переход протромбина в тромбин, а затем фибриногена в фибрин. Хорошо изучена гемофилия человека, обусловленная генетической недостаточностью антигемофильного фактора (FVIII) или плазменного компонента тромбопластина (FIX). Возникающее у больных кровотечение может продолжаться длительное время, а при незначительных травмах приводить к смертельному исходу. Болезнь проявляется в большинстве случаев у мужчин и обусловлена рецессивным, сцепленным с полом геном, передается сыновьям от матерей. Так, некоторые потомки английской королевы Виктории страдали наследуемой гемофилией, в их числе был и сын русского царя Николая II Алексей. Среди домашних животных гемофилию регистрируют редко. Описаны отдельные случаи возникновения заболевания у лошадей, собак, крупного рогатого скота. Основной особенностью у больных является резкое замедление времени свертывания крови. Так, если у здоровых лошадей оно длится 10—20 мин, у крупного рогатого скота —8—10, у собак- до 25 мин, то у гемофиликов кровь может не свертываться даже спустя несколько часов. У больных животных спонтанно возникает носовое, легочное, кишечное кровотечения. Одновременно наблюдают вне- запные обширные подкожные и внутримышечные кровоизлияния с образованием гематом, гемаартрозов, развитие параличей. Незначительные ранения способны вызвать тотальное кровотечение. При исследовании приплода от коровы с типичным проявлением гемофилии у всех телят обнаружили снижение уровня плазменного ускорителя (акселератора) превращения протромбина (FV), тромбина (FII) и фибриногена (FI). В английском чистокровном коневодстве со времен его основания (XVI в.) регистрируют носовое кровотечение как свойственное породе заболевание, наследуемое по простому рецессивному признаку. Потомки интенсивно используемых производителей унаследовали предрасположенность к носовым кровотечениям, и за последние 100 лет болезнь среди лошадей распространилась в Америке, во Франции, в Германии, Ирландии. Она стала опасной для полукровного и высококровного конезаводства. У подверженных заболеванию лошадей кровотечения возникают совершенно спонтанно, но могут появиться и после больших физических напряжений. Они проявляются по-разному: от маленьких сгустков в полостях носа до профузного кровотечения. В последнем случае кровь при вдохе способна попасть в легкие, вызвать асфиксию и смерть. Гемофилия, описанная у свиней, характеризуется сниженным содержанием антигемофильного фактора плазмы, удлиненным временем свертывания крови. Она наследуется как простой аутосомный рецессивный признак, чем отличается от классической гемофилии А человека и гемофилии собак. |
