2 мартынов терапия 01. Учебник для вузов москва гэотарм вд уд к6 16. 1. 4 (075. 8) Ббк 54. 1 я73 В56 Рецензенты
 Скачать 6.88 Mb. Скачать 6.88 Mb.
|
|
Глава 64 базофильный, полихроматофильный, оксифильный эритробласт (нормобласт), ретикулоцит, эритроцит. Гранулоцитопоэз В ходе дифференцировки предшественников гранулоцитов выделяют: мие-лобласт, промиелоцит, миелоцит, метамиелоцит, палочкоядерный и сегмен-тоядерный гранулоцит. По мере дифференцировки уменьшаются размеры клетки, появляются гранулы в цитоплазме, уплотняется ядро и изменяется его форма (от округлой к сегментированной). Моноцитопоэз Моноциты и гранулоциты имеют общую клетку-предшественницу — коло-ниеобразующую единицу гранулоцитов и моноцитов (CFU-GM), образующуюся из полипотентной клетки-предшественницы миелопоэза (CFU-GEMM). В развитии моноцитов выделяют две стадии — монобласт и промоноцит. Тромбоцитопоэз Из мегакариобластов развиваются самые крупные (30-100 мкм) клетки костного мозга — мегакариоциты. При дифференцировке мегакариоцит увеличивается в размерах, его ядро становится дольчатым. Образуется развитая система демаркационных мембран, по которым происходит отделение («отшнуровка») тромбоцитов. Лимфопоэз Из стволовой кроветворной клетки (CFU-blast) происходит полипотентная клетка-предшественница лимфопоэза (CFU-Ly), которая впоследствии даёт начало клеткам-предшественницам В-лимфопоэза, Т-лимфопоэза и (частично) предшественницам естественных киллеров (NK-клетки). Дальнейшая диффе-ренцировка включает в себя уровни про-В(Т)-клеток, пре-В(Т)-клеток, незрелых В(Т)-клеток, зрелых наивных В(Т)-клеток и (после контакта с Аг) — зрелых В(Т)-клеток окончательных стадий дифференцировки. ФАКТОРЫ ГЕМОПОЭЗА Образование клеточных элементов крови активируется и регулируется факторами гемопоэза: гемопоэтическими факторами роста, факторами транскрипции, фолиевой кислотой и витамином В12. Гемопоэтические факторы роста — фактор стволовых клеток (SCF), колоние-стимулирующие факторы (CSF), интерлейкины, эритропоэтин, тромбопоэтин. Факторы транскрипции — белки, связывающиеся с ДНК и регулирующие экспрессию генов кроветворных клеток. Фолиевая кислота и витамин В12 необходимы для синтеза ДНК. Фолаты и витамин В12 поступают с пищей и всасываются в тонкой кишке. Для всасывания витамина Bi2 в кишечнике необходим внутренний фактор Касла, синтезируемый париетальными клетками желудка. Фактор связывает витамин Bi2 и защищает его от разрушения ферментами. Комплекс внутреннего фактора с витамином В12 в присутствии ионов кальция взаимодействует с рецепторами эпителиальной клетки дистального отдела подвздошной кишки. При этом витамин В12 поступает в клетку, а внутренний фактор высвобождается. Отсутствие внутреннего фактора Касла приводит к развитию анемии. Гемопоэз ОРГАНЫ КРОВЕТВОРЕНИЯ И КРОВЕРАЗРУШЕНИЯ К кроветворным органам относят костный мозг (основной орган постна-тального гемопоэза), тимус, лимфатические узлы, селезёнку, пейерову бляшку кишечника. Разрушение клеток крови происходит в основном в селезёнке. Костный мозг — основной кроветворный орган постнатального гемопоэза. Различают жировой костный мозг, деятельный костный мозг и строму. Жёлтый костный мозг (назван так из-за большого скопления жировых клеток) — неактивная часть, начинающая действовать при необходимости для усилении гемопоэза (например, при хронической гипоксии или тяжёлых кровотечениях). В красном костном мозге преобладают созревающие эритроциты, что придаёт костномозговым очагам гемопоэза красный цвет. Строма костного мозга состоит из эндотелиальных, адвентициальных и ретикулярных клеток (фибробла-сты костного мозга), макрофагов, жировых клеток, остеокластов, остеобластов, остеоцитов и внеклеточного матрикса. Вилочковая железа (тимус) — центральный орган лимфопоэза. Здесь происходит антигеннезависимая дифференцировка Т-лимфоцитов. Предшественники Т-клеток попадают в корковое вещество тимуса из костного мозга. Тимус состоит из двух долей, разделённых соединительнотканной трабекулой. В доле зрелого тимуса различают корковый и мозговой слои. Корковый слой содержит делящиеся клетки — клетки-предшественницы Т-лимфоцитов, ранние про-тимоциты, имеющие морфологию лимфобластов. Их дальнейшая дифференцировка в CD4+- и CD8+-Т-лимфоциты протекает в мозговой части дольки тимуса и состоит в селекции клеток, которые способны связывать чужеродные Аг (положительная селекция), но не способны реагировать с собственными Аг (отрицательная селекция). В результате селекции только 3—5% клеток, продуцируемых в тимусе, приобретают специфические маркёры Т-хелперов и Т-супрессоров и мигрируют через мозговое вещество во вторичные лимфо-идные органы (селезёнка, лимфатические узлы). Остальные клетки погибают в корковом слое. Кроме того, в тимусе вырабатываются гуморальные факторы иммунной системы. Лимфатический узел — снаружи покрыт соединительнотканной капсулой, от которой отходят трабекулы. В лимфатическом узле различают корковую и мозговую части, а также синусы. В корковой части располагаются в основном В-лимфоциты и макрофаги, организованные в первичные и вторичные фолликулы. Т-лимфоциты преимущественно располагаются в субкортикальной зоне и в центре вторичных фолликулов. В лимфатическом узле Т-лимфоциты взаимодействуют с В-лимфоцитами и фолликулярными дендритными клетками в процессе иммунного ответа. Из паренхимы лимфатического узла лимфоциты поступают в выносящие лимфатические сосуды. Пейеровы бляшки. По ходу ЖКТ в непосредственной связи с эпителием располагаются лимфоидные скопления, называемые пейеровымибляшками. Их строение аналогично лимфоидным фолликулам селезёнки и лимфатических узлов. Главный компонент — большие зародышевые центры, окружённые лимфоцитами. Селезёнка — самый большой орган системы крови, покрытый снаружи соединительнотканной капсулой. Растяжение капсулы при увеличении селезёнки вызывает болевой синдром. В паренхиме органа различают красную пульпу (содержит эритроциты и многочисленные макрофаги, уничтожающие старые эритроциты), белую пульпу (совокупность лимфоидной ткани селезёнки, представленную скоплениями Т-лимфоцитов вокруг артерий, выходящих из трабе-кул) и лимфатические фолликулы, содержащие скопление В-лимфоцитов. ГШ 65 АНЕМИИ Анемия — уменьшение общего количества НЬ (или эритроцитов), которое, за исключением острых кровопотерь, характеризуется снижением уровня НЬ в единице объёма крови. Термин «анемия» отражает только изменения крови, выявленные лабораторными методами. Таким образом, анемия может характеризовать конкретное заболевание (например, железодефицитная анемия) или быть одним из симптомов других патологических состояний. В патогенезе нарушений, возникающих при анемии, ведущую роль играет нарушение оксигенации клеток различных органов и систем. Как следствие тканевой гипоксии возникают нарушение клеточного метаболизма и метаболический ацидоз. Раньше других на гипоксию реагирует ЦНС. Клинически данные патологические процессы проявляются в виде анемического синдрома, характеризующегося бледностью кожных покровов и видимых слизистых оболочек, слабостью, утомляемостью. Компенсаторно увеличиваются сердечный выброс и минутный объём, учащается сердечный ритм. Общие лабораторные признаки анемии (возможно изолированное существование одного признака или их сочетание, например для талассемий не характерно снижение количества эритроцитов): • содержание НЬ менее 100 г/л; • количество эритроцитов менее 4 • 1012/л; • содержание железа в сыворотке крови менее 14,3 мкмоль/л. Классификации анемий Анемия — всегда симптом какого-либо общего заболевания, поэтому строго классифицировать анемии невозможно. КЛАССИФИЦИРУЮЩИЕ КРИТЕРИИ Морфология эритроцитов. Объективный критерий оценки — размер эритроцита, составляющий в норме 7-8 мкм. В соответствии с этим выделяют микроцитарные (средний диаметр менее 6,7 мкм), нормоцитарные и макроцитарные (средний диаметр менее 9,5 мкм) анемии. Анемии Степень насыщения эритроцитов гемоглобином (или содержание сывороточного железа). Объективный критерий оценки — среднее содержание НЬ в эритроците, в норме составляет 27—33 пикограмма (пг). В повседневной практике наиболее доступный метод определения содержания НЬ в эритроцитах — определение цветового показателя. В норме значение цветового показателя — 0,8—1,0 (нормохромия эритроцитов), при значении цветового показателя менее 0,8 говорят об их гипохромии, при цветовом показателе более 1,0 — о гиперхромии (-хромный указывает на содержании НЬ в эритроцитах). Возможно сочетание двух критериев, например гипохромные микроци-тарные анемии, нормохромные нормоцитарные анемии. Степень регенерации эритроцитов определяют по количеству ретикулоцитов в периферической крови и по этому значению оценивают эффективность эрит-ропоэза. В норме количество ретикулоцитов в крови — 0,5—1,5% (5—15%о). Количество ретикулоцитов — индикатор работы красного ростка костного мозга. При их увеличении речь идёт о напряжённом эритропоэзе (гемолитические анемии, железодефицитные анемии). При их уменьшении говорят о неэффективном эритропоэзе (апластические анемии, витамин В^-дефицит-ные анемии, лейкозы). Ретикулоцитарный криз — повышение содержания ретикулоцитов в ответ на успешное лечение железодефицитной и витамин В12-дефицитной анемий. Концентрация гемоглобина. В зависимости от уровня НЬ различают лёгкую степень анемии (НЬ от 80 до 100 г/л), среднюю степень (НЬ от 60 до 80 г/л), тяжёлую степень (НЬ ниже 60 г/л). ПАТОГЕНЕТИЧЕСКАЯ КЛАССИФИКАЦИЯ • Анемии, вызванные нарушением синтеза гема (гипохромные микроцитар-ные): железодефицитные анемии, анемии, связанные с нарушением синтеза или утилизации порфиринов. • Анемии, вызванные нарушением синтеза глобина: количественные (талассе-мии) и качественные (аномальные гемоглобины — гемоглобинопатии). • Анемии гемолитические, связанные с дефектом мембраны эритроцита (мик-росфероцитоз, овалоцитоз, стоматоцитоз и др.); с дефицитом активности ферментов мембраны (Г-6-ФД и др.); связанные с образованием AT к Аг мембраны эритроцита (аутоиммунные гемолитические анемии — АИГА). • Анемии вследствие нарушения синтеза ДНК (гиперхромные макроцитар-ные с мегалобластным типом кроветворения): витамин Bi2-дефицитная анемия, фолиеводефицитная анемия. • Апластические анемии. ЖЕЛЕЗОДЕФИЦИТНАЯ АНЕМИЯ Железодефицитная анемия — гипохромная микроцитарная анемия, развивающаяся вследствие абсолютного уменьшения запасов железа в организме. Железодефицитная анемия возникает, как правило, при хронической потере крови или недостаточном поступлении железа в организм. ОБМЕН ЖЕЛЕЗА В ОРГАНИЗМЕ Железо участвует в функционировании всех биологических систем. Суточная потребность в железе составляет для мужчин 10 мг, для женщин 18 мг (в ВНУТРЕННИЕ БОЛЕЗНИ Глава 65 Железо, поступившее с пищей в течение суток (1-2 м г) Потеря железа с калом (> 0,7 мг/сут) \ / Кишечник
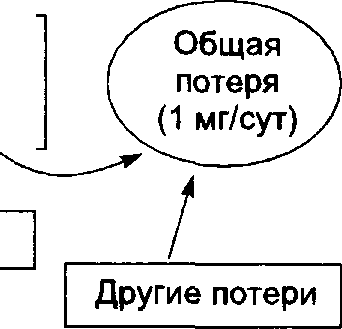 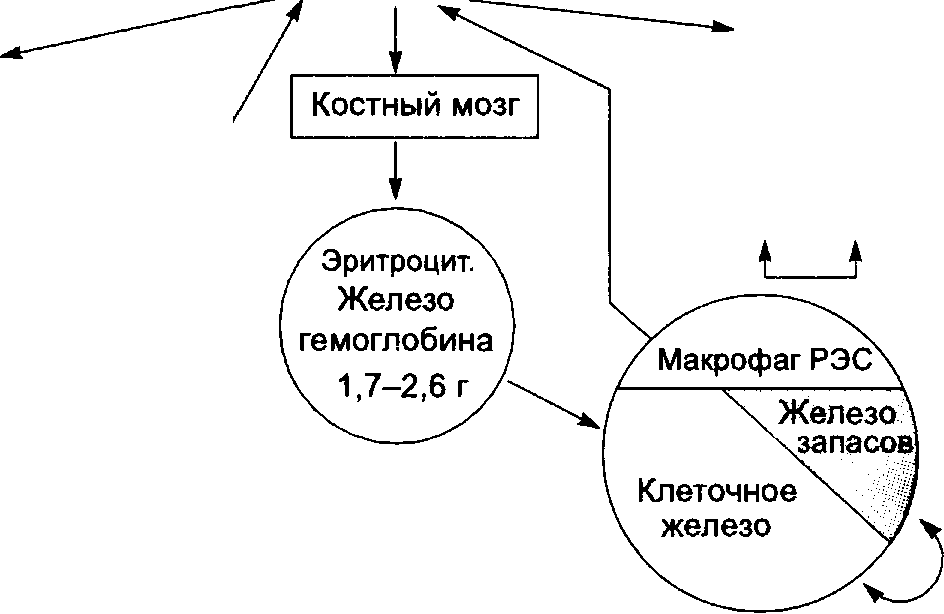
t_i Рис. 65-1. Схема обмена железа (Fe) в организме здорового мужчины с массой тела 70 кг. период беременности и лактации — 38 и 33 мг соответственно). Общее количество железа в организме составляет 4—4,5 г. Различают клеточное железо, внеклеточное железо и железо запасов (рис. 65-1). • Клеточное железо составляет значительную часть от общего количества железа в организме, участвует во внутреннем обмене железа и входит в состав гемсодержащих соединений (гемоглобина, миоглобина, ферментов, например, цитохромов, каталаз, пероксидазы), негемовых ферментов (например, НАДН-дегидрогеназы), металлопротеидов (например, аконитазы). • Внеклеточное железо. К нему относят свободное железо плазмы и желе-зосвязывающие сывороточные белки (трансферрин, лактоферрин), участвующие в транспорте железа. • Железо запасов находится в организме в виде двух белковых соединений — ферритина и гемосидерина — с преимущественным отложением в печени, селезёнке и мышцах и включается в обмен при недостаточности клеточного железа. Железо, попадая в организм с пищей, всасывается в кишечнике (в основном в двенадцатиперстной кишке и начальном отделе тощей кишки). Всасывание железа в ЖКТ ограничено и контролируется его концентрацией плазме (соотношением белков — апоферритина, свободного от железа, и ерритина). Усиливают всасывание аскорбиновая, янтарная, пировиноград-ная кислоты, сорбит, алкоголь, подавляют — оксалаты, препараты кальция и кальцийсодержащие продукты (например, творог, молоко и т.д.). В среднем в сутки всасывается 10 мг железа. Анемии Транспорт железа осуществляется белком трансферрином, который переносит железо в костный мозг, в места клеточных запасов железа (паренхиматозные органы, мышцы) и во все клетки организма для синтеза ферментов. Железо погибших эритроцитов фагоцитируют макрофаги. Основная потеря железа происходит с калом. Незначительная часть железа теряется с потом и клетками эпидермиса. Общая потеря железа — 1 мг/сут. Также физиологическими считают потери железа с менструальной кровью, с грудным молоком. РАСПРОСТРАНЁННОСТЬ Железодефицитная анемия — наиболее распространённая форма анемии, составляющая 80—95% всех анемий. Железодефицитную анемию наблюдают у 10—30% взрослого населения. У женщин она возникает значительно чаще, чем у мужчин. Приблизительно 60% всех случаев железодефицитной анемии наблюдают у пациентов старше 65 лет. ЭТИОЛОГИЯ • Хроническая потеря крови: желудочно-кишечные кровотечения (в том числе из дивертикула Меккеля),телеангиэктазии и другие сосудистые аномалии, маточные кровотечения (гиперполименорея, меноррагия), кровоточащие опухоли, гематурия, донорство крови, кровотечения в замкнутые полости, эндометриоз, синдром Гудпасчера. • Нарушение всасываемости железа: синдром нарушенного всасывания, це-лиакия, хронические заболевания ЖКТ (гастродуодениты, хронические энтериты, колиты), резецированный желудок и кишечник. • Увеличение потребности организма в железе при росте организма, хронических кровопотерях, беременности и лактации. • Недостаточное поступление железа во время беременности при анемии у матери и с пищей. • Другие причины — хроническая почечная недостаточность, гемосидероз лёгких. ПАТОГЕНЕЗ Недостаточность железа НЬ приводит к гемической гипоксии, так как снижается способность эритроцитов к связыванию и транспорту кислорода. Снижение транспортной функции крови приводит к усилению работы сердца. Повышение ударного объёма и учащение сердечных сокращений приводит к увеличению минутного объёма крови, что частично компенсирует недостаток кислорода. Этот механизм становится недостаточным при выраженной анемии, и развивается тканевая гипоксия. Гипоксия приводит к нарушению метаболизма и развитию ацидоза. Уменьшение синтеза миогло-бина приводит к мышечной гипотонии и дистрофии. Истощение клеточных ферментов, участвующих в основных видах обмена, приводит к нарушению трофики клеток и тканей, их дегенеративным изменениям. Недостаточное поступление железа в костный мозг обусловливает нарушение эритропоэза. При истощении клеточного железа во внутренний обмен вступает железо запасов. Таким образом, в результате перечисленных механизмов развивается сидеропения — обеднение железом клеток. ВНУТРЕННИЕ БОЛЕЗНИ | ||||||||||||||||||||||||||||||
