1Коллапсотерапия применение при туберкулезе
 Скачать 1.68 Mb. Скачать 1.68 Mb.
|
|
Медицинская помощь сельскому населению организована по принципу этапности. Такими этапами являются фельдшерско-акушерские пункты (ФАП), врачебная амбулатория или сельская участковая больница, центральная районная больница (ЦРБ), областные учреждения. Такая этапность сохраняется и в организации противотуберкулезной помощи детям. В сельской местности противотуберкулезная работа проводится работниками общелечебной медицинской сети на местах и требует постоянного руководства и контроля фтизиатра районного противотуберкулезного диспансера (кабинета). Раннее выявление туберкулеза при существующей системе расселения небольшими поселками представляет наибольшие трудности. Все виды специализированной медицинской помощи в сельском районе сосредоточены в районном центре, в ЦРБ. Чем дальше расположен тот или иной поселок от районного центра, тем меньше активная обращаемость населения в районную больницу. Например, уже на расстоянии 1 — 5 км от врачебного участка количество обращений уменьшается на 38 %, на расстоянии 6 — 10 км — на 46 %, а за пределами десятикилометрового радиуса оно в 2,7 раза ниже, чем в районном центре. В то же время заболеваемость жителей отдаленных сел, как это показывают углубленные медицинские осмотры, не отличается от заболеваемости жителей районных центров. Следовательно, основная масса больных в отдаленных сельских местностях получает медицинскую помощь у фельдшеров. И значение этой помощи увеличивается с увеличением расстояния от места проживания больного до врачебного учреждения. Поэтому для значительной части сельского населения один из важнейших путей выявления туберкулеза — обращение в поликлинику — существенно затрудняется. 73 Эпидемиологические показатели смотри 36 74 Обязанности первичного звена медпомощи  75 Обязанности терап службы смотри 74 76 Современные особенности выявления костно – суставного туберкулеза Костно-суставной туберкулез, как и другие локализации внелегочного туберкулеза, возникает в результате гематогенной диссеменации микобактерий туберкулеза, которая наступает либо при первичном инфицировании организма, либо в более поздние сроки, когда ее источником являются активные или скрытые, многолетней давности туберкулезные очаги, локализующиеся в том или ином органе. Костно-суставной туберкулёз, по своей сути является специфическим гематогенным остеомиелитом. Костный туберкулёз в типичных случаях характеризуется вялым течением с прогрессированием клинической картины, и отсутствием эффекта от проводимой неспецифической антибактериальной терапии. Туберкулёзом поражаются те кости или отделы костей, которые содержат максимальное количество миелоидного костного мозга, и имеют богатое кровоснабжение - это позвоночник и метаэпифизы трубчатых костей. В структуре костно-суставного туберкулёза первое место по частоте встречаемости занимает туберкулез позвоночника, далее по убывающей - туберкулёз тазобедренного, коленного, голеностопного, плечевого, локтевого суставов и т. д. Туберкулез костей и суставов поражает лиц разного возраста и является одной из самых частых локализацией внелегочного туберкулеза. В последние годы отмечается "постарение" больных этой формой заболевания, она стала чаще возникать в пожилом возрасте. Однако также увеличилось и количество детей, страдающих этим тяжким недугом, в возрасте от 1 до 4-5 лет. В течение 1-2 лет туберкулезный очаг, развивающийся внутрикостно, может давать только малую симптоматику: которая проявляется в первую очередь признаками туберкулезной интоксикации (слабость, повышенная утомляемость, субфебрильная температура, снижение аппетита, нарушение сна), а также уплотнение подкожно-жировой клетчатки на стороне поражения, гипотрофия мышц, локальный остеопороз, нарушения трабекулярной структуры костной ткани, определяемые на рентгенограмме (симптом "тающего сахара"). В дальнейшем боли становятся постоянными, подчас мучительными, ограничиваются движения, нарушается функция позвоночника или конечности. На рентгенограммах кроме остеопороза появляются ограниченные деструктивные изменения в виде изолированных внутрикостных очагов преимущественно с нечеткими контурами в эпиметафизарных отделах. Иногда в деструктивной полости обнаруживаются костные секвестры. В дальнейшем при развитии заболевания деструктивный процесс распространяется через суставной хрящ или межпозвонковый диск на смежные отделы и проявляются контактной деструкцией суставных концов костей или нескольких позвонков. В завершающей стадии туберкулеза прогрессирующие деструктивные изменения ведут к полному разрушению сустава или распространенному поражению позвоночника. В настоящее время теоретически обоснованным и практически оправдавшим себя является принцип раннего хирургического лечения, который при отдельных формах различных локализаций позволяет сократить сроки лечения в 2 - 3 раза. Следует отметить, что значение хирургического метода возрастает в связи с увеличением числа запущенных случаев заболевания, снижением эффективности противотуберкулезной терапии, увеличивающимся количеством заболеваний, вызванных устойчивыми штаммами микобактерий. Характерной особенностью туберкулёзных очагов, возникающих в костях, является рано наступающее творожисто-некротическое их перерождение, обусловливающее необычайно устойчивое существование таких образований и сохранность в них признаков потенциальной активности в течение длительного времени после клинического затихания, что служит источником новых вспышек процесса. Оперативное удаление костного очага предупреждает дальнейшую деструкцию кости, устраняет препятствие для регенерации костной ткани, а вместе с тем создаёт благоприятные условия для антибактериальной терапии в послеоперационном периоде и для полной ликвидации туберкулёзного воспаления, значительно ускоряя клиническое излечение. Для своевременного выявления туберкулезной этиологии поражения позвоночника, других костей и суставов необходим сбор фтизиатрического анамнеза, осмотр больного с оценкой двигательных функций, общие анализы крови и мочи, туберкулиновая проба, ИФА крови, флюорография органов грудной клетки, прицельная рентгенография в прямой и боковой проекциях пораженного отдела позвоночника, сустава или кости, рентгенотомография их для выявления очагов воспаления и деструкции в костное ткани. При поражении сустава на ранних стадиях для сравнения должна быть сделана рентгенограмма здорового симметричного сустава. Необходима биопсия увеличенных регионарных лимфоузлов, цитологическое исследование содержимого абсцессов и биоптатов и бактериологический анализ их на микобактерии туберкулеза. В пользу туберкулезной этиологии заболевания будут говорить фтизиатрический анамнез, изменения на флюорограмме органов грудной клетки, положительные результаты ИФА и туберкулиновых проб, изменения в анализах крови и мочи, наличие характерных признаков при рентгено-томографии костей и суставов. Наиболее убедительным признаком туберкулеза является обнаружение микобактерии туберкулеза в отделяемом свищей и биоптатах. Но даже, если при бактериоскопии их микобактерии туберкулеза не найдены, но имеется хотя бы часть признаков, позволяющих заподозрить туберкулез, больной должен быть направлен к специалисту по костно-суставному туберкулезу для дальнейшего обследования и уточнения диагноза. Врач общей лечебной сети должен помнить, что каждому больному, обратившемуся с жалобами на боли в позвоночнике, других костях и суставах, необходимо выполнить рентгенограммы этих отделов в прямой и боковой проекциях. 78 Алгоритм обследования на туберкулез МПС Классификация туберкулёза мочеполовой системы включает следующие клинические формы: туберкулёз паренхимы почек (I стадия, недеструктивная форма); туберкулёзный папиллит (II стадия, ограниченно-деструктивная форма;. кавернозный нефротуберкулёз (III стадия, деструктивная форма); поликавернозный нефротуберкулёз (IV стадия, распространённо деструктивная форма). Осложнения туберкулёза мочеполовой системы: туберкулёз мочеточника; туберкулёз мочевого пузыря; туберкулёз мочеиспускательного канала; хроническая почечная недостаточность; свищ поясничной области.   79 Режимы химиотерапии туберкулеза Основные противотуберкулезные препараты: изониазид (H), рифампицин (R), пиразинамид (Z), этамбутол (E) и стрептомицин (S) являются высокоэффективными в отношении микобактерий, чувствительных ко всем противотуберкулезным препаратам. Следует отметить, что только в России имеются альтернативные изониазиду препараты, такие как феназид, фтивазид и метазид, которые вызывают меньше побочных эффектов При лечении лекарственно–устойчивого туберкулеза легких используются резервные противотуберкулезные препараты: канамицин (K), амикацин (A), капреомицин (Cap), циклосерин (Cs), этионамид (Et), протионамид (Pt), фторхинолоны (Fq), парааминосалициловая кислота – ПАСК (PAS) и рифабутин (Rfb). Одновременное назначение нескольких противотуберкулезных препаратов (не менее 4–х) позволяет завершить курс лечения до появления лекарственной резистентности микобактерий или же преодолеть начальную резистентность их к одному и двум препаратам. В связи с различным состоянием микобактериальной популяции на разных этапах болезни научно–обоснованным является деление химиотерапии туберкулеза на 2 периода или фазы лечения [1,5,9,11]. Начальная (или интенсивная) фаза лечения направлена на подавление быстро размножающейся и активно метаболизирующей микобактериальной популяции и содержащихся в ней лекарственно резистентных мутантов, уменьшение ее количества и предотвращение развития вторичной резистентности. Для лечения туберкулеза, вызванного лекарственно чувствительными микобактериями, применяются 4 противотуберкулезных препарата: изониазид, рифампицин, пиразинамид, этамбутол или стрептомицин в течение 2–х месяцев и затем 2 препарата – изониазид и рифампицин в течение 4–х месяцев. Изониазид, рифампицин и пиразинамид составляют ядро комбинации при воздействии на чувствительные микобактерии туберкулеза. При этом необходимо подчеркнуть, что изониазид и рифампицин, одинаково эффективно воздействуют на все популяции микобактерий, находящиеся в очаге туберкулезного воспаления. В то же время изониазид бактерицидно воздействует на всех чувствительных к обоим препаратам микобактерий и убивает рифампицин–резистентных возбудителей. В то время как рифампицин также убивает микобактерии, чувствительные к двум этим препаратам, и, что особенно важно, бактерицидно воздействует на изониазид–резистентные микобактерии. Рифампицин эффективно воздействует на персистирующие микобактерии, если они начинают «просыпаться» и усиливать свою метаболическую активность. В этих случаях рифампицин более эффективен, чем изониазид. Присоединение пиразинамида и этамбутола к комбинации изониазида и рифампицина создает условия усиления воздействия их на возбудителя и препятствует формированию резистентности микобактерий. В случаях лекарственно-устойчивого туберкулеза возникает вопрос использования резервных противотуберкулезных препаратов, комбинации которых и длительность их приема еще полностью не разработаны в контролируемых клинических испытаниях и до сих пор носят в основном эмпирический характер [2,6,1]. Комбинация фторхинолона, пиразинамида и этамбутола проявляет активность в отношении штаммов с множественной лекарственной резистентностью, но не достигает уровня активности комбинации изониазида, рифампицина и пиразинамида в отношении чувствительных микобактерий. Это необходимо учитывать при продолжительности интенсивной фазы лечения лекарственноустойчивого туберкулеза легких. Длительность и эффективность интенсивной фазы лечения должны основываться на показателях прекращения бактериовыделения по мазку и посеву мокроты, выявленной лекарственной резистентности и положительной клинико–рентгенологической динамики заболевания. Вторая фаза лечения – это воздействие на оставшуюся медленно размножающуюся и медленно метаболизирующую микобактериальную популяцию, в большинстве своем находящуюся внутриклеточно, в виде персистирующих форм микобактерий. На этом этапе главной задачей является предупреждение размножения оставшихся микобактерий, а также стимуляция репаративных процессов в легких с помощью различных патогенетических средств и методов лечения. Лечение необходимо проводить еще в течение длительного периода времени, чтобы обезвредить микобактерии, которые в силу своей низкой метаболической активности плохо поддаются уничтожению с помощью противотуберкулезных препаратов. Режим антибактериального лечения туберкулеза, то есть выбор оптимальной комбинации противотуберкулезных препаратов, их доз, путей введения (внутрь, внутривенно, внутримышечно, ингаляционно и т.д.), продолжительность и ритм применения (однократно или интермиттирующим методом), определяется с учетом: эпидемиологической опасности (заразности) больного при обнаружении микобактерий туберкулеза в мокроте методом микроскопии и посева на питательные среды; характера заболевания (впервые выявленный случай, рецидив, хроническое течение); распространенности и тяжести специфического процесса; лекарственной резистентности микобактерий туберкулеза. Принимая во внимание необходимость химиотерапии для всех больных, нуждающихся в лечении, и различную методику для разных категорий разных групп больных, общее признание получило разделение больных туберкулезом в соответствии со следующими 4–я категориями химиотерапии [1,4,6,9,10,11]. Стандартные режимы химиотерапии, применяемые у больных различных категорий, представлены в таблице 1. 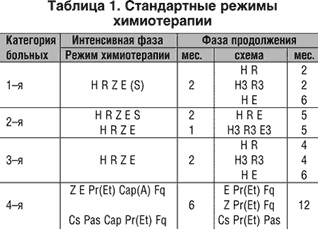 К 1–й категории химиотерапии относятся больные с впервые выявленным туберкулезом легких с выделением микобактерий, обнаруженных при микроскопии мазка мокроты, и больные с впервые выявленными распространенными (более 2–х сегментов) и тяжело протекающими формами туберкулеза (диссеминированный, генерализованный, казеозная пневмония) при отрицательных данных микроскопии мазка мокроты. Интенсивная фаза химиотерапии предусматривает назначение в течение 2 месяцев 4–х лекарств из числа основных противотуберкулезных препаратов: изониазид, рифампицин, пиразинамид, этамбутол или стрептомицин (2 H R Z E или S). За этот срок пациент должен принять 60 доз комбинации назначенных противотуберкулезных препаратов. Если будут дни, когда полную дозу химиотерапии больной не принял, то не количество календарных дней будет определять длительность данной фазы лечения, а количество принятых доз химиопрепаратов, т.е. 60. Такой расчет длительности лечения по принятым дозам химиотерапии должен проводиться у больных всех 4–х категорий. Назначение стрептомицина вместо этамбутола должно основываться на данных распространенности резистентности микобактерий туберкулеза к данному препарату и изониазиду в конкретном регионе. В случаях высокой начальной резистентности к изониазиду и стрептомицину четвертым препаратом назначается этамбутол, так как только этамбутол в этом режиме эффективно воздействует на изониазид– и рифампицин–резистентные микобактерии туберкулеза. При продолжающемся бактериовыделении и отсутствии положительной клинико–рентгенологической динамики процесса в легких интенсивная фаза лечения должна быть продолжена еще на 1 месяц (30 доз), пока не будут получены данные лекарственной резистентности микобактерий туберкулеза. При выявлении лекарственной резистентности микобактерий проводится коррекция химиотерапии. Возможно сочетание основных, к которым сохранилась чувствительность МБТ, и резервных препаратов. Однако комбинация должна состоять из 4–5 препаратов, из которых не менее 2–х должны быть резервными. В режим химиотерапии никогда не следует добавлять только 1 резервный препарат из–за опасности монотерапии и формирования резистентности, т.к. только добавление 2–х и более резервных препаратов в режим химиотерапии минимизирует риск дополнительного развития лекарственной резистентности микобактерий туберкулеза. Показанием для фазы продолжения лечения является прекращение бактериовыделения по микроскопии мазка мокроты и положительная клинико–рентгенологическая динамика процесса в легких. При сохранении чувствительности микобактерий туберкулеза лечение продолжается 4 месяца (120 доз) изониазидом и рифампицином (4 H R) как ежедневно, так и в интермиттирующим режиме 3 раза в неделю (4 H3 R3). Альтернативным режимом в фазе продолжения лечения является использование изониазида и этамбутола в течение 6 месяцев (6 H Е). Общая продолжительность лечения больных 1–й категории составляет 6–7 месяцев. При выявлении лекарственной резистентности микобактерий туберкулеза по исходным данным, но при прекращении бактериовыделения по микроскопии мокроты к концу начальной фазы лечения через 2 месяца возможен переход на фазу продолжения с удлинением ее сроков. При исходной резистентности к изониазиду и/или стрептомицину лечение в фазе продолжения проводится рифампицином, пиразинамидом и этамбутолом в течение 6–ти месяцев (6 R Z E) или рифампицином и этамбутолом в течение 9–ти месяцев (9 R E). Общая продолжительность лечения при этом составляет 9–12 месяцев. При исходной резистентности к рифампицину и/или стрептомицину фаза продолжения лечения проводится изониазидом, пиразинамидом и этамбутолом в течение 12 месяцев (12 H Z E) или изониазидом и этамбутолом в течение 15 месяцев (15 H E). В этом случае общая продолжительность лечения составляет 15–18 месяцев. При множественной резистентности микобактерий туберкулеза к изониазиду и рифампицину больному назначается индивидуальный режим лечения по 4–й категории. Ко 2–й категории химиотерапии относят больных с рецидивом заболевания, неудачей предыдущего лечения, перерывом лечения более 2–х месяцев, получающих неадекватную химиотерапию более 1 месяца (неправильная комбинация препаратов и недостаточные дозы), и с высоким риском развития лекарственноустойчивого туберкулеза легких. Интенсивная фаза химиотерапии предусматривает назначение в течение 3 месяцев 5–ти основных противотуберкулезных препаратов: изониазид, рифампицин, пиразинамид, этамбутол и стрептомицин, и за этот срок пациент должен получить 90 доз комбинации назначенных лекарств. В интенсивной фазе применение стрептомицина ограничено 2 месяцами (60 доз) (2 H R Z E S + 1 H R Z E). Интенсивная фаза химиотерапии может быть продолжена при сохраняющемся бактериовыделении и при отрицательной клинико–рентгенологической динамике заболевания, пока не будут получены данные лекарственной резистентности микобактерий туберкулеза. Если к концу интенсивной фазы лечения продолжается бактериовыделение по микроскопии мазка и посева мокроты и выявлена лекарственная резистентность к аминогликозидам, изониазиду или рифампицину, то вносятся изменения в режим химиотерапии. При этом остаются те основные препараты, к которым сохранилась чувствительность микобактерий туберкулеза, и дополнительно вводится в режим не менее 2–х резервных химиопрепаратов, ведет к удлинению интенсивной фазы еще на 2–3 месяца. Возможные схемы и режимы химиотерапии в этих случаях приводятся в таблице 2. Показанием для фазы продолжения лечения является прекращение бактериовыделения по микроскопии мазка и посева мокроты и положительная клинико–рентгенологическая динамика специфического процесса. При сохранении чувствительности микобактерий туберкулеза лечение продолжается 5 месяцев (150 доз) 3 препаратами: изониазидом, рифампицином, этамбутолом (5 H R E) ежедневно или в интермиттирующем режиме 3 раза в неделю (5 H3 R3 E3). Общая продолжительность лечения 8–9 месяцев. У больных, у которых имеются эпидемиологические (высокий уровень резистентности МБТ к изониазиду и рифампицину в данном регионе), анамнестические (контакт с известными диспансеру больными, выделяющими МБТ с множественной лекарственной резистентностью), социальные (лица БОМЖ, освобожденные из пенитенциарных учреждений) и клинические (больные остро прогрессирующим туберкулезом, неадекватным лечением на предыдущих этапах с использованием 2–3 препаратов, перерывами в лечении) основания для предположения о множественной лекарственной резистентности микобактерий туберкулеза возможно в интенсивную фазу в течение 3–х месяцев применение эмпирического режима химиотерапии, состоящего из изониазида, рифампицина (рифабутина), пиразинамида, этамбутола канамицина (амикацина, капреомицина) и фторхинолона [3 H R(Rf) Z E + K(A Cap) Fq ] [1, 2]. При множественной резистентности МБТ к изониазиду и рифампицину больному назначается индивидуализированный режим лечения по 4–й категории. К 3–й категории относят больных с впервые выявленными малыми формами туберкулеза легких (протяженностью до 2–х сегментов) с отсутствием выделения микобактерий туберкулеза при микроскопии мазка мокроты. В основном это больные с очаговым, ограниченным инфильтративным туберкулезом и туберкулемами. В течение 2–х месяцев интенсивной фазы химиотерапии используются 4 противотуберкулезных препарата: изониазид, рифампицин, пиразинамид и этамбутол (2 H R Z E). Введение в режим химиотерапии четвертым препаратом этамбутола обусловлено высокой начальной резистентностью микобактерий туберкулеза к стрептомицину. Интенсивная фаза химиотерапии продолжается 2 месяца (60 доз). Если получен положительный результат посева культуры МБТ, а результат чувствительности еще не готов, лечение продолжается до получения сведений о лекарственной чувствительности МБТ, даже если продолжительность интенсивной фазы лечения превысит 2 месяца (60 доз). Показанием для фазы продолжения лечения является выраженная клинико–рентгенологическая динамика заболевания. В течение 4–х месяцев (120 доз) проводится химиотерапия изониазидом и рифампицином как ежедневно (4 H R), так и в инттермиттирующем режиме 3 раза в неделю (4 H3 R3) или же 6 месяцев изониазидом и этамбутолом (6 H E). Общая продолжительность лечения 4–6 месяцев. К 4–й категории относятся больные туберкулезом, выделяющие множественно лекарственно–резистентные микобактерии. Подавляющее большинство их составляют больные фиброзно–кавернозным и хроническим диссеминированным туберкулезом, с наличием деструктивных изменений, сравнительно небольшую часть составляют больные с цирротическим туберкулезом и наличием деструкций. Перед началом химиотерапии необходимо обязательно уточнить лекарственную чувствительность микобактерий по данным предшествующих исследований, а также в процессе обследования больного перед началом лечения. Поэтому желательно применение ускоренных методов бактериологического исследования полученного материала и ускоренных методов определения лекарственной чувствительности, в том числе используя BACTEC и прямой метод бактериологического исследования. Лечение проводится по индивидуальным режимам химиотерапии согласно данным лекарственной резистентности микобактерий туберкулеза и должно осуществляться в специализированных противотуберкулезных учреждениях, где проводится централизованный контроль качества микробиологических исследований и имеется необходимый набор резервных противотуберкулезных препаратов, таких как канамицин, амикацин, протионамид (этионамид), фторхинолоны, циклосерин, капреомицин, ПАСК. Интенсивная фаза лечения составляет 6 месяцев, в течение которых назначается комбинация как минимум из 5–ти химиопрепаратов: пиразинамида, этамбутола, фторхинолонов, капреомицина (канамицина) и протионамида (этионамида) [6 Z E Fq Cap(K) Pr(Et)]. В этом плане из–за вероятной малой эффективности использования комбинации резервных препаратов, а также рецидивов туберкулеза, вызванного множественно резистентным возбудителем, химиотерапия проводится не менее 12–18 месяцев. При этом больным рекомендуется принимать лекарства ежедневно и не применять резервные препараты в интермиттирующем режиме, т. к. не существует подтверждающих эту возможность клинических испытаний. При резистентности к этамбутолу, пиразинамиду и/или другому препарату возможна замена на циклосерин или ПАСК [6 Cs Pas Fq Cap Pr(Et)]. Интенсивная фаза должна продолжаться до получения положительной клинико–рентгенологической динамики и отрицательных мазков и посевов мокроты. В этот период искусственный пневмоторакс и хирургическое лечение является важным компонентом лечения лекарственноустойчивого туберкулеза легких с множественной резистентностью микобактерий, однако при этом должен быть проведен полный курс химиотерапии. Показанием для фазы продолжения лечения является прекращение бактериовыделения по микроскопии мазка и посева мокроты, положительная клинико–рентгенологическая динамика специфического процесса в легких и стабилизация течения заболевания. Комбинация препаратов должна состоять, как минимум, из 3–х резервных препаратов, таких как этамбутол, протионамид и фторхинолон, которые применяются в течение не менее 12 месяцев (12 E Pr Fq). Общая длительность лечения больных 4–й категории определяется темпами инволюции процесса, но не менее 12–18 месяцев. Столь длительный срок лечения обусловлен задачей добиться стойкой стабилизации процесса и ликвидации бактериовыделения. При этом очень важно обеспечить длительное лечение таких больных резервными противотуберкулезными препаратами. 80 Диагностика и лечение острого отравления ГИНК Препараты ГИНК применяют с 1952 г., хотя изониазид был синтезирован в Праге на 40 лет раньше. Главным из них считают изониазид (Isoniazidum), эмпирическая формула которого C6H7N3O. Применяют также метазид (С13Н10N6O2), фтивазид (C14H13N3O3), ларусан (C14H13N3O2), салюзид (C16H15N3O5) и некоторые другие. Причины и патогенетические механизмы Клиническая характеристика подочных реакций изониазида. По выраженности и тяжести токсического действия изониазида в первую очередь на ЦНС представляется целесообразным выделить 4 степени клинических проявлений побочных реакций: 1) легкая; 2) средняя; 3) тяжелая; 4) острое отравление изониазидом. Реакции легкой степени характеризуются кратковременными, не постоянными головными болями, головокружением, тошнотой, не глубокими нарушениями сна и психического статуса, преходящим умеренным повышением артериального кровяного давления. Общее состояние при этом страдает мало, больные соблюдают активный режим. При реакциях средней степени тяжести – эти симптомы имеют более выраженный и стойкий характер с постоянными в течение дня интенсивными головными болями, сильным головокружением, неустойчивостью при ходьбе, плохим сном, депрессией, высоким артериальным давлением. Подобное ухудшение состояния вынуждает больного соблюдать постельный режим. Тяжелые токсические реакции, наряду с вышеназванными симптомами характеризуются развитием кратковременных, 1-2 кратных эпилептиформных судорог с потерей сознания на короткий срок без признаков отека головного мозга. Крайней степенью токсического действия изониазида является острое отравление, характеризующееся в первую очередь многократными продолжительными судорожными сокращениями, длительной потерей сознания, выраженной патологией многих систем организма и клиническим синдромом отека головного мозга. Т.е. острое отравление изониазидом является качественно новым проявлением токсического действия препарата, отличающимся выраженным, длительным нарушением жизненно важных функций организма, и представляет собой крайнюю степень опасности для жизни больного. Согласно официальным токсикологическим формулировкам острое медицинское отравление – это особое болезненное состояние, вызванное неправильной дозировкой, неправильным применением или неправильным приготовлением лекарственного средства. В большинстве своем отравление изониазидом связано с приемом больших доз препарата (20-60 грамм), главным образом, с целью самоубийства, а также в связи с небрежностью медицинского или аптечного персонала, ошибками больного. Следует подчеркнуть особую тяжесть токсических реакций на изониазид при употреблении алкоголя, особенно выпитого непосредственно после приема изониазида. Употребление алкоголя вызывает пищеварительные нарушения и недостаток витаминов группы В, а также ускоряет всасывание изониазида из пищеварительного тракта (при приеме внутрь), что утяжеляет клиническую картину и прогноз отравления. Сроки развития острого отравления зависят от дозы препарата и метода его введения. При приеме внутрь средней токсической дозы изониазида (условно в пределах 40-70 мг/кг) синдром отравления развивается, как правило, через 1,5-2часа, при приеме внутрь высокой токсической дозы (условно выше 70мг/кг) – через 30-40 минут после приема изониазида. При внутривеннном введении препарата в зависимости от его количества, скорости вливания признаки отравления развиваются или в конце инфузии, или спустя 20-40 минут после её окончания. Патогенетическую основу побочных реакций составляет описанное выше воздействие изониазида на обмен пиридоксина с образованием высокотоксичных соединений. С другой стороны изониазид, обладая низким молекулярным весом, быстро и в значительном количестве проникает в ткани организма, легко преодолевает гематоэнцефалический барьер и создает высокую концентрацию в ликворе. При передозировке препарата он может оказывать и прямое токсическое воздействие на ЦНС (как непосредственно на ткань мозга, так и на его сосудистую систему). На секции больных, умерших от отравления ГИНК, находят картину вазогенного диатеза с набуханием эндотелия, с наличием гиперемии, кровоизлияний, кровавых транссудатов в органах и различных полостях. Наиболее интенсивные изменения находят в ЦНС, что обусловливает ведущий симптомокомплекс в общей картине острого отравления. 81 Приказ № 109 |
