конспект лекций по физхимии. Конспект лекций по дисциплине Химия тема 1 основые понятия и законы химии. Основные законы химии. Закон сохранение массы
 Скачать 1.45 Mb. Скачать 1.45 Mb.
|
|
ТЕМА 9: АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ. Ароматическими углеводородами или аренами называют вещества, в молекулах которых содержится одно или несколько бензольных колец. Простейшим представителем класса аренов является бензол. БЕНЗОЛ. Строение молекулы бензола. В 1865 г немецкий химик Ф. Кекуле предложил первую структурную формулу бензола, представляющую собой цикл из шести атомов углерода с чередующимися одинарными и двойными связями. Эту формулу широко использует химики и сейчас. По современным представлениям все шесть атомов углерода в бензоле находятся в состоянии sp2-гибридизации. За счет трех гибридных sр2-орбиталвй каждый атом образует сигма-связи с двумя соседними углеродными атомами и с одним атомом водорода. Оставшиеся p-электроны образуют общее шестиэлектронное облако равномерно распределенное по бензольному кольцу. Все связи С-С будут равноценными. Они являются полуторными или, как говорит, носят ароматический характер.  Физические свойства бензола. Бензол - бесцветная жидкость, температура кипения t = 80º, легче воды, имеет характерный запах, хороший растворитель, ядовит. Химические свойства бензола. По химическим свойствам бензол как бы занимает промежуточное положение между предельными и непредельными углеводородами, гак как для него возможны реакции замещения и присоединения. 1. Реакции замещения: а) галогенирование б) нитрование 2. Реакции присоединения: а) гидрирование б) хлорирование 3. Горение. Получение бензола.
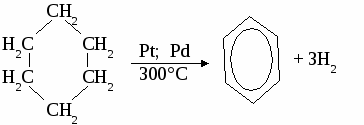 3. Тримеризация ацетилена. Гомологи бензола 1. Номенклатура гомологов бензола. 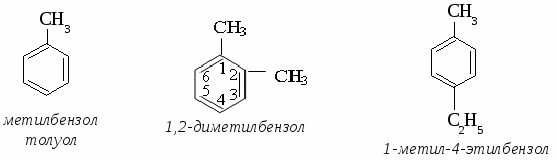 Химические свойства толуола. (взаимное влияние групп атомов в молекуле толуола) 1. Нитрование. 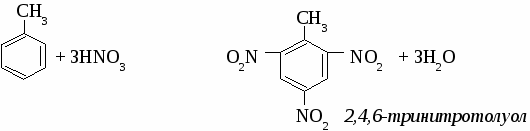 2. Окисление раствором перманганата калия.  Упражнение. Составить уравнения реакций по схеме: метан → хлорметан → этан → этилен → дихлорэтан Задача №1. Сколько мл бензола (плотность 0,9 г (мл))потребуется для получения 30,75 г нитробензола, если массовая доля выхода нитробензола составляет 90%? Задача №2. Сколько г бромбензола можно получить при бромировании бензола массой 117 г бромом массой 316 г? Какое из исходных веществ останется в избытке? ТЕМА 10: ПРИРОДНЫЕ ИСТОЧНИКИ УГЛЕВОДОРОДОВ. 1.Природные газы. Природные газы образуют самостоятельные месторождения, состоят в основном из метана (до 98%). Природные газы используются как топливо и сырье для химической промышленности. 2.Попутные нефтяные газы. Попутные нефтяные газы встречаются вместе с нефтью в ее месторождениях, образуя газовую шапку и частично растворяясь в нефти. Попутные нефтяные газы содержат газообразные углеводороды от метана до бутана илегкокипящие жидкие углеводороды от пентана до гептана. Попутные нефтяные газы используются как высококалорийное топливо и очень ценное сырье для химической промышленности. 3.Нефть. Нефть - маслянистая жидкость, цвет от желтого до черного с характерным запахом, в основном легче воды. В состав нефти входят около 900 различных соединений, поэтому нефть не имеет определенной температуры кипения. Сырая нефть используется для получения различных нефтепродуктов. Нефтепродукты. 1 Бензин. Бензин содержит углеводороды от С5 до С11 стемпературой кипения от 20° до 200° С. По назначению бензин подразделяют на автомобильный и авиационный. Автомобильные бензины маркируют буквой А, авиационные - буквой Б. Например: А 72, А 96, Б 70, Б 115. Цифра в марке бензина указывает его октановоечисло, то есть определяет его качество (детонационную стойкость). СН3 – СН2 – СН2 – СН2 – СН2 – СН2 – СН3 нормальный гептан (октановое число равно нулю) 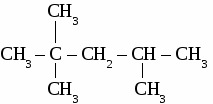 2,2,4-триметплпентан (изооктан) - октановое число равно 100. Для повышения октанового числа используют антидетонаторы. 1. Этиловая жидкость (смесь тетраэтилсвинца и бромэтана). (С2Н5)4Pb и С2Н5Br 2. Циклопентадиенилмарганецтрикарбонил (ЦТМ).  Керосин. - Авиационное и ракетное топливо, осветительный керосин. Газойль. - Дизельное топливо. Мазут. - Котельное топливо, сырье для получения смазочных масел. Парафин. Используется в медицине, электротехнике. Переработка нефти. 1. Перегонка нефти. Перегонку осуществляют при температурах 320°-350°С Крекинг нефтепродуктов.  а) термический крекинг температура процесса 500° - 550°С б) каталитический крекинг температура процесса 450° - 500°С катализаторы: Al2O3; SiO2; Pt. КОКСОВАНИЕ КАМЕННОГО УГЛЯ. Коксование - разложение каменного угля при нагревании его без доступа воздуха при температуре около 1100°С. Продукта коксования.
Упражнения:
а) 1,2,4-триметилбензол б) 3-бром-2,2-диметилгексан в) 3-метилбутин-1 г) 2,4-диметилпентадиен-2,3 д) 2-хлор-3,3-диэтилгексан ТЕСТ ПО ТЕМЕ «УГЛЕВОДОРОДЫ» Вариант №1 Часть I. 1. Углеводород С4Н10 относится к классу:
2. Общая формула циклоалканов:
3. Молекулы алкадиенов содержат:
4. Угол связи в молекуле бензола:
5. Тип гибридизации атомов углерода в молекуле этилена:
6. Вещества одинакового состава, но различного строения и с различными свойствами называют: а) радикалами в) изомерами б) гомологами г) аналогами 7. Какой тип реакции характерен для алкенов:
8. При гидрировании алкенов образуются:
9. Продуктом реакции бутена -1 с хлором является:
10. Каучук получают, используя реакцию:
11. Ацетилен не может реагировать
12.Cпособ разделения нефти фракции основан на:
Часть II. 1. Составьте формулы четырех изомеров пентена, назовите их. (4 балла) 2. Составьте формулы по названиям: (4 балла) а) 2,3,4-триметилпентан б) 2,2-дибром-4-эгилгептан в) 1-хлор-3-метилбензол г) 2,4-дихлор-3-метилгексен-2 д) 1,5-дибромпентан 3. Составьте уравнения реакций взаимодействия: (5 баллов) а) бутадиена-1,3 с хлором (1-я стадия) б) бутена-1 с бромоводородом в) бутина-2 с бромом (1-я стадия) г) дегидрирования этана д) нитрования бензола Вариант №2 Часть I. 1. Общая формула алкенов:
2. Молекулы алкинов содержат:
3. Угол связи в молекуле метана:
4. В какой молекуле угол связи равен 1200?
5. Тип гибридизации атомов углерода в молекуле ацетилена:
6. Чем отличается друг от друга бутен-1 и бутен-2:
7. Взаимодействие метана с хлором – это реакция:
8. Реакция гидрирования: а) С2Н6 + О2 →; в) С2Н4 + Н2О →; б) С3Н8 →; г) С2Н4 + Н2 → 9. 2 - метилбутен -1 не взаимодействует:
10. Характерные для алкинов реакции, обусловленные наличием двух π- связей в молекулах, относятся к типу реакции:
11. С раствором перманганата калия реагирует
12. Основной целью крекинга нефтепродуктов является получение
Часть II. 1. Составьте формулы четырех изомеров гептана, назовите их. (4 балла) 2. Составьте формулы по названиям: (4 балла) а) 1,2,4-триметилбензол б) 3-бром-2,2-диметилгексан в) 3-метилбутин-1 г) 2,4-диметилпентадиен-2,3 д) 2-хлор-3,3-диэтилгексан 3. Составьте уравнения реакций взаимодействия: (5 баллов) а) бромирования этана (1стадия) б) гидратации пропилена в) хлорирования бутена-2 г) горения метана д) гидрирования бензола Вариант №3 Часть I. 1. Углеводород С7Н8 относится к классу:
2. Обая формула алкинов:
3. Молекулы алканов содержат:
4. Угол связи в молекуле этилена:
5. Тип гибридизации атомов углерода в молекуле бензола:
6. Пропин и пропадиен – это:
7. Взаимодействие метана с хлором – это реакция:
8. При дегидратации этилового спирта образуется:
9. С раствором перманганата калия не реагирует
10. При взаимодействии пропена с хлором образуется
11. Органическим веществом, при пропускании которого через бромную воду раствор обесцвечивается, является
12. Термическое разложение мазута называется
Часть II. 1. Составьте формулы четырех изомеров пентина, назовите их. (4 балла) 2. Составьте формулы по названиям: (4 балла) а) 2-бром-2-этилпентан б) 3-хлор-2,2-диметилгексан в) 2-пропилпентадиен-1,4 г) 2,4-дибромпентен-2 д) 1,4-диметилбензол 3. Составьте уравнения реакций взаимодействия: (5 баллов) а) 2-хлорбутадиеном-1,3 и хлором (1-я стадия) б) бутеном-1 и водой в) пентаном и кислородом (горение г) нитрования толуола д) этилена с раствором КMnO4 Вариант №4 Часть I. 1. Общая формула аренов:
2. Молекулы алкенов содержат:
3. Угол связи в молекуле ацетилена:
4. Тип гибридизации атомов углерода в молекуле метана:
5. Соединение, имеющее название 2, 3, 3 - триметилпентан, имеет молекулярную формулу:
6. Реакция дегидрирования: а) С2Н6 + О2 →; в) С2Н4 + Н2О →; б) С3Н8 →; г) С2Н4 + Н2 → 7. Какой тип реакции характерен для алканов:
8. При гидратации этилена образуется:
9. Полиэтилен получают, используя реакцию
10. В уравнении полного сгорания этана коэффициент перед формулой кислорода равен а) 7 б) 8 в) 6 г) 9 11. Бензиновая фракция перегонки нефти содержит:
12. Основным компонентом природного газа является
Часть II. 1. Составьте формулы четырех изомеров пентена, назовите их. (4 балла) 2. Составьте формулы по названиям: (4 балла) а) 1-метил-3-этилбензол б) 2,3-дибромпентадиен-1,4 в) 2,4-диметил-2,4-диэтилгексан г) 2-бром-3-метилбутан д) 3-метилбутин-1 3. Составьте уравнения реакций взаимодействия: (5 баллов) а) горения этана б) этилена с хлороводородом в) тримеризации ацетилена г) бутена-1 с водой д) толуола с азотной кислотой. |
