ЛЕКЦИИ 50 лекций по хирургии под редакцией академика B.C. Савельева. ЛЕКЦИИ 50 лекций по хирургии под редакцией академика B.C. Савель. Media medica 2003 п од редакцией академика B. C. Савельева
 Скачать 9.44 Mb. Скачать 9.44 Mb.
|
|
Клиническая семиотика ХПЭЛГ легко заподозрить при наличии анамнестических указаний на острый тромбоз вен нижних конечностей, осложненный ТЭЛА. Следует учитывать такие признаки массивной легочной эмболии, как приступ удушья, боли в грудной клетке (за грудиной или в области сердца), коллапс, кратковременную потерю сознания, кашель с кровохарканьем. К сожалению, интерпретация анамнестических сведений довольно часто представляет значительные трудности. Клинические проявления постэмболической легочной гипертензии зачастую мало специфичны и могут наблюдаться при различных заболеваниях сердца и легких. Основным, а иногда и единствен- ным симптомом заболевания является прогрессирующая одышка. Выраженность физикальных изменений определяется объемом поражения артериального русла малого круга кровообращения, степенью легочной гипертензии, тяжестью нарушений газообмена и функциональным статусом правого желудочка сердца. Отсутствие клиники посттромботической болезни нижних конечностей не исключает данную патологию. Можно выделить комплекс клинических признаков, который позволяет с большой долей вероятности предположить ее наличие. Необходимо принимать во внимание следующее:
Окончательный диагноз можно поставить только с помощью применения специальных методов исследования. Топическая диагностика постэмболических поражений легочных артерий При определении показаний к хирургическому лечению необходимо иметь достоверные сведения о локализации постэмболической обструкции легочных артерий, объеме их поражения и проходимости дистального сосудистого русла. Только располагая подобной информацией, можно выбрать наиболее рациональную методику проведения реконструктивного оперативного вмешательства. Основным методом выявления окклюзионно-стенотических изменений легочных артерий клиницистами признана ангиопульмонография. Любое указание на наличие центральной формы ХПЭЛГ диктует необходимость ее выполнения. Вопрос о возможности проведения рентгеноконтра-стного исследования решается после катетеризации полостей сердца и оценки выраженности ге-модинамических нарушений. Использование полипозиционных методик позволяет повысить точность и информативность ангиографического заключения. Большими разрешающими возможностями в диагностике хронических постэмболических поражений крупных легочных артерий обладает компьютерная томография. Ее производят после интравенозного введения рентгеноконтрастного препарата. Этот метод можно использовать как в качестве дополнения к ангиографическому исследованию, так и самостоятельно, особенно у больных с тяжелой гипертензией малого круга кровообращения. Определенное диагностическое значение имеет обнаружение во время зондирования сердца градиента систолического давления между легочным стволом и дистальными сосудами легких, ко- 101 сердечно-сосудистая хирургия   Рис. 2. Постэмболическое поражение ствола и правой легочной артерии. Ангиопульмоно-грамма (а) и кривая давления (б) при постэмболическом стенозе правой легочной артерии. Имеется выраженный градиент давления между легочным стволом и правой верхнедолевой ветвью легочной артерии. Рис. 2. Постэмболическое поражение ствола и правой легочной артерии. Ангиопульмоно-грамма (а) и кривая давления (б) при постэмболическом стенозе правой легочной артерии. Имеется выраженный градиент давления между легочным стволом и правой верхнедолевой ветвью легочной артерии.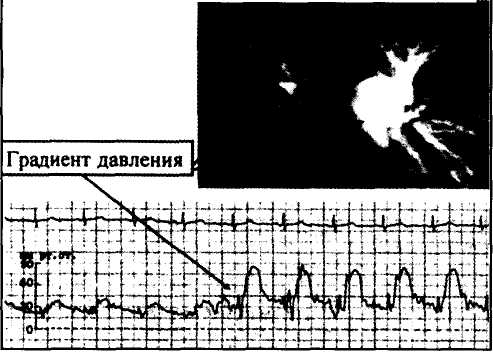 торый обусловлен выраженным постэмболическим стенозом (рис.2). В диагностическом арсенале должны находиться также и неинвазивные методики, позволяющие ориентировочно судить о состоянии легочно-ар-териального русла, которые можно использовать и в амбулаторных условиях. Безопасным исследованием считается радионуклидное перфузионное сканирование, которое следует применять у всех больных с подозрением на ХПЭЛГ. Отсутствие характерных перфузионных нарушений исключает эмболическую причину хронического легочного сердца. К сожалению, сканирование позволяет поставить точный диагноз только при окклюзивном поражении сосудов. Метод имеет существенные диагностические ограничения в выявлении постэмболических стенозов легочного ствола и его главных ветвей. Между тем полученные результаты дают возможность правильно планировать проведение рентгеноконтрастного исследования, направляя внимание рентгенангиолога в нужном направлении. В ряде случаев получить прямое изображение тромбов в просвете легочного ствола и его центральных ветвей позволяет двухмерная эхокардио-графия. Ее всегда необходимо дополнять доппле-рографией, которая дает дополнительную информацию. В частности, она позволяет уловить изменения спектральных характеристик кровотока в зонах расположения тромбов и подтвердить сте-нотический характер их поражения. Перспективным методом, позволяющим определить проксимальную границу постэмболической окклюзии, представляется фиброангиопульмо-носкопия. Она дает возможность провести прямой осмотр сосудистого русла легких. Для визуализации анатомических структур в потоке крови используется принцип осмотра артерий через прозрачный баллончик на торце прибора, который заполняется физиологическим раствором. Ставя вопрос о возможности выполнения хирургической дезобструкции легочных артерий, желательно иметь информацию о протяженности тромботической окклюзии. В случае облитерации дистального сосудистого русла, оперативное вмешательство обречено на неудачу. Оценить проходимость сегментарных легочных артерий и их разветвлений можно с помощью бронхиальной ар-териографии и бронхиального ангиоскани-рования В отдельных случаях приходится прибегать к проведению биопсии легкого с целью получения гистологических данных о выраженности структурных изменений периферической сосудистой сети. В ближайшем будущем предстоит оценить диагностические возможности спиральной компьютерной томографии, магнитно-резонансной томографии и многопроекционного сверхбыстрого компьютерного томографического сканирования. Диагностический алгоритм В оптимальном варианте специальные диагностические исследования должны применяться в такой последовательности. Сначала необходимо произвести эхолокацию легочного ствола и его ветвей, затем перфузионное сканирование легких. По результатам радиоизотопного исследования судят о необходимости ангиопульмонографии. Ее применяют при отсутствии выраженной контрак-тильной недостаточности правого желудочка. При сомнениях в ангиографическом диагнозе следует прибегать к рентгеновской компьютерной томографии с контрастированием сосудов, а в отдельных случаях, когда решается вопрос о хирургическом вмешательстве, и к прямому осмотру легочных артерий с помощью ангиоскопа. Для определения состояния периферического русла легких дисталь-нее места окклюзии желательно выполнить бронхиальную артериографию и ангиосканирование. Лечение Единственным радикальным методом лечения ХПЭЛГ является реконструктивное хирургическое вмешательство, восстанавливающее проходимость васкулярного русла, что приводит к снижению давления в малом круге кровообращения. В отдельных случаях выполнима транслюминальная баллонная ангиопластика ограниченных легочных стенозов. При неэффективности медикаментозной терапии, с целью гемодинамической разгрузки правых отделов сердца, используют непрямую атриосептосто-мию. Прямые оперативные вмешательства Первая успешная тромбэктомия из легочной артерии при ее хронической окклюзии была сделана P. Allison в 1958 г. [5]. Работами, опубликованными в 70-е и последующие годы, была доказана эффективность хирургического восстановления проходимости крупных легочных артерий при их постэмболической окклюзии [2, 6-10]. Суммарный мировой хирургический опыт составляет несколько сотен оперативных вмешательств, сделанных преимущественно с применением экстракорпорального кровообращения. Успех хирургических вмешательств, выполняемых в отдаленном постэмболическом периоде, зависит в основном от таких факторов, как длительность заболевания, уровень гипертензии, выраженность недостаточности правого желудочка и состояние дистального легочно-артериального русла. Дезобструкция может закончиться удачно при уровне систолического легочно-артериального 102 сердечно-сосудистая хирургия  давления не выше 100 мм рт. ст. Тромбинтимэкто-мия не представляет значительной технической сложности при сроке постэмболической окклюзии не более 18 мес. Выполнение ее возможно также и в сроки от 2 до 3 лет с момента эмболии. При большей длительности заболевания адекватно восстановить проходимость артериальных магистралей легких, как правило, не удается. давления не выше 100 мм рт. ст. Тромбинтимэкто-мия не представляет значительной технической сложности при сроке постэмболической окклюзии не более 18 мес. Выполнение ее возможно также и в сроки от 2 до 3 лет с момента эмболии. При большей длительности заболевания адекватно восстановить проходимость артериальных магистралей легких, как правило, не удается.По абсолютным показаниям оперативное вмешательство следует проводить больным с постэмболической окклюзией легочного ствола и/или его главных ветвей на фоне относительной компенсации сердечной деятельности, если уровень систолического давления в малом круге превышает 50 мм рт. ст. Длительность заболевания не должна быть более 3 лет. По относительным показаниям тромбинтимэк-томия может выполняться из главных и долевых артерий при I степени легочной гипертензии с целью профилактики развития тяжелых гемодинами-ческих расстройств в малом круге кровообращения, которые могут развиваться у ряда больных при естественном течении заболевания. Абсолютными противопоказаниями к операции мы считаем наличие: 1) периферической формы легочной гипертензии; 2) декомпенсированного легочного сердца у больных с проксимальной локализацией окклюзии; 3) вторичных необратимых органических изменений со стороны всего сосудистого русла малого круга и паренхимы легких; 4) тяжелых сопутствующих заболеваний. К относительным противопоказаниям относится выраженное ожирение. Выбор метода операции При обтурации легочных артерий организованными тромбами, плотно приросшими к стенке сосуда и покрытых неоинтимой, произвести дезобст-рукцию в условиях временной окклюзии полых вен, как это делается у больных с острой тромбоэмболией, технически невозможно. Без искусственного кровообращения, временно пережимая пораженную легочную артерию, можно оперировать больных только при одностороннем поражении сосудов, уровне систолического легочно-артери-ального давления не более 60—70 мм рт. ст. и отсутствии контрактильной недостаточности правого желудочка. При этом всегда следует иметь в виду, что во время вмешательства могут встретиться непредвиденные трудности, связанные, как правило, с ошибками в оценке локализации постэмболического поражения. Необходимость в применении экстракорпоральной перфузии возникает при постэмболическом поражении легочного ствола или обеих его главных ветвей, а также в случаях отсутствия точных данных о локализации окклюзии. Тромбинтимэктомию можно производить из срединного стернального доступа через легочный ствол, при этом, как правило, удается освободить просвет только центральных легочных артерий. Поэтому более рационально использовать дополнительный трансперикардиальный подход к долевым легочным артериям (рис.3) для выполнения дезобструкции на уровне периферического сосудистого русла легких. С целью контроля массивного ретроградного кровотечения из бронхиальных артерий необходимо применять глубокую гипотермию с прерывистой экстракорпоральной пер- фузией. Преимущества такого методического подхода очевидны: 1) тромбэктомия выполняется на «сухом» операционном поле; 2) не надо обходить со всех сторон сосуды в местах проведения дополнительных артериотомий — достаточно освободить только переднюю их полуокружность; 3) возможен прямой визуальный и ангиоскопический (с помощью фиброволоконной оптики) контроль состояния периферического артериального русла в процессе операции. Техника тромбинтимжтомии в условиях глубокой гипотермии с прерывистой экстракорпоральной перфузией Грудную клетку вскрывают путем продольной стернотомии. Подключают АИК. Начинают экстракорпоральную перфузию и охлаждение больного. При наступлении асистолии накладывают зажим на аорту и в корень ее вводят охлажденный кардио-плегический раствор, который эвакуируют через вскрытое правое предсердие. Сердце обкладывают мелко истолченным льдом. Сразу же проводят осмотр межпредсердной перегородки на предмет выявления в ней дефектов. Основной этап оперативного вмешательства начинают с продольного рассечения передней стенки легочного ствола и ревизии центральных легочных артерий. При невозможности осуществления радикальной дезобструкции через артериотомию на легочном стволе продолжают охлаждать пациента до температуры в прямой кишке 18-20°С. По достижению этой температуры прекращают искусственное кровообращение на 20 мин. Собрав кровь в оксигенатор, пережимают венозную магистраль. Через дополнительные артериотомические отверстия производят дезобструкцию долевых и сегментарных ветвей. Техническая сложность вмешательства диктует необходимость продольного вскрытия артерий. Перед выполнением дезобструкции необходимо точно идентифицировать артериальную стенку, чтобы избежать расслоения и сквозного повреждения сосуда при удалении фиброзно трансформированного и эндотелизированного тромба. Ушить такой дефект артерии крайне сложно. Тромбинти- Р  ис. 3. Тромбинтимэктомия из легочных артерий. Этапы оперативного вмешательства. ис. 3. Тромбинтимэктомия из легочных артерий. Этапы оперативного вмешательства.а — после рассечения перикарда над корнем легкого выделяются долевые артерии; б — артериотомий выполняют в зонах, указанных на схеме;  в — при выраженных изменениях сосудистой стенки для закрытия артериотомий применяется боковая пластика легочной артерии «заплатой» из ау-то- или ксеноперикарда. 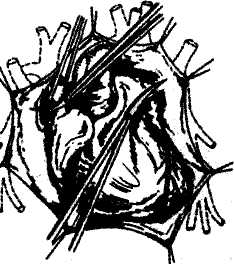  103 103сердечно-сосудистая хирургия мэктомию производят острым путем с использованием специальных сосудистых инструментов. В отдельных случаях удается удалить плотные тромбы, представляющие собой слепки сосудов, целиком. При большом объеме реконструкции сосудов приходится на 10-15 мин восстанавливать экстракорпоральную перфузию. После завершения тромбинтимэктомии дефекты в стенках артерий зашивают. Можно накладывать непрерывный обвивной синтетический шов. С целью профилактики прорезывания швов и стеноза артерии в зоне их наложения целесообразно прибегать к боковой пластике сосудов заплатами из ау-то- или ксеноперикарда (рис. 3). В случае необходимости выполняют различные оперативные вмешательства на сердце. Тщательная дезобструкция легочного артериального русла обеспечивает не только успешный исход операции, но и хороший ее функциональный результат. При правильном отборе больных на операцию и использовании усовершенствованных методик выполнения тромбинтимэктомии, в частности из сегментарных легочных артерий, удается значительно снизить послеоперационную летальность (до 8,7%) и улучшить гемодинамический итог сосудистой реконструкции [9]. Эндоваскулярные вмешательства При ХПЭЛГ иногда используют транслюми-нальную баллонную ангиопластику, которая применяется для коррекции различных типов врожденных стенозов легочных артерий. По нашему мнению, метод должен входить и в арсенал современного лечения этого патологического состояния. Показанием к нему служит наличие стеноза мембранозного типа на уровне главных и долевых легочных артерий при отсутствии тяжелых гемо-динамических расстройств в малом круге кровообращения. Об эффективности вмешательства свидетельствует исчезновение или существенное снижение градиента систолического давления в зоне ангиопластики. Проводя повторное контрастирование легочных артерий, можно убедиться в эффективности эндоваскулярного вмешательства. Трансвенозная катетерная атриосептосто-мия позволяет осуществить декомпрессию правых отделов сердца в случаях развития миокардиаль-ной недостаточности, рефрактерной к медикаментозной терапии. У больных с терминальной легочной гипертензией она является паллиативным и единственно возможным методом хирургического лечения, позволяющим продлить их жизнь за счет снижение давления в правых камерах сердца. Эта эндоваскулярная операция показана больным с III—IV степенью легочной гипертензии, низким минным выбросом (сердечный индекс < 2,0 л/ мин/м^ и уровнем правожелудочкового конечного диастолического давления, превышающим 20 мм рт. ст. Непременными условиями ее проведения служат отсутствие недостаточности левого желудочка и положительный градиент давления между правым и левым предсердиями. Одним из ключевых моментов этого вмешательства является транссептальная пункция. Вопрос о возможности проведения атриосептостомии решают после регистрации внутрисердечного давления. Межпредсердную перегородку рассекают сеп-тотомом Парка. Созданное отверстие в области овальной ямки расширяют 2-х просветным баллонным катетером Грюнцига до 1,5-2 см. При этом уменьшается или исчезает градиент давления между правым и левым предсердиями. Ультразвуковая эхолокация сердца позволяет оценить истинные размеры сформированного соустья. Неблагоприятным последствием этой операции является нарастание артериальной гипоксемии. Консервативное лечение Возможности фармакологической терапии ХПЭЛГ невелики. Не следует отказываться от тром-болитической терапии, если есть подозрение на развитие «свежего» продолженного тромбоза в по-стэмболически измененном сосудистом русле легких. Можно применять различные периферические вазодилататоры, однако назначение этой группы препаратов не влияет на продолжительность жизни больных. При высокой активности ренин-ангиотензин-альдостероновой системы показано применение блокаторов ангиотензинпревращаю-щего фермента. Гипотензивным действием на малый круг кровообращения обладают антагонисты кальция. В комплекс консервативной терапии в обязательном порядке должны входить средства нормализующие гемостаз и реологию крови. В случае гиперкоагуляции показан длительный перо-ральный прием непрямых антикоагулянтов. Медикаментозную коррекцию декомпенсированного легочного сердца следует проводить по общепринятым терапевтическим канонам. Для купирования реологических расстройств при ХПЭЛГ также используют метод квантовой гемотерапии — инфузии небольших количеств ауто-крови, облученной ультрафиолетовыми лучами. За счет биофизического воздействия происходит снижение вязкости и повышение оксигенации крови. Курс терапии состоит из 3—5 процедур, выполняемых в течение двух недель. После их проведения в большинстве наблюдений наступает видимый клинический эффект, что обусловлено нормализацией текучих свойств крови и возрастанием объемного кровотока в большом и малом кругах кровообращения. Заканчивая эту лекцию, следует констатировать, что хирургическая дезобструкция сосудов, предпринимаемая при центральной форме ХПЭЛГ своевременно и выполняемая в полном объеме, позволяет добиться регрессии сердечно-легочной недостаточности. Вместе с тем только за счет этих мер данная проблема не может быть решена. Необходимо изыскивать пути улучшения диагностики и лечения тромбоэмболии на ранних стадиях заболевания. Еще лучше предотвращать ТЭЛА с помощью различных профилактических мер. Если массивная легочная эмболия все же возникла, то после проведения курса тромболитической терапии такие больные должны находиться на диспансерном наблюдении. В случае отсутствия восстановления легочной перфузии в течение 3—6 месяцев необходимо чаще прибегать к хирургическому лечению, чтобы предотвратить развитие декомпенсированного хронического легочного сердца. В перспективе, у пациентов с распространенной облитерацией дистального сосудистого русла малого круга кровообращения, которую невозможно устранить оперативным путем, видимо, следует прибегать к пересадке сердечно-легочного комплекса. 104 сердечно-сосудистая хирургия  Литература Литература
Surg, 1986.- Vol. 20.- N4.- С 67-70.
 Эндоваскулярная хирургия: возможности и перспективы Эндоваскулярная хирургия: возможности и перспективыВ.И.Прокубовский, С.А.Капранов  Рентгенохирургия (РХ), возникшая на стыке хирургических дисциплин и рентгенологии, в последние 30 лет стала самостоятельным направлением клинической медицины. Она объединяет эндоваскулярную хирургию (ЭХ), чре-скожные вмешательства на желче- и мочевыводя-щих путях, стентирование трахеи, бронхов, пищевода, толстой кишки, проведение ортопедических операций и удаление инородных тел под контролем рентгеноскопии и др. |
