Учебнометодическое пособие для студентов i курса медицинского вуза Рекомендовано Учебнометодическим объединением по медицинскому и фармацевтическому образованию вузов России в качестве учебного пособия для студентов медицинских вузов
 Скачать 5.49 Mb. Скачать 5.49 Mb.
|
Учебно-исследовательская лабораторная работа «Химическое равновесие»Цель работы: изучить влияние на смещение химического равновесия изменения концентрации реагирующих веществ, температуры, среды раствора. Опыт № 1. Влияние концентрации реагирующих веществ на смещение химического равновесияОборудование: штатив с пробирками. Реактивы: дистиллированная вода, насыщенные растворы: хлорида железа (III), роданида аммония, хлорида аммония. Порядок выполнения работы1. В пробирку налейте 10,0 мл воды и прибавьте по одной капле насыщенных растворов FeCl3 и NH4SCN. 2. Содержимое пробирки разделите на 4 части. К первой – добавьте одну каплю насыщенного раствора FeCl3, ко второй – три капли насыщенного раствора NH4SCN, в третью – три капли насыщенного раствора NH4Cl, четвертую оставьте для сравнения. Результаты опыта внесите в таблицу. Таблица
Составьте уравнение реакции, лежащей в основе опыта в молекулярном и ионном виде. Запишите математическое выражение константы равновесия для данной реакции. Сделайте вывод о влиянии концентрации реагирующих веществ на сдвиг химического равновесия. Опыт № 2. Влияние температуры на смещение химического равновесияОборудование: штатив с пробирками, спиртовка. Реактивы: раствор крахмала, 0,1 н. раствор йода. При взаимодействии йода с крахмалом образуется окрашенное в синий цвет адсорбционное соединение. Упрощенно образование его можно представить схемой:  йод + крахмал йодокрахмал. йод + крахмал йодокрахмал. Порядок выполнения работыВ две пробирки поместите по 5,0 мл раствора крахмала и добавьте в каждую 3-4 капли 0,1 н. раствора йода. Отметьте внешний признак реакции. Одну пробирку оставьте для сравнения. Содержимое второй пробирки нагрейте с помощью спиртовки, отметьте изменение окраски, затем охладите под струей воды до восстановления первоначальной окраски. Укажите направление смещения равновесия изучаемой реакции при повышении температуры. Сделайте вывод о тепловом эффекте реакции образования йодокрахмала. Опыт № 3. Влияние среды раствора на смещение химического равновесияОборудование: штатив с пробирками. Реактивы: 0,5 н. раствор дихромата калия, 0,5 н. раствор NaOH, 0,5 н. раствор H2SO4. В растворах, содержащих Cr(VI), осуществляется равновесие: Cr2O 72 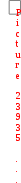 H 2O H 2O  2CrO 24 2CrO 24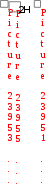 бихромат-ион хромат-ион (оранжевый) (желтый) В щелочной среде образуется хромат-ион, в кислой – бихроматион. Порядок выполнения работыВ две пробирки налейте по 1 мл раствора K2Cr2O7. Одну пробирку оставьте для сравнения, а во вторую добавьте по каплям раствор щелочи до изменения окраски. В эту же пробир- ку затем по каплям добавьте раствор H2SO4 до получения первоначальной окраски. Составьте молекулярные уравнения взаимодействия: а) дихромата калия с гидроксидом натрия; б) хромата калия с серной кислотой. Объясните причину изменения окраски раствора при действии щелочи и кислоты с точки зрения принципа Ле Шателье. План оформления отчета 1. Дата и название работы. Цель работы. Краткое описание проведения опыта. Результаты полученных опытных данных. Выводы по работе. Контрольные вопросы для защиты экспериментальной работыКакие реакции называют: а) необратимыми, б) обратимыми? Одинаковы или различны значения констант скоростей для прямой и обратной реакции? Объясните. Как изменяются скорости прямой и обратной реакций во времени от начала реакции? Чем это обусловлено и в какое состояние приводит данную систему? Что называют химическим равновесием? Почему оно является динамическим? Какие концентрации реагирующих веществ называют равновесными? Что называют константой химического равновесия? Зависит ли это величина от природы реагирующих веществ, их концентрации, температуры, давления? Объясните, почему числовое значение константы равновесия определяет глубину превращения исходных веществ в продукты реакции. Если константа скорости прямой реакции много меньше константы скорости обратной реакции, то как это влияет на числовое значение константы равновесия и выход продуктов реакции? 8. Почему в выражение для скорости химической реакции или константы равновесия не входят концентрации веществ, находящихся в твердой фазе? Какой процесс называют смещением химического равновесия? На конкретных примерах покажите, как смещается равновесие системы под влиянием изменения: а) концентрации одного из реагирующих веществ, б) температуры, в) давления. Какими параметрами характеризуется химическое равновесие? К чему приводит изменение одного из параметров? Почему катализатор не влияет на тепловой эффект реакции и не смещает химического равновесия? Какое уравнение выражает связь константы равновесия с основными термодинамическими характеристиками?  Задачи для самостоятельного решенияВ организме человека реакция окисления этилового спирта протекает в две стадии. Первая – окисление этилового спирта до уксусного альдегида: С 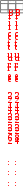 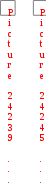 2Н5ОН(ж)+ 2Н5ОН(ж)+Вторая – окисление уксусного альдегида до уксусной кислоты: 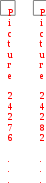 СН3СНО(р-р)+ СН3СНО(р-р)+ Р 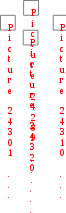 ассчитайте Нор-ции окисления этанола до уксусной кислоты. Ответ: Нор-ции = 493 кДж/моль. ассчитайте Нор-ции окисления этанола до уксусной кислоты. Ответ: Нор-ции = 493 кДж/моль. Р  ассчитайте Нор-ции сгорания этанола, если известно, что при сгорании 4,6 г спирта выделяется 137 кДж теплоты. Ответ: Нор-ции = 1370 кДж/моль. ассчитайте Нор-ции сгорания этанола, если известно, что при сгорании 4,6 г спирта выделяется 137 кДж теплоты. Ответ: Нор-ции = 1370 кДж/моль. В организме человека в результате метаболизма образуется глицерин, который далее окисляется в СО2(г) и Н2О(ж). Вычислите G Какое количество теплоты поглотится при растворении в воде 2 Д  АМФ + Н2О; Gор-ции = 14 кДж/моль. В каком направлении реакция идет самопроизвольно при стандартных условиях? Каково значение константы равновесия? Ответ: в обратном направлении; K = 3,5210–3. АМФ + Н2О; Gор-ции = 14 кДж/моль. В каком направлении реакция идет самопроизвольно при стандартных условиях? Каково значение константы равновесия? Ответ: в обратном направлении; K = 3,5210–3. В  заимодействует ли алюминий с водой? Нет ли опасности, что изделия из алюминия, широко применяемые в быту и медицинской технике, будут разрушаться под действием воды в результате протекания реакции: 2Al(т)+6Н2О(ж) 3Н2(г)+2Al(ОН)3(т). Надо ли слишком тщательно чистить алюминиевые изделия? Ответ: G 0, однако защитный слой Al2O3 предохраняет алюминий от разрушения. заимодействует ли алюминий с водой? Нет ли опасности, что изделия из алюминия, широко применяемые в быту и медицинской технике, будут разрушаться под действием воды в результате протекания реакции: 2Al(т)+6Н2О(ж) 3Н2(г)+2Al(ОН)3(т). Надо ли слишком тщательно чистить алюминиевые изделия? Ответ: G 0, однако защитный слой Al2O3 предохраняет алюминий от разрушения. В 100 г трески в среднем содержится 11,6 г белков и 0,3 г жиров. Рассчитайте (в кДж и ккал) энергию, которая выделится при усвоении порции трески массой 228 г. Калорийность белков 17,1 кДж/г, а жиров – 38,8 кДж/г. Ответ: 478,8 кДж; 114,5 ккал. Теплоты сгорания углеводов и белков в организме человека составляют 4,1 ккал/г, жиров 9,3 ккал/г. Среднесуточная потребность в белках, жирах и углеводах для студента составляет соответственно 113, 106 и 451 г. Найдите суточную потребность в энергии у студентов. Ответ: 3300 ккал. Р Н Рассчитайте массу углеводов, необходимую для восполнения энергии, затраченной при выделении 800 г воды через кожу, если для испарения 1 моль воды через кожу требуется 40,7 кДж. Ответ: 105,7 г. При растворении одного моль H2SO4 в 800 г воды температура повысилась на 22,4 К. Определите энтальпию растворения Н2SO4, принимая во внимание удельную теплоемкость раствора равной 3,76 Дж/г·К. Ответ: –75,6 кДж/моль. О Сравните стандартные энергии Гиббса полного аэробного окисления глюкозы: и неполного анаэробного гидролиза до молочной кислоты: | OH Какой процесс является более эффективным с точки зрения использования глюкозы? Ответ: реакция (1) более эффективна. Предположим, что платье, в котором вы вымокли, впитало 1 кг воды и холодный ветер его высушил. Какое количество потерянный теплоты необходимо возместить организму? Сколько г глюкозы нужны потребить, чтобы восполнить эту потерю? Принять мольную энтальпию парообразования воды равной 44 кДж/моль. Ответ: mглюкозы = 157 г, Q = 2444,4 кДж. По стандартным теплотам сгорания веществ рассчитайте энтальпию синтеза уксусноэтилового эфира: С2Н5ОН(ж) + СН3СООН(ж)  СН3СООС2Н5(ж) + Н2О(ж), если СН3СООС2Н5(ж) + Н2О(ж), если Н Используя стандартные энтальпии образования вычислите, сколько теплоты выделится при разложении 54 г глюкозы по реакции: С6Н12О6(к)=2С2Н5ОН(ж)+2СО2(г). Ответ: 20,76 кДж. Н  АД+ и НАДН – окисленная и восстановленная формы никотинамидадениндинуклеотида Gореакции окисления НАДН: АД+ и НАДН – окисленная и восстановленная формы никотинамидадениндинуклеотида Gореакции окисления НАДН: НАДН + Н+ НАД+ + Н2 р Ферментативная реакция дегидрирования пропанола-2 протекает по уравнению: СН3–СН–СН3(р-р)  СН3–С–СН3(р-р) + Н2(г) СН3–С–СН3(р-р) + Н2(г) | || ОН О О  В печени протекает ферментативный обратимый процесс:  глюкозо-1-фосфат глюкозо-6-фосфат. глюкозо-1-фосфат глюкозо-6-фосфат. При 37оС равновесная концентрация глюкозо-1-фосфат 0,001 моль/л, а глюкозо-6-фосфат – 0,019 моль/л. Рассчитайте Kравн. Ответ: Kравн. = 19. В  АДФ + Фн, в условиях, характерных для мышечной клетки, находящейся в состоянии покоя: [АТФ] = 0,005 моль/л; [АДФ] = 0,0005 моль/л; [Фн] = 0,005 моль/л; рН = 6,0, t = 25оС. Константа реакции гидролиза при указанной температуре равна 8,92104. Ответ: G = –46,09 кДж. АДФ + Фн, в условиях, характерных для мышечной клетки, находящейся в состоянии покоя: [АТФ] = 0,005 моль/л; [АДФ] = 0,0005 моль/л; [Фн] = 0,005 моль/л; рН = 6,0, t = 25оС. Константа реакции гидролиза при указанной температуре равна 8,92104. Ответ: G = –46,09 кДж. В загрязненном воздухе содержится примесь CO, которая образуется при неполном сгорании твердого топлива и при работе двигателей внутреннего сгорания. Монооксид углерода медленно окисляется кислородом воздуха до диоксида углерода. При определенных условиях скорость такой реакции составляет 0,05 моль/(лс), а концентрация CO2 становится равной 0,2 моль/л. Рассчитайте концентрацию CO2 через 10 с после указанного момента. Ответ: 0,7 моль/л. П ричиной образования опасного для здоровья тумана – "смога" – считают большое количество выхлопных газов автомобилей при высокой влажности воздуха. В смоге присутствует ядовитый диоксид азота, который получается по реакции монооксида азота с атомарным кислородом. Рассчитайте скорость этой реакции, если через 5 минут после ее начала концентрация диоксида азота стала равна 0,05 моль/л, а через 20 минут – 0,08 моль/л. Ответ: 3,310–5 моль/лс. Н 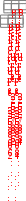 апишите выражение констант равновесия для обратимых реакций по равновесным концентрациям и парциальным давлениям: 4HCl(г) + О2(г) 2Н2О(г) + 2Сl2(г); FeO(т) + Н2(г) Fe(т) + Н2О(г). апишите выражение констант равновесия для обратимых реакций по равновесным концентрациям и парциальным давлениям: 4HCl(г) + О2(г) 2Н2О(г) + 2Сl2(г); FeO(т) + Н2(г) Fe(т) + Н2О(г). Во время аварии на Чернобыльской АЭС (1986) среди других радионуклидов произошел выброс Cs-137. Какая часть этого радионуклида, попавшего в организм пострадавших, осталась в нем до настоящего времени? Ответ: 59%. В каком направлении сместится равновесие в обратимых системах: N 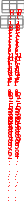 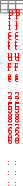 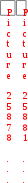  2 + O2 2NO – 180 кДж; 2СО + О2 2СО2; Н < 0; CаCО3 CаО + СО2; Н > 0, при: 2 + O2 2NO – 180 кДж; 2СО + О2 2СО2; Н < 0; CаCО3 CаО + СО2; Н > 0, при: а) повышении температуры; б) повышении давления. К   ак необходимо изменить температуру, давление и концентрацию веществ, чтобы увеличить выход хлора в реакции: 4НСl(г) + О2(г) 2Н2О(г) + Cl2(г), Н < 0? ак необходимо изменить температуру, давление и концентрацию веществ, чтобы увеличить выход хлора в реакции: 4НСl(г) + О2(г) 2Н2О(г) + Cl2(г), Н < 0? В  ычислите константу равновесия и исходные концентрации йода и водорода в системе: Н2 + I2 2HI, если в состоянии равновесия концентрации веществ равны: ычислите константу равновесия и исходные концентрации йода и водорода в системе: Н2 + I2 2HI, если в состоянии равновесия концентрации веществ равны: [I2] = 0,025 моль/л; [Н2] = 0,004 моль/л; [НI] = 0,35 моль/л. Ответ: Kравн = 5916, с(I2) = 0,2 моль/л; c(Н2) = 0,179 моль/л. Теоретические вопросы к контрольной работе по модулю «Основы химической термодинамики, химической кинетики и равновесия»для студентов лечебного и педиатрического факультетов Основные понятия химической термодинамики: Система, системы гомогенные и гетерогенные, системы открытые, закрытые и изолированные. Параметры системы: интенсивные, экстенсивные, функции состояния. Состояние системы равновесное, стационарное, переходное. Термодинамические процессы: изобарические, изохорические, изотермические. Внутренняя энергия, работа, теплота, связь между ними. I начало термодинамики: определение, математическое выражение для изолированных и закрытых систем, биологическое значение. Закон Гесса: формулировка, определение теплового эффекта реакции по энтальпиям образования и энтальпиям сгорания; значение для термохимических расчетов. Энтальпия реакции, процессы экзо- и эндотермические; стандартные энтальпии образования простых и сложных веществ. Энтальпия сгорания. Э  нтропия: определение, смысловое значение, факторы, влияющие на ее величину; определение S в химических реакциях при с.у. нтропия: определение, смысловое значение, факторы, влияющие на ее величину; определение S в химических реакциях при с.у. II закон термодинамики: сущность, формулировка, математическое выражение для изолированных систем. Энергия Гиббса как обобщенная термодинамическая функция, ее применение для прогнозирования возможности и предела самопроизвольного протекания процессов. Особенности живых организмов как открытых систем: стационарное состояние, принцип И. Пригожина, поддержание состояния гомеостаза. Особенности биохимических процессов в организме: принцип энергетического сопряжения, многостадийность, обратимость. Основные понятия химической кинетики: Реакции гомогенные, гетерогенные, математическое выражение скорости гомогенных и гетерогенных реакций, скорость средняя и истинная, единицы измерения, примеры; Реакции простые и сложные: последовательные, параллельные, последовательно-параллельные, циклические, примеры. Факторы, влияющие на скорость гомогенных реакций: природа, концентрация реагентов, температура, катализаторы. Закон действующих масс, кинетические уравнения реакций, физический смысл константы скорости реакции. Понятие о молекулярности и порядке реакции. Энергия активации, ее значение, факторы, влияющие на величину энергии активации, связь с константой скорости реакции – уравнение Аррениуса. Катализ, катализаторы, ингибиторы, общие принципы катализа. Суть механизма гомогенного катализа, примеры. Понятие о кислотно-основном катализе. Особенности механизма гетерогенного катализа, примеры. Ферментативный катализ и его особенности: активность, специфичность, размер, необходимость определенных условий. Уравнение Михаэлиса – Ментен, его значение для кинетики ферментативных реакций. Химическое равновесие и его смещение, принцип Ле–Шателье и его аналог в природе – принцип адаптивных перестроек. К Экзаменационные вопросы по модулю «Основы химической термодинамики, химической кинетики и равновесия»для студентов лечебного и педиатрического факультетов Основные понятия химической термодинамики: система (определение, классификации); основные параметры системы; функции состояния системы (внутренняя энергия, энтальпия, энтропия и факторы, влияющие на ее величину, свободная энергия Гиббса); процессы, определение, классификации. I закон термодинамики для закрытых и изолированных систем, энтальпия химической реакции. Закон Гесса и следствия из него. Биологическая роль закона Гесса и I закона термодинамики. Термодинамические критерии самопроизвольного протекания процесса. II закон термодинамики, его значение. Особенности протекания биохимических процессов в живых организмах как открытых системах. Понятие о гомеостазе. Основные понятия химической кинетики: реакции (гомогенные, гетерогенные, простые, сложные, обратимые и необратимые); скорость реакции (средняя, истинная); константа скорости химической реакции; - катализ, катализаторы, виды катализа. Скорость химических реакций. Факторы, влияющие на скорость гомогенных и гетерогенных реакций. Напишите кинетические уравнения для реакций:  СаСО3(т) t СаО(т)+ СО2(г) . Особенности кинетики сложных реакций. Понятие о молекулярности и порядке реакции. Примеры. Биологическая роль. Влияние температуры на скорость реакции. Особенности для биохимических процессов. Правило Вант-Гоффа. Уравнение Аррениуса. Энергия активации. Закон действующих масс для обратимых процессов. Константа химического равновесия, ее значение. Связь Kравн. с изменением энергии Гиббса обратимого процесса. Общие принципы катализа. Понятие о механизме гомогенного и гетерогенного катализа. Примеры. Особенности ферментативного катализа. Экзаменационные вопросы по модулю «Основы химической термодинамики, химической кинетики и равновесия» для студентов стоматологического факультета Энергетическая характеристика систем и процессов. Основные понятия: внутренняя энергия, теплота, работа, энтальпия химической реакции, стандартные энтальпии сгорания и образования. I закон термодинамики, его применение к изолированным и закрытым системам. Закон Гесса и следствия из него, значение, применение в термохимических расчетах. Термодинамические критерии самопроизвольного протекания процесса. Понятие об энтропии системы, энергии Гиббса. II закон термодинамики для изолированных систем. Общая формулировка II закона термодинамики для любых систем. Представление об особенностях протекания биохимических процессов в живых организмах. Понятие о гомеостазе. С Влияние температуры на скорость реакции, особенности для биохимических процессов. Правило Вант-Гоффа. Понятие об энергии активации, ее роли в осуществлении химических реакций. Значение уравнения Аррениуса для характеристики скорости протекания химических реакций. Понятие о катализе. Виды катализа. Особенности ферментативного катализа. Химическое равновесие, принцип Ле Шателье, его значение для характеристики смещения химического равновесия. Закон действующих масс для обратимых процессов. Связь Kравн. с изменением энергии Гиббса обратимого процесса. Роль Kравн для характеристики обратимых процессов. Экзаменационные вопросы по модулю «Основы химической термодинамики, химической кинетики и равновесия» для студентов медико-профилактического факультета Термодинамическая система. Классификация и примеры термодинамических систем. Основные параметры системы. Термодинамические процессы. Энтальпия системы, стандартная энтальпия образования, сгорания. Энтальпия химической реакции. Закон Гесса и следствия из него. Сущность 1 начала термодинамики. Математическое выражение для закрытых и изолированных систем. Понятие о внутренней энергии, работе, теплоте. Энтропия системы. Факторы, влияющие на энтропию системы. Энтропия химической реакции. II закон термодинамики для изолированных систем. Энергия Гиббса. Термодинамические критерии самопроизвольного протекания процесса. Общая формулировка II закона термодинамики для любых систем. Особенности протекания биохимических процессов в живых организмах как открытых системах. Понятие о гомеостазе. С Влияние температуры на скорость реакции. Особенности для биохимических процессов. Правило Вант-Гоффа. Уравнение Аррениуса. Энергия активации. Понятие о катализе. Особенности ферментативного катализа. Закон действующих масс для обратимых процессов. Связь значения Kравн. с изменением энергии Гиббса обратимого процесса. В экзаменационные вопросы также включены задачи и упражнения, которые являются вариативной частью и ежегодно меняются. |
